WikiDer > Фактор 1 из стромальных клеток - Википедия
В фактор 1, полученный из стромальных клеток (SDF1), также известный как Хемокин с мотивом C-X-C 12 (CXCL12), является хемокин белок что у людей кодируется CXCL12 ген на хромосома 10.[5] Он повсеместно экспрессируется во многих тканях и типах клеток.[6] Факторы 1-альфа и 1-бета, происходящие из стромальных клеток, представляют собой небольшие цитокины, которые принадлежат к хемокин семья, члены которой активируют лейкоциты и часто вызываются провоспалительными раздражителями, такими как липополисахарид, TNF, или же IL1. Хемокины характеризуются наличием 4 консервативных цистеины эта форма 2 дисульфидные связи. Их можно разделить на 2 подсемейства. В подсемействе СС остатки цистеина прилегают друг к другу. В подсемействе CXC они разделены промежуточной аминокислотой. Белки SDF1 относятся к последней группе.[5] Передача сигналов CXCL12 наблюдалась при нескольких видах рака.[7][8] В CXCL12 ген также содержит один из 27 SNP связано с повышенным риском ишемическая болезнь сердца.[9]
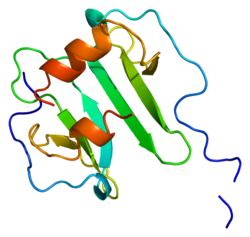
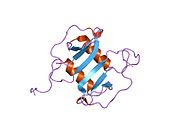
Структура
Ген
В CXCL12 ген находится на хромосоме 10 на полосе 10q11.1 и содержит 9 экзоны.[5] Этот ген производит 7 изоформы через альтернативное сращивание.[10]
Протеин
Этот белок относится к интеркринный альфа (хемокин CXC) семейство.[10] SDF-1 продуцируется в двух формах, SDF-1α / CXCL12a и SDF-1β / CXCL12b, путем попеременного сплайсинга одного и того же гена.[11] Хемокины характеризуются наличием четырех консервативных цистеины, которые образуют два дисульфидные связи. Белки CXCL12 принадлежат к группе хемокинов CXC, у которых начальная пара цистеинов разделена одним промежуточным аминокислота. Кроме того, первые 8 остатков CXCL12 N-концевой служить рецептор сайт связывания, хотя только Lys-1 и Pro-2 непосредственно участвуют в активации рецептора. Между тем, мотив RFFESH (остатки 12-17) в области петли функционирует как стыковочный сайт для связывания рецептора CXCL12.[12]
Функция
CXCL12 экспрессируется во многих тканях мышей, включая мозг, вилочковая железа, сердце, легкое, печень, почка, селезенка, и Костный мозг.[13] CXCL12 сильно хемотаксический за лимфоциты.[14][15][16][17] Во время эмбриогенеза он направляет миграцию кроветворный клетки плода печень к Костный мозг и образование крупных кровеносных сосудов. Также было показано, что передача сигналов CXCL12 регулирует экспрессию CD20 на В-клетках. CXCL12 также хемотаксик для мезенхимальные стволовые клетки и выражается в области воспалительной деструкции костей, где опосредует их подавляющее действие на остеокластогенез.[18]
В зрелом возрасте CXCL12 играет важную роль в ангиогенез путем привлечения эндотелиальных клеток-предшественников (EPCs) из костного мозга посредством механизма, зависимого от CXCR4.[19]
CXCR4, ранее называемый LESTR или фузин, является рецептором для CXCL12.[14] Это взаимодействие CXCL12-CXCR4 раньше считалось исключительным (в отличие от других хемокинов и их рецепторов), но недавно было высказано предположение, что CXCL12 может также связывать Рецептор CXCR7 (теперь называется ACKR3).[20][21][22] Блокируя CXCR4, главный корецептор для проникновения ВИЧ-1, CXCL12 действует как эндогенный ингибитор CXCR4-тропных штаммов ВИЧ-1.[23]
ЦНС
Во время эмбрионального развития CXCL12 играет роль в формировании мозжечка посредством миграции нейронов.[24] В ЦНС CXCL12 способствует пролиферации клеток, нейрогенезу (развитию и росту нервной ткани), а также нейровоспалению. Клетки-предшественники нейронов (NPC) - это стволовые клетки, которые дифференцируются в глиальные и нейрональные клетки. CXCL12 способствует их миграции к участкам поражения в головном мозге, особенно в широком диапазоне. Оказавшись в месте повреждения, NPC могут начать восстановление ткани на основе стволовых клеток.[25] Ось CXCL12 / CXCR4 обеспечивает ориентиры для аксонов и нейритов, тем самым способствуя разрастанию нейритов (нейроны, образующие проекции) и нейрогенезу.[26] Как и другие хемокины, CXCL12 участвует в миграции клеток, что способствует воспалению. Что касается ЦНС, CXCL12 играет роль в нейровоспалении, привлекая лейкоциты через гематоэнцефалический барьер.[25] однако чрезмерное производство и накопление CXCL12 может стать токсичным, а вызванное воспаление может привести к серьезным последствиям.[27]
Клиническое значение
У людей CXCL12 вовлечен в широкий спектр биомедицинских состояний, затрагивающих несколько систем органов.[28] Более того, передача сигналов CXCL12 в сочетании с передачей сигналов CXCR7 участвует в прогрессировании рака поджелудочной железы.[7] В системе мочевыводящих путей метилирование промотора CXCL12 и экспрессия PD-L1 могут быть мощными прогностическими биомаркерами биохимического рецидива у пациентов с карциномой простаты после радикальной простатэктомии, и продолжаются дальнейшие исследования, чтобы подтвердить, может ли метилирование CXCL12 помочь в стратегиях активного наблюдения.[29] В области онкологии ассоциированные с меланомой фибробласты стимулируются стимуляцией аденозинового рецептора A2B с последующей стимуляцией фактора роста фибробластов и повышенной экспрессией CXCL12.[8]
Клинический маркер
Мультилокусное исследование генетической шкалы риска, основанное на комбинации 27 локусов, включая ген CXCL12, выявило лиц с повышенным риском как эпизодов, так и рецидивов ИБС, а также увеличения клинической пользы от терапии статинами. Исследование было основано на когортном исследовании сообщества (исследование Malmo Diet and Cancer) и четырех дополнительных рандомизированных контролируемых исследованиях когорт первичной профилактики (JUPITER и ASCOT) и когорт вторичной профилактики (CARE и PROVE IT-TIMI 22).[9]
Рассеянный склероз
Неврологическое заболевание, возникающее в результате неправильного взаимодействия иммунной и нервной систем в рассеянный склероз. РС характеризуется демиелинизацией нервов из-за того, что иммунная система организма атакует ЦНС. Повышенные уровни CXCL12 наблюдаются в спинномозговой жидкости пациентов с РС. CXCL12 пересекает гематоэнцефалический барьер и причины нейровоспаление что способствует повреждению аксонов и, следовательно, прогрессированию рассеянного склероза.[30][ненадежный медицинский источник]
Болезнь Альцгеймера
Хотя CXCL12 может быть вредным для людей с рассеянным склерозом, недавние исследования предполагают, что этот хемокин может быть полезным для снижения прогрессирования пациентов с болезнью Альцгеймера. Болезнь Альцгеймера - еще одно неврологическое заболевание и наиболее распространенная форма деменции, при которой когнитивные способности значительно ухудшаются. Одной из основных характеристик болезни Альцгеймера является накопление бляшки в головном мозге, известной как бета-амилоид. Нейрозащитные аспекты CXCL12 у мышей с этими бляшками / болезнью Альцгеймера. PAK - это белок, связанный с поддержанием дендритных шипов, которые необходимы в синапсах для получения информации от аксонов. Неверная локализация PAK происходит у пациентов с болезнью Альцгеймера, однако предварительная обработка нейронов мышей CXCL12 показала подавление этой неправильной локализации.[31][ненадежный медицинский источник] Кроме того, эта предварительная обработка CXCL уменьшала распространенность апоптоза и окислительного повреждения, обычно вызываемого присутствием бета-амилоидных бляшек.[31]
Как мишень для наркотиков
Хемокины и рецепторы хемокинов, из которых выделяется CXCR, регулируют множество процессов, таких как морфогенез, ангиогенез и иммунные ответы, и считаются потенциальными мишенями для разработки лекарств. В системе желудочно-кишечного тракта ось CXCL12-CXCR4 исследуется в качестве противофиброзной терапии при лечении хронического панкреатита.[32] Например, блокировка CXCR4, рецептор для CXCL12, с Plerixafor (AMD-3100) увеличивал эффективность комбретастатина на мышиной модели рака молочной железы, предположительно, предотвращая рекрутирование макрофагов в опухоли.[15][16] AMD-3100 также широко используется в сочетании с G-CSF для мобилизации гемопоэтических стволовых клеток в кровоток, что позволяет собирать пересадка костного мозга.[33]
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000107562 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000061353 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ а б c «Ген Entrez: хемокин CXCL12 (мотив C-X-C), лиганд 12 (фактор 1, происходящий из стромальных клеток)».
- ^ «BioGPS - ваша система генного портала». biogps.org. Получено 11 октября 2016.
- ^ а б Гуо Дж.С., Ли Дж., Чжоу Л., Ян Дж.Й., Чжан З.Г., Лян З.Й., Чжоу В.Х., Ю Л., Чжан Т.П., Чжао Ю.П. (август 2016 г.). «Ось CXCL12-CXCR7 способствует инвазивному фенотипу рака поджелудочной железы». Oncotarget. 7 (38): 62006–62018. Дои:10.18632 / oncotarget.11330. ЧВК 5308707. PMID 27542220.
- ^ а б Соррентино C, Miele L, Porta A, Pinto A, Morello S (август 2016 г.). «Активация аденозинового рецептора A2B в меланоме B16 индуцирует экспрессию CXCL12 в FAP-положительных стромальных клетках опухоли, усиливая прогрессирование опухоли». Oncotarget. 7 (39): 64274–64288. Дои:10.18632 / oncotarget.11729. ЧВК 5325441. PMID 27590504.
- ^ а б Mega JL, Stitziel NO, Smith JG, Chasman DI, Caulfield MJ, Devlin JJ, Nordio F, Hyde CL, Cannon CP, Sacks FM, Poulter NR, Sever PS, Ridker PM, Braunwald E, Melander O, Kathiresan S, Sabatine MS (Июнь 2015 г.). «Генетический риск, события ишемической болезни сердца и клиническая польза от терапии статинами: анализ испытаний первичной и вторичной профилактики». Ланцет. 385 (9984): 2264–71. Дои:10.1016 / S0140-6736 (14) 61730-X. ЧВК 4608367. PMID 25748612.
- ^ а б «CXCL12 - предшественник фактора 1, полученный из стромальных клеток - Homo sapiens (человек) - ген и белок CXCL12». UniProt.
- ^ Де Ла Луз Сьерра М., Ян Ф., Наразаки М., Сальвуччи О, Дэвис Д., Ярчоан Р., Чжан Х. Х., Фалес Х, Тосато Дж. (Апрель 2004 г.). «Дифференциальная обработка стромального фактора-1альфа и стромального фактора-1бета объясняет функциональное разнообразие». Кровь. 103 (7): 2452–9. Дои:10.1182 / кровь-2003-08-2857. PMID 14525775.
- ^ Крамп М.П., Гонг Дж. Х., Лётчер П., Раджаратнам К., Амара А., Арензана-Сейсдедос Ф., Вирелизье Дж. Л., Баггиолини М., Сайкс Б. Д., Кларк-Льюис I. (декабрь 1997 г.). «Структура раствора и основа функциональной активности фактора-1, полученного из стромальных клеток; диссоциация активации CXCR4 от связывания и ингибирования ВИЧ-1». Журнал EMBO. 16 (23): 6996–7007. Дои:10.1093 / emboj / 16.23.6996. ЧВК 1170303. PMID 9384579.
- ^ Schrader AJ, Lechner O, Templin M, Dittmar KE, Machtens S, Mengel M, Probst-Kepper M, Franzke A, Wollensak T., Gatzlaff P, Atzpodien J, Buer J, Lauber J (апрель 2002 г.). «Экспрессия CXCR4 / CXCL12 и передача сигналов при раке почки». Британский журнал рака. 86 (8): 1250–6. Дои:10.1038 / sj.bjc.6600221. ЧВК 2375348. PMID 11953881.
- ^ а б Bleul CC, Fuhlbrigge RC, Casasnovas JM, Aiuti A, Springer TA (сентябрь 1996 г.). «Высокоэффективный хемоаттрактант лимфоцитов, фактор 1, полученный из стромальных клеток (SDF-1)». Журнал экспериментальной медицины. 184 (3): 1101–9. Дои:10.1084 / jem.184.3.1101. ЧВК 2192798. PMID 9064327.
- ^ Ара Т., Накамура И., Эгава Т., Сугияма Т., Абе К., Кисимото Т., Мацуи Ю., Нагасава Т. (апрель 2003 г.). «Нарушение колонизации гонад первичными зародышевыми клетками у мышей, лишенных хемокина, фактора-1, происходящего из стромальных клеток (SDF-1)». Труды Национальной академии наук Соединенных Штатов Америки. 100 (9): 5319–23. Дои:10.1073 / pnas.0730719100. ЧВК 154343. PMID 12684531.
- ^ Аскари А.Т., Унзек С., Попович З. Б., Гольдман С. К., Форуди Ф, Кедровски М., Ровнер А., Эллис С. Г., Томас Дж. Д., ДиКорлето П. Е., Тополь Е. Д., Пенн М. С. (август 2003 г.). «Влияние фактора 1, полученного из стромальных клеток, на возвращение стволовых клеток и регенерацию тканей при ишемической кардиомиопатии». Ланцет. 362 (9385): 697–703. Дои:10.1016 / S0140-6736 (03) 14232-8. PMID 12957092. S2CID 24354002.
- ^ Ма К., Джонс Д., Боргесани П. Р., Сегал Р. А., Нагасава Т., Кишимото Т., Бронсон Р. Т., Спрингер Т. А. (август 1998 г.). «Нарушение В-лимфопоэза, миелопоэза и нарушение миграции нейронов мозжечка у мышей с дефицитом CXCR4 и SDF-1». Труды Национальной академии наук Соединенных Штатов Америки. 95 (16): 9448–53. Дои:10.1073 / пнас.95.16.9448. ЧВК 21358. PMID 9689100.
- ^ Такано Т., Ли Й.Дж., Кукита А., Ямаза Т., Аюкава Ю., Морияма К., Уехара Н., Номияма Х, Кояно К., Кукита Т. (2014). «Мезенхимальные стволовые клетки заметно подавляют воспалительное разрушение костей у крыс с адъювантом-индуцированным артритом». Лабораторные исследования. 94 (3): 286–96. Дои:10.1038 / labinvest.2013.152. PMID 24395111.
- ^ Чжэн Х, Фу Г, Дай Т, Хуан Х (2007). «Миграция эндотелиальных клеток-предшественников, опосредованная фактором-1альфа / CXCR4, полученным из стромальных клеток, через путь передачи сигнала PI3K / Akt / eNOS». Журнал сердечно-сосудистой фармакологии. 50 (3): 274–80. Дои:10.1097 / FJC.0b013e318093ec8f. PMID 17878755. S2CID 13616442.
- ^ Balabanian K, Lagane B, Infantino S, Chow KY, Harriague J, Moepps B, Arenzana-Seisdedos F, Thelen M, Bachelerie F (2005). «Хемокин SDF-1 / CXCL12 связывается и передает сигнал через сиротский рецептор RDC1 в Т-лимфоцитах». Журнал биологической химии. 280 (42): 35760–6. Дои:10.1074 / jbc.M508234200. PMID 16107333.
- ^ Бернс Дж. М., Саммерс BC, Ван И, Меликиан А., Берахович Р., Мяо З, Пенфолд М. Дж., Саншайн М. Дж., Литтман Д. Р., Куо С. Дж., Вей К., Макмастер Б. Е., Райт К., Ховард М. С., Шалл Т. Дж. (2006). «Новый хемокиновый рецептор для SDF-1 и I-TAC, участвующий в выживании клеток, клеточной адгезии и развитии опухолей». Журнал экспериментальной медицины. 203 (9): 2201–13. Дои:10.1084 / jem.20052144. ЧВК 2118398. PMID 16940167.
- ^ Круз-Оренго Л., Холман Д. В., Дорси Д., Чжоу Л., Чжан П., Райт М., МакКэндлесс Е. Е., Патель Дж. Р., Люкер Г. Д., Литтман Д. Р., Рассел Дж. Х., Кляйн Р. С. (2011). «CXCR7 влияет на проникновение лейкоцитов в паренхиму ЦНС, контролируя содержание CXCL12 в аблюминальной полости во время аутоиммунитета». Журнал экспериментальной медицины. 208 (2): 327–39. Дои:10.1084 / jem.20102010. ЧВК 3039853. PMID 21300915.
- ^ Оберлин Е., Амара А., Башелери Ф, Бессия С., Вирелизье Дж. Л., Аренцана-Сейсдедос Ф, Шварц О, Херд Дж. М., Кларк-Льюис I, Леглер Д. Ф., Лётчер М., Баггиолини М., Мозер Б. «Хемокин CXC SDF-1 является лигандом для LESTR / фузина и предотвращает заражение ВИЧ-1, адаптированным к Т-клеточной линии» (PDF). Природа. 382 (6594): 833–5. Дои:10.1038 / 382833a0. PMID 8752281.
- ^ Баджетто А., Бонавиа Р., Барберо С., Флорио Т., Скеттини Г. (июль 2001 г.). «Хемокины и их рецепторы в центральной нервной системе». Границы нейроэндокринологии. 22 (3): 147–84. Дои:10.1006 / frne.2001.0214. PMID 11456467. S2CID 29689159.
- ^ а б Ли М., Хейл Дж. С., Рич Дж. Н., Рансохофф Р. М., Латиа Дж. Д. (октябрь 2012 г.). «Хемокин CXCL12 при нейродегенеративных заболеваниях: сигнал SOS для восстановления стволовых клеток». Тенденции в неврологии. 35 (10): 619–28. Дои:10.1016 / j.tins.2012.06.003. ЧВК 3461091. PMID 22784557.
- ^ Гийон А. (март 2014 г.). «Хемокин CXCL12 и его рецепторы как основные участники взаимодействия между иммунной и нервной системами». Границы клеточной неврологии. 8: 65. Дои:10.3389 / fncel.2014.00065. ЧВК 3944789. PMID 24639628.
- ^ Гийон А. (2014). «Хемокин CXCL12 и его рецепторы как основные участники взаимодействия между иммунной и нервной системами». Границы клеточной неврологии. 8: 65. Дои:10.3389 / fncel.2014.00065. ЧВК 3944789. PMID 24639628.
- ^ Поццобон Т., Гольдони Г., Виола А, Молон Б. (сентябрь 2016 г.). «Передача сигналов CXCR4 в здоровье и болезни». Письма иммунологии. 177: 6–15. Дои:10.1016 / j.imlet.2016.06.006. PMID 27363619.
- ^ Гольц Д., Холмс Э., Гевенслебен Х, Зайлер В., Дитрих Дж, Юнг М., Рёлер М., Меллер С., Эллингер Дж., Кристиансен Г., Дитрих Д. (июль 2016 г.). «Метилирование промотора CXCL12 и экспрессия PD-L1 как прогностические биомаркеры у пациентов с раком простаты». Oncotarget. 7 (33): 53309–53320. Дои:10.18632 / oncotarget.10786. ЧВК 5288188. PMID 27462860.
- ^ Крумбхольц М., Тейл Д., Чепок С., Хеммер Б., Кивисакк П., Рансохофф Р. М., Хофбауэр М., Фарина С., Дерфус Т., Хартл С., Ньюкомб Дж., Хольфельд Р., Майнл Е. (январь 2006 г.). «Хемокины при рассеянном склерозе: повышающая регуляция CXCL12 и CXCL13 по-разному связана с привлечением иммунных клеток ЦНС». Мозг: журнал неврологии. 129 (Pt 1): 200–11. Дои:10.1093 / мозг / awh680. PMID 16280350.
- ^ а б Раман Д., Милатович С.З., Милатович Д., Сплиттгербер Р., Фан Г.Х., Ричмонд А. (ноябрь 2011 г.). «Хемокины, макрофагальный воспалительный белок-2 и фактор-1α, полученный из стромальных клеток, подавляют нейротоксичность, вызванную амилоидом β». Токсикология и прикладная фармакология. 256 (3): 300–13. Дои:10.1016 / j.taap.2011.06.006. ЧВК 3236026. PMID 21704645.
- ^ Neesse A, Ellenrieder V (сентябрь 2016 г.). «Ось NEMO-CXCL12 / CXCR4: новая точка зрения для антифибротической терапии хронического панкреатита?». Кишечник. 66 (2): gutjnl – 2016–312874. Дои:10.1136 / gutjnl-2016-312874. PMID 27590996. S2CID 3493909.
- ^ Де Клерк Э. (2019) Mozobil (R) (Plerixafor, AMD3100), через 10 лет после его утверждения Управлением по контролю за продуктами и лекарствами США. Антивир Chem Chemother 27: 1.
дальнейшее чтение
- Куча М., Река Р., Миекус К., Ванцек Дж., Вояковски В., Яновска-Вечорек А., Ратайчак Дж., Ратайчак М.З. (август 2005 г.). «Торговля нормальными стволовыми клетками и метастазирование раковых стволовых клеток включает сходные механизмы: центральная роль оси SDF-1-CXCR4». Стволовые клетки. 23 (7): 879–94. Дои:10.1634 / стволовые клетки.2004-0342. PMID 15888687. S2CID 22504846.
- Kryczek I, Wei S, Keller E, Liu R, Zou W. (март 2007 г.). «Фактор стромы (SDF-1 / CXCL12) и патогенез опухолей человека». Американский журнал физиологии. Клеточная физиология. 292 (3): C987–95. Дои:10.1152 / ajpcell.00406.2006. PMID 16943240. S2CID 7423893.
- Стеллос К., Гаваз М. (март 2007 г.). «Тромбоциты и фактор-1, полученный из стромальных клеток в рекрутинге клеток-предшественников». Семинары по тромбозу и гемостазу. 33 (2): 159–64. Дои:10.1055 / с-2007-969029. PMID 17340464.
- Ван Дж, Лю Х, Лу Х, Цзян Ц, Цуй Х, Ю Л, Фу Х, Ли Кью, Ван Дж (март 2015 г.). «Субпопуляция CXCR4 (+) CD45 (-) BMMNC превосходит нефракционированные BMMNC в плане защиты после ишемического инсульта у мышей». Мозг, поведение и иммунитет. 45: 98–108. Дои:10.1016 / j.bbi.2014.12.015. ЧВК 4342301. PMID 25526817.
- Арья М., Ахмед Х., Силхи Н., Уильямсон М., Пател Х.Р. (2007). «Клиническое значение и терапевтические последствия основного взаимодействия CXCL12-CXCR4 (хемокиновый лиганд-рецептор) в миграции раковых клеток». Биология опухоли. 28 (3): 123–31. Дои:10.1159/000102979. PMID 17510563. S2CID 44356923.