WikiDer > Трансдермальный
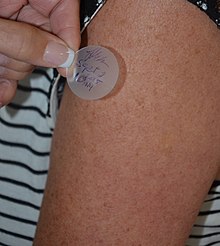
Трансдермальный это путь введения при этом активные ингредиенты доставляются через кожу для системного распределения. Примеры включают трансдермальные пластыри Используется для доставки лекарств. Препарат вводится в виде пластыря или мази, которые доставляют лекарство в кровоток для системного действия.
Методы
Препятствия
Хотя кожа является большой и логичной мишенью для доставки лекарств, ее основные функции ограничивают ее полезность для этой цели. Кожа в основном защищает тело от внешних воздействий (например, вредных веществ и микроорганизмов) и удерживает все жидкости организма. Он должен быть жестким, но достаточно гибким, чтобы допускать движение. Липиды в нашей коже служат плохими проводниками электричества и, следовательно, могут защитить нас от электрических токов, если в этом возникнет необходимость.
Человеческая кожа состоит из двух важных слоев: (1) Эпидермис и (2) Дермы. Для трансдермальной доставки лекарства должны пройти через два подслоя эпидермиса, чтобы достичь микроциркуляции дермы.
В Роговой слой представляет собой верхний слой кожи и варьируется по толщине от примерно десяти до нескольких сотен микрометров, в зависимости от области тела.[1] Он состоит из слоев мертвых, уплощенных кератиноцитов, окруженных липидной матрицей, которые вместе действуют как сложная система из кирпича и раствора.[2]
Роговой слой обеспечивает наиболее значительный барьер для диффузии. Фактически, роговой слой является барьером приблизительно для 90% трансдермальных применений лекарственных препаратов. Однако почти все молекулы в той или иной степени проникают в него.[3] Под роговым слоем находится жизнеспособный эпидермис. Этот слой примерно в десять раз толще рогового слоя; однако диффузия здесь происходит намного быстрее из-за большей степени гидратации живых клеток жизнеспособного эпидермиса. Под эпидермисом находится дерма, которая имеет толщину примерно один миллиметр, что в 100 раз превышает толщину рогового слоя. Дерма содержит мелкие сосуды, которые распределяют лекарства в системный кровоток и регулируют температуру, система, известная как микроциркуляция кожи.[2][3]
Трансдермальные пути
Есть два основных пути, по которым лекарства могут проникать через кожу в системный кровоток. Более прямой путь известен как трансцеллюлярный путь.
Трансклеточный путь
Таким путем лекарственные препараты проникают через кожу, непосредственно проходя через фосфолипидные мембраны и цитоплазму мертвых кератиноцитов, составляющих роговой слой.
Хотя это путь кратчайшего расстояния, лекарства обладают значительным сопротивлением проникновению. Это сопротивление вызвано тем, что лекарственные препараты должны пересечь липофильную мембрану каждой клетки, затем гидрофильное клеточное содержимое, содержащее кератин, и затем еще раз фосфолипидный бислой клетки. Эта серия шагов повторяется много раз, чтобы пройти через всю толщину рогового слоя.[1][2]
Межклеточный путь
Другой более распространенный путь через кожу - межклеточный. Лекарства, проходящие через кожу этим путем, должны проходить через небольшие промежутки между клетками кожи, что делает путь более извилистым. Хотя толщина рогового слоя составляет всего около 20 мкм, фактический путь диффузии большинства молекул, пересекающих кожу, составляет порядка 400 мкм.[4] 20-кратное увеличение фактического пути проникновения молекул значительно снижает скорость проникновения лекарства.[3]
Недавние исследования показали, что межклеточный путь может быть значительно улучшен, если уделить внимание физической химии системы, солюбилизирующей активный фармацевтический ингредиент, что значительно повысит эффективность доставки полезной нагрузки и обеспечит доставку большинства соединений этим путем.[5][6][7]
Микроиглы
Было предложено, чтобы этот раздел был Трещина в другую статью под названием доставка лекарств с помощью микроигл. (Обсуждать) (Июль 2017 г.) |
Третий путь к разрушению рогового слоя - крошечные микроканалы, созданные медицинским микронидлинг устройство, которого существует множество марок и вариантов.[8] Исследования в Марбургском университете, Германия, с использованием стандартной диффузионной ячейки Франца показали, что этот подход эффективен для повышения проницаемости кожи как для липофильных, так и для гидрофильных соединений.[9]
Подход микронидлинга также рассматривается как вакцина о будущем'.[10] Микроиглы могут быть полыми, твердыми, покрытыми, растворяющимися или образующими гидрогель.[11] Некоторые из них имеют одобрение регулирующих органов.[11] Микроиглы / пластыри могут использоваться для доставки лекарства с наночастицами.[12]
Устройства и составы
Устройства и составы для трансдермально вводимых веществ включают:
- Трансдермальный пластырь
- Трансдермальный гель
- специально разработанные спреи
Рекомендации
- ^ а б Флинн, Г.Л. (1996). «Кожная и трансдермальная доставка: процессы и системы доставки». В Современная фармацевтика, Banker, G.S & Rhodes, C.T, ред. Нью-Йорк, Нью-Йорк: Марсель Деккер, 239-299.M
- ^ а б c Маккарли К.Д., Бунге А.Л. (2001). «Обзор фармакокинетических моделей кожной абсорбции». J Pharm Sci. 90 (11): 1699–1719. Дои:10.1002 / jps.1120. PMID 11745728.
- ^ а б c Морганти П., Руокко Э., Вольф Р., Руокко В. (2001). «Чрескожные системы всасывания и доставки». Клин дерматол. 19 (4): 489–501. Дои:10.1016 / s0738-081x (01) 00183-3. PMID 11535394.CS1 maint: несколько имен: список авторов (ссылка на сайт)
- ^ Хэдграфт Дж (2001). «Модуляция барьерной функции кожи». Кожа Pharmacol Appl Skin Physiol. 14 (1): 72–81. Дои:10.1159/000056393. PMID 11509910. S2CID 33920480.
- ^ AT Tucker, 1 Z. Chik, 2 L. Michaels, 3 K. Kirby, 4 MP Seed, 5 A. Johnston2 и CAS Alam5 Исследование комбинированного чрескожного местного анестетика и системы TDS для венепункционной анестезии, 2006 г., 61, стр. 123 –126
- ^ З. Чик, А. Джонстон, А. Т. Такер, С. Л. Чу, Л. Майклс и С. А. С. Алам Фармакокинетика новой системы трансдермальной доставки тестостерона, TDS® -тестостерона у здоровых мужчин Дои:10.1111 / j.1365-2125.2005.02542.x
- ^ З. Чик, А. Джонстон, К. Кирби, A.T. Такер и К.А. Алам; Коррекция эндогенных концентраций тестостерона влияет на биоэквивалентность и демонстрирует превосходство TDS®-тестостерона над Androgel® Int J Clin Pharmacol Ther. 2009 Апрель; 47 (4): 262-8.
- ^ Колли, К.С., Каллури, Х., Десаи, Н.Н. И Банга, А.К. (2007). «Дермароллер как альтернативное средство для преодоления барьера рогового слоя». Колледж фармации и медицинских наук, Университет Мерсера, Атланта, Джорджия, 30341, США.
- ^ Верма, Д. & Fahr, A. "Исследование эффективности нового устройства для осаждения веществ в более глубокие слои кожи: Dermaroller" Institut für Pharmazeutische Technologie und Biopharmazie, Philipps-Universität Marburg, Марбург, Германия.
- ^ Джудиче Э.Л., Кэмпбелл Д.Д. (2006). «Безыгольная доставка вакцины». Adv Drug Deliv Rev. 58 (1): 68–89. Дои:10.1016 / j.addr.2005.12.003. PMID 16564111.
- ^ а б Ита, К (2015). «Трансдермальная доставка лекарств с помощью микроигл - возможности и проблемы». Фармацевтика. 7 (3): 90–105. Дои:10.3390 / фармацевтика7030090. ЧВК 4588187. PMID 26131647.
- ^ Ларранета; и другие. (2016). «Микроиглы: новый рубеж в области наномедицины». Pharm. Res. 33 (5): 1055–73. Дои:10.1007 / s11095-016-1885-5. ЧВК 4820498. PMID 26908048.