WikiDer > Площадь пострема
| Площадь пострема | |
|---|---|
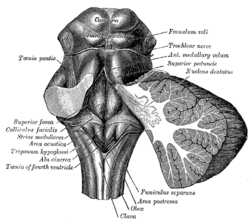 Ромбовидная ямка. (Площадь пострема отмечена внизу по центру.) | |
 Описание заднего вида хвостового отдела ствола головного мозга человека (Area postrema # 8) | |
| Подробности | |
| Часть | Медулла |
| Идентификаторы | |
| Акроним (ы) | AP |
| MeSH | D031608 |
| NeuroNames | 772 |
| НейроЛекс Я БЫ | birnlex_2636 |
| TA98 | A14.1.04.258 |
| TA2 | 6009 |
| FMA | 72607 |
| Анатомические термины нейроанатомии | |
В область пострема, парная структура в продолговатый мозг из мозговой ствол,[1] это окжелудочковый орган имея проницаемый капилляры и сенсорные нейроны которые позволяют выполнять двойную роль обнаруживать циркулирующие химические посланники в крови и преобразовывать их в нейронные сигналы и сети.[2][3][4] Его положение прилегает к двустороннему ядра одиночного тракта и роль сенсорного преобразователя позволяет ему интегрировать кровь в мозг автономные функции. Такие роли области постремы включают обнаружение циркулирующих гормоны участвует в рвота, жажда, голод, и артериальное давление контроль.[1][5]
Структура
Постремная зона представляет собой парный бугорок, обнаруживаемый на нижне-задней границе четвертый желудочек.[1][5] Специализированный эпендимные клетки находятся в области пострема. Эти клетки немного отличаются от большинства эпендимных клеток (эпендимоцитов), образуя одноклеточную эпителиальную выстилку желудочков и центральный канал. Область пострема отделена от блуждающий треугольник посредством Funiculus separans, тонкий полупрозрачный гребень.[1][5] Блуждающий треугольник перекрывает дорсальное ядро блуждающего нерва и расположен на каудальном конце ромбовидная ямка или «дно» четвертого желудочка. Площадь пострема расположена прямо перед obex, нижняя вершина каудального дна желудочков. Как семенной канатик, так и постремная зона имеют одинаковое толстое покрытие таницитов, содержащее эпендиму. Эпендима и танициты может участвовать в перевозке нейрохимические вещества в и из спинномозговая жидкость из его клеток или соседних нейронов, глии или сосудов. Эпендима и танициты также могут участвовать в хеморецепции.[1][5]
Область пострема считается окжелудочковый орган из-за его близости к желудочковая система.[2] В морфологический этюд, зона пострема капилляры в вентральный Подобласть area postrema оказалась относительно непроницаемой, как и области мозга, тогда как медиальный и спинной капилляры области postrema имели микроскопические характеристики высокой проницаемости, характеристика, называемая синусоидальный.[6] Плотность субрегиональных капилляров в области postrema была максимальной около межжелудочковой границы и почти вдвое больше плотности капилляров соседних одиночное ядро (SN) и дорсальное моторное ядро блуждающего нерва.[6] А таницит барьер частично компенсирует высокую проницаемость капилляров в области постремы.[7]
Физиологический субрегиональные исследования ареала Пострема показали, что его объем крови относительно большой, и кровоток и время прохождения маркеров крови относительно невелико, что усиливает способность распознавания циркулирующих соединений, таких как гормоны или передатчики.[8]

Подключения
Область пострема соединяется с одиночное ядро, или nucleus tractus solitarii (NTS), и другие центры вегетативного контроля в мозговой ствол. Он возбуждается висцеральными афферентными импульсами (симпатическими и блуждающими), возникающими из желудочно-кишечный тракт и другие периферийные триггерные зоны, и по гуморальные факторы.[2] Постремная зона составляет часть дорсального комплекса блуждающего нерва, который является критическим местом завершения афферентные нервные волокна блуждающего нерва, вместе с дорсальное моторное ядро блуждающего нерва и НТС.
Тошнота скорее всего индуцируется стимуляцией области postrema через ее связь с NTS, что может служить началом пути, запускающего рвоту в ответ на различные рвотные вещества. Однако эта структура не играет ключевой роли при тошноте, вызванной активацией волокон блуждающего нерва или движением, и ее функция при радиационной рвоте остается неясной.[9]
Потому что район пострема и специализированный район НТС имеют проницаемые капилляры,[2] пептиды и другие гормональные сигналы В крови есть прямой доступ к нейронам областей мозга, играющих жизненно важную роль в вегетативном контроле над телом.[2][6] В результате пострема считается местом интеграции различных физиологических сигналов в крови, когда они поступают в Центральная нервная система.[2][3]
Функция
Хеморецепция
Площадь пострема, одна из окружные желудочковые органы,[10] обнаруживает токсины в кровь и действует как центр, вызывающий рвоту. Постремная зона является критическим центром гомеостатической интеграции гуморальных и нейронных сигналов благодаря своей функции триггерная зона хеморецептора за рвота в ответ на рвотные препараты. Это плотно васкуляризованная структура с субрегиональной капиллярной специализацией для обеспечения высокой проницаемости для циркулирующих сигналов крови, что позволяет обнаруживать различные химические посредники в крови и спинномозговая жидкость.[4][6] Капиллярный кровоток, по-видимому, уникально медленен в области постремы, увеличивая время контакта гормонов с кровью, чтобы взаимодействовать с нейронными рецепторами, участвующими в регуляции кровяного давления, биологических жидкостей и рвотных реакций.[4][8]
Вегетативная регуляция
В фенестрированные синусоидальные капилляры района пострема и специализированного района НТС делают этот регион мозговое вещество имеет решающее значение для вегетативного контроля над различными физиологическими системами, включая сердечно-сосудистую систему и системы, контролирующие питание и обмен веществ.[2][6] Ангиотензин II вызывает дозозависимое увеличение артериальное кровяное давление без значительных изменений в частота сердцебиения, эффект, опосредованный областью постремы.[11]
Клиническое значение
Повреждать
Повреждение области постремы, вызванное, прежде всего, поражением или абляция, препятствует нормальным функциям постремной области. Эта абляция обычно проводится хирургическим путем и с целью выявления точного воздействия постремной области на остальное тело. Поскольку постремная область действует как точка входа в мозг для информации от сенсорные нейроны В желудке, кишечнике, печени, почек, сердце и других внутренних органах различные физиологические рефлексы полагаются на постремную область для передачи информации. Постремная зона непосредственно контролирует химический статус организма. Поражения постремной области иногда называют «центральной ваготомией», потому что они лишают мозг возможности контролировать физиологическое состояние тела через блуждающий нерв.[12] Таким образом, эти поражения служат для предотвращения обнаружения ядов и, следовательно, предотвращения срабатывания естественной защиты организма. В одном примере эксперименты, проведенные Bernstein et al. на крысах показали, что пораженная область постремы препятствовала обнаружению хлорид лития, который может стать токсичным при высоких концентрациях. Поскольку крысы не могли обнаружить химическое вещество, они не могли использовать психологическую процедуру, известную как отвращение к вкусу кондиционирование, заставляя крысу постоянно глотать раствор сахарина с литиевыми парами. Эти данные показывают, что крысы с поражением области постремы не приобретают нормального условного отвращения к вкусу, когда хлорид лития используется как безусловный раздражитель. В дополнение к простому отвращению к вкусу, крысы с поражением области постремы не смогли выполнить другие поведенческие и физиологические реакции, связанные с введением токсина и присутствующие в контрольной группе, такие как лежание на животе, задержка опорожнения желудка и переохлаждение.[13] Такие эксперименты подчеркивают важность области postrema не только для идентификации токсичных веществ в организме, но и для многих физических реакций на токсин.
Эффект дофамина
Область пострема также играет важную роль в обсуждении болезнь Паркинсона. Препараты, которые лечат болезнь Паркинсона, используют дофамин оказывают сильное влияние на область постремы. Эти препараты стимулируют передачу дофамина и пытаются нормализовать двигательные функции, на которые влияют: Болезнь Паркинсона. Это работает, потому что нервные клетки, в частности, базальный ганглий, который играет решающую роль в регуляции движений и является первичным местом патологии болезни Паркинсона, используют дофамин в качестве своего нейромедиатора и активируются лекарствами, которые повышают концентрацию дофамина или работают, чтобы стимулировать рецепторы дофамина. Допамину также удается стимулировать постремную область, поскольку в этой части мозга находится высокая плотность дофаминовых рецепторов. Постремная зона очень чувствительна к изменениям токсичности крови и ощущает присутствие ядовитых или опасных веществ в крови. В качестве защитного механизма постремная зона вызывает рвоту, чтобы предотвратить дальнейшую интоксикацию. Высокая плотность дофаминовых рецепторов в области постремы делает ее очень чувствительной к препаратам, повышающим дофамин. Стимуляция дофаминовых рецепторов в области постремы активирует эти рвотные центры мозга; вот почему тошнота - один из наиболее частых побочных эффектов противопаркинсонические препараты.[14]
История
Область postrema была впервые названа и расположена в грубой анатомии мозга Магнусом. Густав Ретциус, шведский анатом, антрополог и профессор гистология. В 1896 году он опубликовал двухтомную монографию по макроанатомии человеческого мозга, в которой упоминалась postrema.[нужна цитата] В 1975 году были опубликованы свидетельства наличия нейронов в области postrema у нескольких видов млекопитающих.[15]
Ученые стали проявлять все больший интерес к исследованиям рвоты в 1950-х годах, возможно, отчасти из-за возросшего понимания обществом лучевая болезнь, состояние, при котором многие пациенты, рвавшие после радиационного облучения, умерли. Исследования показали наличие двух областей в головном мозге, связанных с рвотой: одна - хемосенсор для рвоты без координирующей функции, расположенный в четвертый желудочек и два, координатор рвоты без хемосенсорной функции, расположенный в латеральная ретикулярная формация из продолговатый мозг.[нужна цитата]
В 1953 году Борисон и Ван определили, что область хемосенсора действует как зона запуска рвоты в стволе мозга, которую они назвали зоной запуска хеморецептора (CTZ) для рвоты. Используя кошек и собак в качестве модельных организмов, они обнаружили, что удаление этой триггерной зоны из головного мозга позволило предотвратить рвоту у животных сразу после инъекции определенных химических веществ в кровь, продемонстрировав наличие связи между триггерной зоной и акт рвоты. ЗТЗ анатомически располагалась в постремной зоне продолговатого мозга. Постремная зона была анатомически идентифицирована и названа почти 60 лет назад, но ее функция оставалась неизвестной, пока ее роль в рвоте не была позже подтверждена.[16]
Текущее исследование
Сегодня во всем мире продолжаются исследования функций области постремы. Помимо своей роли в возникновении рвоты, как это интенсивно изучали исследователи середины 1900-х годов, активность области постремы была тесно связана с другими вегетативными функциями, такими как регулирование приема пищи, гомеостаз жидкости организма и сердечно-сосудистый регулирование посредством поведенческих исследований и электрофизиологический исследования. В 2007 году в Японии было проведено исследование механизма возбудимости нейронов области postrema внеклеточным АТФ. Зажим напряжения На срезах головного мозга крыс использовали методы регистрации целых клеток. Результаты показали, что большинство ответов на АТФ являются возбуждающими и опосредуются определенными пуриноцепторами P2, обнаруженными в области постремы.[17] Роль области postrema в обусловленном вкусом отвращении и предпочтении была изучена в 2001 году исследователями из Бруклинский колледж на Городской университет Нью-Йорка. В эксперименте проверялось влияние поражений области постремы у крыс на их способность обучаться отвращению к ароматизаторам, обусловленному вкусом, в сочетании с лечением токсичными лекарствами, что действительно показало, что поражения области постремы приводят к нарушению обучения отвращению к вкусам.[18]В 2009 году исследование отслеживало развитие области постремы с использованием модели обезьяны макаки в попытке идентифицировать и охарактеризовать нейротрансмиссия в этой области, а также для устранения несоответствий между исследованиями. В итоге эти ученые обнаружили, что предыдущие исследования предполагают норадреналин и / или дофамин вызывают флуоресценцию CA в области postrema macaque-CA, что означает катехоламинергические или полученные из амина и функционирующие как нейротрансмиттер или же гормон или оба. Однако исследование обнаружило доказательства секреции нейромедиаторов вместо их высвобождения в везикулах. Кроме того, их выводы пришли к выводу ГАМК является основным нейротрансмиттером в области постремы, а не глутамат. Текущие исследования продолжают раскрывать несоответствия между различными моделями исследований крыс, кошек, а теперь и макак.[19]
Возможные способы лечения
В исследовании 2002 года, проведенном в Японии, тестировалось лекарство, которое может быть использовано для сдерживания рвотной реакции на препараты, повышающие концентрацию дофамина. В исследовании изучали рвоту, вызванную морфином, у хорьков, объясняя, что воздействие морфина вызывает высвобождение дофамина в организме. продолговатый мозг и в области постремы, активируя опиатные рецепторы, которые, в свою очередь, вызывали рвоту у хорьков. Тем не менее предварительное лечение 6-гидроксидофамином, дофаминергическим нейротоксином, значительно уменьшило количество эпизодов рвоты у хорьков после воздействия морфина. Этот нейротоксин снижает уровень дофамина, норадреналина и гомованиллиновой кислоты, метаболита дофамина, и, как известно, разрушает норадренергические и дофаминергические нейроны. Здесь 6-гидроксидофамин вводили непосредственно в продолговатый мозг, но не в другие части мозга. Это исследование показывает, как можно управлять дофаминергическим путем в продолговатом мозге, чтобы уменьшить тошнотворные побочные эффекты, связанные с таким количеством препаратов, повышающих уровень дофамина.[20]
Продолжение патологических исследований
Площадь пострема также указана в инсулин лечение сахарного диабета 1 и 2 типа. Особый механизм, используемый лекарством прамлинтид, действует в основном на область постремы и приводит к уменьшению глюкагон секреция, которая, в свою очередь, замедляет опорожнение желудка и эффект насыщения. Такое нацеливание на постремную зону позволяет улучшить гликемический контроль без увеличения веса. Поскольку препарат действует на постремную зону, дозы следует титровать медленно, чтобы не вызвать у пациента тошноту.[21]
В настоящее время также проводятся исследования для определения влияния абляции постремной области на гипертония и сердечно-сосудистая функция. Например, исследования на крысах и кроликах показывают, что ангиотензин II- зависимая гипертензия устраняется поражением области постремы.[22][23] Механизм этой физиологической реакции до сих пор полностью не изучен, но способность области postrema регулировать сердечно-сосудистую функцию представляет собой очень интересное направление для нейроэндокринологии.
Рекомендации
- ^ а б c d е Мирза М, М Дас Дж (8 июля 2019 г.). Нейроанатомия, Зона Пострема. StatPearls; Остров сокровищ (Флорида): StatPearls Publishing. PMID 31334969. Получено 4 декабря 2019.CS1 maint: использует параметр авторов (связь)
- ^ а б c d е ж грамм Гросс, П. М; Уолл, К. М; Панг, Дж. Дж; Shaver, S.W; Вайнман, Д. С (1990). «Специализации микрососудов, способствующие быстрой межклеточной дисперсии растворенного вещества в солитарном ядре». Американский журнал физиологии. Регуляторная, интегративная и сравнительная физиология. 259 (6, п. 2): R1131–8. Дои:10.1152 / ajpregu.1990.259.6.R1131. PMID 2260724.
- ^ а б Price, C.J .; Hoyda, T. D .; Фергюсон, А. В. (2007). «Область пострема: монитор мозга и интегратор системного вегетативного состояния». Нейробиолог. 14 (2): 182–194. Дои:10.1177/1073858407311100. PMID 18079557.
- ^ а б c Гросс, П. М. (1991). «Морфология и физиология капиллярных систем в подобластях субфорного органа и области постремы». Канадский журнал физиологии и фармакологии. 69 (7): 1010–25. Дои:10.1139 / y91-152. PMID 1954559.
- ^ а б c d МакКинли, Майкл Дж .; Дентон, Дерек А .; Райан, Филип Дж .; Yao, Song T .; Стефанидис, Анета; Олдфилд, Брайан Дж. (14 марта 2019 г.). «От органов чувств околожелудочковых органов к коре головного мозга: нервные пути, контролирующие жажду и голод». Журнал нейроэндокринологии. 31 (3): e12689. Дои:10.1111 / jne.12689. ISSN 0953-8194. PMID 30672620.
- ^ а б c d е Бритва, Стивен В .; Панг, Джуди Дж .; Wall, Katharine M .; Спозито, Надин М .; Гросс, Пол М. (1 марта 1991 г.). «Субрегиональная топография капилляров в дорсальном блуждающем комплексе крыс: I. Морфометрические свойства». Журнал сравнительной неврологии. 306 (1): 73–82. Дои:10.1002 / cne.903060106. ISSN 0021-9967. PMID 2040730.
- ^ Уильямс, председатель редакционной коллегии, Питер Л., изд. (1995). Анатомия Грея: анатомические основы медицины и хирургии (38-е изд.). Нью-Йорк: Черчилль Ливингстон. ISBN 978-0-443-04560-8.
- ^ а б Гросс, Пол М .; Wall, Katharine M .; Wainman, Dan S .; Шейвер, Стивен В. (1 марта 1991 г.). «Субрегиональная топография капилляров дорсального блуждающего комплекса крыс: II. Физиологические свойства». Журнал сравнительной неврологии. 306 (1): 83–94. Дои:10.1002 / cne.903060107. ISSN 0021-9967. PMID 2040731.
- ^ Miller, A.D .; Лесли, Р. А. (1994). «Область пострема и рвоты». Границы нейроэндокринологии. 15 (4): 301–320. Дои:10.1006 / frne.1994.1012. PMID 7895890.
- ^ Ганонг, В. Ф. (2000). «Циркументрикулярные органы: определение и роль в регуляции эндокринной и вегетативной функции». Клиническая и экспериментальная фармакология и физиология. 27 (5–6): 422–427. Дои:10.1046 / j.1440-1681.2000.03259.x. PMID 10831247.
- ^ Veljković, S .; Йованович-Мичич, Д .; Japundzić, N .; Samardzić, R .; Белеслин, Д. Б. (1989). «Зона постремы и гипертонический эффект ангиотензина». Метаболическое заболевание головного мозга. 4 (1): 61–65. Дои:10.1007 / BF00999495. PMID 2704347.
- ^ Словарь биологической психологии Филипа Винна (2001), Рутледж
- ^ Бернштейн, И. Л .; Чавес, М .; Allen, D .; Тейлор, Э. М. (1992). «Посредничество области postrema физиологических и поведенческих эффектов хлорида лития у крысы». Исследование мозга. 575 (1): 132–137. Дои:10.1016/0006-8993(92)90432-9. PMID 1324085.
- ^ Дэвид Э. Голан и Армен Х. Ташджян "Принципы фармакологии: патофизиологические основы лекарственной терапии"
- ^ Клара, П. М .; Бриззи, К. (1975). «Ультраструктурная морфология беличьей обезьяны area postrema». Исследования клеток и тканей. 160 (3): 315–26. Дои:10.1007 / BF00222042. PMID 807331.
- ^ Джон Кухарчик, Дэвид Дж. Стюарт, Алан Д. Миллер (1991). Тошнота и рвота: последние исследования и клинические достижения. Бока-Ратон: CRC Press. ISBN 0-8493-6781-6. OCLC 24066772.CS1 maint: использует параметр авторов (связь)
- ^ Kodama, N .; Funahashi, M .; Mitoh, Y .; Minagi, S .; Мацуо, Р. (2007). «Пуринергическая модуляция нейрональной возбудимости области postrema в срезах головного мозга крысы». Исследование мозга. 1165: 50–59. Дои:10.1016 / j.brainres.2007.06.003. PMID 17658494.
- ^ Touzani, K .; Склафани, А. (2002). «Поражения постремной области нарушают обучение отвращению вкусовых и токсинных веществ, но не усваивают предпочтения вкусовых и питательных веществ». Поведенческая неврология. 116 (2): 256–266. Дои:10.1037/0735-7044.116.2.256. PMID 11996311.
- ^ Pangestiningsih, T. W .; Хендриксон, А .; Сигит, К .; Sajuthi, D .; Нурхидаят; Боуден, Д. М. (2009). «Развитие области постремы: иммуногистохимическое исследование у макак». Исследование мозга. 1280: 23–32. Дои:10.1016 / j.brainres.2009.05.028. PMID 19460361.
- ^ Yoshikawa, T .; Йошида, Н. (2002). «Влияние лечения 6-гидроксидофамином в области постремы на морфин-индуцированную рвоту у хорьков». Японский журнал фармакологии. 89 (4): 422–425. Дои:10.1254 / jjp.89.422. PMID 12233822.
- ^ Дэй, К. (2005). «Аналог амилина как противодиабетическое средство». Британский журнал диабета и сосудистых заболеваний. 5 (3): 151–154. Дои:10.1177/14746514050050030701.
- ^ Averill, D. B .; Matsumura, K .; Ganten, D .; Феррарио, К. М. (1996). «Роль области постремы в трансгенной гипертензии». Гипертония. 27 (3, часть 2): 591–597. Дои:10.1161 / 01.HYP.27.3.591. PMID 8613209.
- ^ Бишоп, В. С .; Хэй, М. (1993). «Вовлечение Area Postrema в регуляцию симпатического оттока в сердечно-сосудистую систему». Границы нейроэндокринологии. 14 (2): 57–75. Дои:10.1006 / frne.1993.1003. PMID 8486207.