WikiDer > Циклопентилметиловый эфир
 | |
| Имена | |
|---|---|
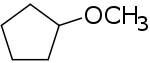
| Название ИЮПАК Метоксициклопентан | |
| Другие имена CPME | |
| Идентификаторы | |
3D модель (JSmol) | |
| ChemSpider | |
| ECHA InfoCard | 100.104.006 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Свойства | |
| C6ЧАС12О | |
| Молярная масса | 100.161 г · моль−1 |
| Внешность | Бесцветная прозрачная жидкость |
| Плотность | 0,8630 г / см3 (20 ° С) [1] |
| Температура плавления | -140 ° С (-220 ° F, 133 К) |
| Точка кипения | 106 ° С (223 ° F, 379 К) [1] |
| 0,011 г / г | |
| Опасности | |
| Паспорт безопасности | MSDS |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасность |
| H225, H302, H312, H315, H319 | |
| P210, P233, P240, P241, P242, P243, P264, P270, P280, P301 + 312, P302 + 352, P303 + 361 + 353, P305 + 351 + 338, P312, P321, P322, P330, P332 + 313, P337 + 313, P362, P363, P370 + 378, P403 + 235, P501 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | -1 ° С (30 ° F, 272 К) |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Циклопентилметиловый эфир (CPME), также известен как метоксициклопентан, является гидрофобный эфирный растворитель. Высокая температура кипения 106 ° C (223 ° F) и предпочтительные характеристики, такие как низкое образование перекиси, относительная стабильность в кислых и основных условиях, образование азеотропов с водой в сочетании с узким диапазоном взрываемости делают CPME альтернативой другим эфирным растворителям, таким как тетрагидрофуран (THF), 2-метилтетрагидрофуран (2-MeTHF), диоксан, и 1,2-диметоксиэтан (DME).[2]
Синтез
Синтез этого соединения можно осуществить двумя способами:
(1) автор метилирование из циклопентанол.
(2) добавлением метанол к циклопентен. Этот второй метод лучше с точки зрения устойчивой химии, поскольку он не дает побочных продуктов.
Приложения
Циклопентилметиловый эфир используется в органическом синтезе, в основном, как растворитель. Однако это также полезно в добыча, полимеризация, кристаллизация и покрытие поверхности.
Вот некоторые примеры реакций, в которых он действует как растворитель:
- Реакции с участием щелочных агентов: нуклеофильные замещения гетероатомов (спиртов и аминов) [3]
- Реакции, опосредованные кислотами Льюиса: реакция Бекмана, реакция Фриделя-Крафтса и др.[4]
- Реакции с использованием металлоорганических реагентов или основных агентов: конденсация Клейзена, образование енолатов или реакция Гриньяра.[5]
- Восстановление и окисление.[6]
- Реакции с катализаторами переходных металлов.[7]
- Реакции с азеотропным удалением воды: ацетализация и др.[8]
использованная литература
- ^ а б Бэрд, Захария Стивен; Ууси-Кыны, Петри; Покки, Юха-Пекка; Педегерт, Эмили; Алопей, Вилле (6 ноя 2019). «Давление паров, плотности и параметры PC-SAFT для 11 биологических соединений». Международный журнал теплофизики. 40 (11): 102. Bibcode:2019IJT .... 40..102B. Дои:10.1007 / s10765-019-2570-9.
- ^ Ватанабэ, Киёси; Ямагива, Нориюки; Торисава, Ясухиро (24 февраля 2007 г.). «Циклопентилметиловый эфир как новый и альтернативный технологический растворитель». Орг. Процесс Res. Dev. 11 (2): 251–258. Дои:10.1021 / op0680136.
- ^ Эфирные соединения и полимеризуемые соединения и способы производства. Автор: Кирики, Сатоши, 3 августа 2015 г., JP 2015140302
- ^ Торисава, Ясухиро (15 января 2007 г.). «Превращение инданоноксимов в изокарбостирилы». Письма по биоорганической и медицинской химии. 17 (2): 453–455. Дои:10.1016 / j.bmcl.2006.10.022. PMID 17064893.
- ^ Окабаяси, Томохито; Иида, Акира; Такай, Кента; Мисаки, Томонори; Танабэ, Ю (18 сентября 2007 г.). «Практический и надежный метод регио- и стереоселективного получения (E) -кетен-трет-бутил-TMS ацеталей и производных β-кетоэфира трет-бутил (1Z, 3E) -1,3-бис (TMS) диенольных эфиров». Журнал органической химии. 72 (21): 8142–8145. Дои:10.1021 / jo701456t. PMID 17877405.
- ^ Шимада, Тоёси; Суда, Масахико; Нагано, Тоёхиро; Какиучи, Киёми (22 октября 2005 г.). «Простое приготовление нового строительного блока на основе BINAP, 5,5'-DiiodoBINAP и его синтетическое применение». Журнал органической химии. 70 (24): 10178–10181. Дои:10.1021 / jo0517186. PMID 16292868.
- ^ Molander, Gary A .; Элиа, Максвелл Д. (3 ноября 2006 г.). "Реакции кросс-связывания Suzuki-Miyaura бензилгалогенидов с арилтрифторборатами калия". Журнал органической химии. 71 (24): 9198–9202. Дои:10.1021 / jo061699f. ЧВК 2515367. PMID 17109547.
- ^ Аззена, Уго; Карраро, Массимо; Мамуйе, Ашенафи Дамтью; Мурджа, Ирэн; Пизано, Луиза; Зедде, Джузеппе (17 апреля 2015 г.). «Циклопентилметиловый эфир - NH4X: новая система растворитель / катализатор для реакций ацетализации с низким воздействием». Зеленая химия. 17 (6): 3281–3284. Дои:10.1039 / c5gc00465a.


