WikiDer > Бис (трифенилфосфин) иминия хлорид
 | |
| Имена | |
|---|---|
| Название ИЮПАК μ-нитридо-бис (трифенилфосфор) хлорид | |
| Другие имена ПНП хлорид PPN хлорид Бис (трифенилфосфин) иминия хлорид Бис (трифенилфосфоранилиден) иминия хлорид Бис (трифенилфосфоранилиден) хлорид аммония Гексафенилдифосфазения хлорид Селектофор | |
| Идентификаторы | |
3D модель (JSmol) | |
| ChemSpider | |
| ECHA InfoCard | 100.040.139 |
| Номер ЕС |
|
PubChem CID | |
| |
| |
| Характеристики | |
| C36ЧАС30ClNP2 | |
| Молярная масса | 574,03 г / моль |
| Внешность | бесцветное твердое вещество |
| Температура плавления | От 260 до 262 ° C (от 500 до 504 ° F; от 533 до 535 K) |
| умеренный | |
| Опасности | |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Предупреждение |
| H315, H319, H332, H335 | |
| P261, P264, P271, P280, P302 + 352, P304 + 312, P304 + 340, P305 + 351 + 338, P312, P321, P332 + 313, P337 + 313, P362, P403 + 233, P405, P501 | |
| Родственные соединения | |
Родственные соединения | Тетрафениларсония хлорид Тетрабутиламмоний хлорид тетрабутиламмоний хлорид |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
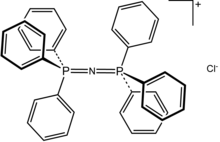
Бис (трифенилфосфин) иминия хлорид это химическое соединение с формулой [(C6ЧАС5)3П)2N] Cl, часто пишется [(Ph3П)2N] Cl и сокращенно [PPN] Cl или [PNP] Cl. Этот бесцветный соль является источником PPN+ катион, который используется как инертный и слабо координирующий катион для выделения реактивных анионов. PPN+ это фосфазен.
Синтез и структура
PPNCl получают в два этапа из трифенилфосфин:[1]
- Ph3P + Cl2 → Ph3PCl2
Этот дихлорид трифенилфосфина относится к пентахлорид фосфора. Лечение этого вида с гидроксиламин в присутствии Ph3P приводит к замене связей P-Cl связями P = N:
- 2 Ph3PCl2 + NH2ОН · HCl + Ph3P → {[Ph3П]2N} Cl + 4HCl + Ph3PO
Оксид трифенилфосфина является побочным продуктом.
Угол PNP в катионе может изменяться от ~ 130 до 180 ° в зависимости от соли. Изогнутые и линейные формы наблюдались в одной и той же элементарной ячейке.[2] Такая же неглубокая потенциальная яма для изгиба наблюдается в изоэлектронных частицах. бис (трифенилфосфоранилиден) метан, (Ph3П)2C, а также более отдаленно родственная молекула недокись углерода. Для хлоридной соли, не содержащей растворителя, валентный угол PNP был определен как 133 °.[3] Длины связи P-N равны 1,597 (2) Å.

Приложения
В лаборатории хлорид PPN является основным предшественником PPN.+ соли. Используя реакции метатезиса солей, нитрит, азид, и другие небольшие неорганические анионы могут быть получены с помощью PPN+ катионы. Полученные соли ППННО2, PPNN3 и др. растворимы в полярных органических растворителях.
PPN+ образует кристаллические соли с рядом анионов, которые иначе трудно кристаллизовать. Его эффективность частично объясняется его жесткостью, отражающей наличие шести фенильных колец. Часто ППН+ образует соли, которые более устойчивы на воздухе, чем соли с меньшими катионами, например, содержащие четвертичный аммоний или катионы щелочных металлов. Этот эффект объясняется стерической защитой, обеспечиваемой этим объемным катионом. Иллюстративный PPN+ соли реакционноспособных анионов включают PPN [HFe (CO)4], PPN [Co (CO)4], (PPN)2[M2(CO)10] (M = Cr, Mo, W) и PPN [Fe (CO)3НЕТ].[1] Роль ионная пара в химических реакциях часто уточняется путем изучения родственной соли, полученной из PPN+.
Связанные катионы
Катион фосфазения, родственный PPN+ равно {[(CH3)2N)3П]2N}+.[4]
Рекомендации
- ^ а б Ruff, J.K .; Шленц, W.J. (1974). «Соли μ-нитридо-бис (трифенилфосфор) (1+ (« PPN ») с карбонильными анионами металлов»). Неорг. Synth. 15: 84–90. Дои:10.1002 / 9780470132463.ch19.
- ^ Харди Г.Е., Зинк Д.И., Каска В.К., Болдуин Дж.С. (декабрь 1978 г.). «Структура и триболюминесценция полиморфов гексафенилкарбодифосфорана». Журнал Американского химического общества. 100 (25): 8001–8002. Дои:10.1021 / ja00493a035.
- ^ Кнапп С., Узун Р. (ноябрь 2010 г.). «Бессольватный бис- (трифенилфосфин) иминий хлорид». Acta Crystallographica Раздел E. 66 (Пт 12): o3185. Дои:10.1107 / S1600536810046325. ЧВК 3011587. PMID 21589480.
- ^ Швезингер, Рейнхард (2001). «1,1,1,3,3,3-Гексакис (диметиламино) -1λ5,3λ5-дифосфазения фторид». Энциклопедия реагентов для органического синтеза e-EROS. С. 1–2. Дои:10.1002 / 047084289X.rh014m.