WikiDer > Микробиота легких
Эта статья нужны дополнительные цитаты для проверка. (Сентябрь 2011 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
В микробиота легких, это легочный микробное сообщество, состоящее из сложного разнообразия микроорганизмы найдено в нижнем дыхательные пути особенно на слизистом слое и эпителиальных поверхностях. Эти микроорганизмы включают: бактерии, грибы, вирусы и бактериофаги. Бактериальная часть микробиоты изучена более внимательно. Он состоит из девяти основных роды: Prevotella, Сфингомонады, Псевдомонады, Acinetobacter, Фузобактерии, Megasphaera, Veillonella, Стафилококк, и Стрептококк.[1][2][3] Это аэробы, а также анаэробы и аэротолерантные бактерии. Микробные сообщества сильно различаются у отдельных людей и составляют около 140 различных семейств. Бронхиальное дерево, например, содержит в среднем 2000 бактериальных геномов на см.2 поверхность. Вредные или потенциально вредные бактерии также обычно обнаруживаются в респираторных образцах. Наиболее значимыми являются Moraxella catarrhalis, Haemophilus influenzae, и Пневмококк. Известно, что они вызывают респираторные расстройства при определенных условиях, а именно, если иммунная система человека ослаблена. Механизм, с помощью которого они сохраняются в нижних дыхательных путях у здоровых людей, неизвестен.
Типы грибов, которые обычно встречаются, составляют легкое. микобиом, в микробиоте легких и включают Candida, Malassezia, Неосартория, Сахаромицеты, и Аспергиллы, среди прочего.[4][5]
Роль эпителиального барьера
Эпителий дыхательных путей вместе с альвеолярными макрофагами и дендритными клетками играет важную роль в начальном распознавании бактериальных продуктов, попадающих в нижние дыхательные пути с воздухом. Поскольку некоторые из этих продуктов являются мощными провоспалительными стимулами, для иммунной системы чрезвычайно важно различать патогенные микроорганизмы и непатогенные комменсалы. Это предотвращает развитие постоянного воспаления и формирует толерантность к безобидной микробиоте.[6]
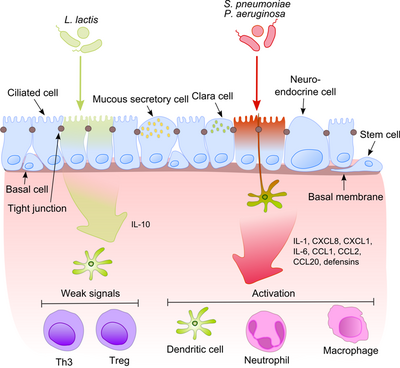
Этот процесс становится гораздо более интригующим, если учесть, что комменсалы часто делятся своими поверхностными молекулами с патогенами. Эпителиальные клетки оснащены очень чувствительными инструментами распознавания - платные рецепторы (TLR), нуклеотид-связывающий домен олигомеризации (NOD) -подобные рецепторы (NLR) и ген, индуцируемый ретиноевой кислотой (RIG) -I-подобные рецепторы (RLR), которые распознают широкий спектр микробных структурных компонентов. После распознавания патогенных бактерий провоспалительные пути активируются, и клеточные компоненты адаптивного и врожденного иммунитета привлекаются к месту инфекции.[7] Одним из ключевых регуляторов этого процесса является NF-κB который перемещается из цитоплазмы в ядро и активирует провоспалительные гены в эпителиальных клетках и макрофагах. Комплекс ДНК-связывающих белков распознает дискретную нуклеотидную последовательность (5’-GGG ACT TTC T-3 ’) в вышестоящей области множества генов ответа. Активация NF-κB рядом стимулов: стенки бактериальных клеток или воспалительные цитокины приводят к его перемещению в ядро.
Напротив, безвредные бактерии не вызывают транслокацию NF-κB в ядро, предотвращая, таким образом, воспаление, хотя они могут экспрессировать то же самое. молекулярные структуры, связанные с микробами (МАМПы). Один возможный механизм, объясняющий этот эффект, был предложен Нейшем, показав, что непатогенные S. typhimurium PhoPc и S. pullorum способны запретить убиквитинирование молекулы ингибитора NF-κB ядерного фактора усилителя гена легкого полипептида NF-κB в ингибиторе B-клеток альфа (IκB-κ).[8] Другое объяснение комменсальной толерантности эпителия относится к посттрансляционной модификации белка путем ковалентного присоединения одного или нескольких мономеров убиквитина (Ub). Ингибирование убиквитинирования приводит к уменьшению воспаления, поскольку только полиубиквитинированный (IκB-κ нацелен на деградацию протеасомой 26 S, что позволяет транслокацию NF-κB в ядро и активацию транскрипции эффекторных генов (например, IL-8). Пробиотические бактерии, такие как Лактобациллы способны модулировать активность Ub-протеасомной системы посредством индукции продукции активных форм кислорода (АФК) в эпителиальных клетках. Было показано, что в клетках млекопитающих АФК служат в качестве важнейших вторичных мессенджеров в множественных путях передачи сигналов в ответ на провоспалительные цитокины. Бактериально индуцированные АФК вызывают окислительную инактивацию каталитического цистеинового остатка Ub 12, что приводит к неполной, но временной потере неддилирования кулина-1 и последующим эффектам на передачу сигналов NF-κB и β-катенина. Другой вид комменсалов, Б. thetaiotaomicron, ослабляет экспрессию провоспалительных цитокинов, способствуя ядерному экспорту NF-κB субъединицы RelA через зависимый от рецептора γ (PPAR-γ) путь, активируемый пролифератором пероксисом. PPAR-γ нацелен на транскрипционно активный Rel A и вызывает ранний ядерный клиренс, ограничивая продолжительность действия NF-κB.
Баланс между патогенами и комменсалами чрезвычайно важен для поддержания гомеостаза в дыхательных путях.
Физиология
Дыхательные пути постоянно подвергаются воздействию множества микроорганизмов, некоторые из которых способны сохраняться и даже колонизировать дыхательные пути. Это возможно благодаря наличию питательных веществ, кислорода и оптимальной температуре роста. Для микробных жителей существует несколько источников питательных веществ хозяина: выделения из эпителиальных клеток дыхательных путей (особенно бокаловидных клеток), выделения из подслизистых желез и транссудат из плазмы. Более того, запас доступных питательных веществ увеличивается за счет деятельности некоторых членов микробиоты. Макромолекулярные компоненты респираторного секрета (белки, гликопротеины, липиды, нуклеиновые кислоты) превращаются в питательные вещества (например, углеводы, аминокислоты). Таким образом, метаболическая активность существующих бактерий позволяет колонизировать новые виды. Комменсальные бактерии непатогены и защищают наши дыхательные пути от патогенов. Есть несколько возможных механизмов. Комменсалы - местные конкуренты патогенных бактерий, потому что они, как правило, занимают одну и ту же экологическую нишу внутри человеческого тела. Во-вторых, они способны производить антибактериальные вещества, называемые бактериоцинами, которые подавляют рост патогенов.
Роды Бациллы, Лактобациллы, Лактококк, Стафилококк, Стрептококк, и Streptomyces являются основными продуцентами бактериоцинов в дыхательных путях. Кроме того, известно, что комменсалы вызывают ответ Th1 и вызывают противовоспалительный интерлейкин (IL) -10, антимикробные пептиды, FOXP3, секреторный иммуноглобулин А (sIgA) производство.
Клиническое значение
Изменения в составе микробного сообщества, по-видимому, играют роль в прогрессировании таких легочных заболеваний, как хроническая обструктивная болезнь легких (ХОБЛ), астма, и кистозный фиброз.[9][10] В людях, S. aureus является частью нормального микробиота присутствует в верхних дыхательных путях,[11] и на коже и слизистой оболочке кишечника.[12] S. aureus, наряду с подобными видами, которые могут колонизировать и действовать симбиотически, но могут вызывать заболевание, если они начинают захватывать ткани, которые они колонизировали, или вторгаются в другие ткани, были названы «патобионтами».[11] Точно так же MRSA может колонизировать людей, не вызывая у них болезней.[13] Наличие таких родов как Микоплазма, Псевдомонады, и Стафилококк коррелирует со стабильным состоянием ХОБЛ. С другой стороны, Prevotella, Мезоризобий, Микробактерии, Микрококк, Veillonela, Ризобий, Стенотрофомонады, и Лактококк присутствуют в основном в когорте здоровых людей. Относительное обилие Протеобактерии увеличивается у детей-астматиков. Синегнойная палочка, Золотистый стафилококк, и Burkholderia cepacia чаще всего встречаются у пациентов с муковисцидозом.
Подходы к высокопроизводительному секвенированию и секвенированию всего генома предоставят дополнительную информацию о сложности и физиологическом значении комменсальных бактерий в нижних дыхательных путях.
Смотрите также
Рекомендации
- ^ Erb-Downward, John R .; Томпсон, Дебора Л .; Хан, Мейлан К .; Freeman, Christine M .; Макклоски, Лиза; Schmidt, Lindsay A .; Янг, Винсент Б.; Тэйвс, Гален Б.; и другие. (2011). Бересвилл, Стефан (ред.). «Анализ микробиома легких у« здорового »курильщика и при ХОБЛ». PLOS One. 6 (2): e16384. Bibcode:2011PLoSO ... 616384E. Дои:10.1371 / journal.pone.0016384. ЧВК 3043049. PMID 21364979.
- ^ Хилти, Маркус; Берк, Конор; Педро, Хелдер; Карденас, Пол; Буш, Энди; Босли, Кара; Дэвис, Джейн; Эрвин, Аарон; и другие. (2010). Нейроллес, Оливье (ред.). «Нарушенные микробные сообщества в дыхательных путях астмы». PLOS One. 5 (1): e8578. Bibcode:2010PLoSO ... 5,8578H. Дои:10.1371 / journal.pone.0008578. ЧВК 2798952. PMID 20052417.
- ^ Бек, Джеймс М .; Янг, Винсент Б.; Хаффнагл, Гэри Б. (1 февраля 2012 г.). «Микробиом легких». Трансляционные исследования. 160 (4): 258–66. Дои:10.1016 / j.trsl.2012.02.005. ЧВК 3440512. PMID 22683412.
- ^ Цуй Л., Моррис А., Гедин Е. (июль 2013 г.). «Микобиом человека в здоровье и болезнях». Геном Мед. 5 (7): 63. Дои:10,1186 / г 467. ЧВК 3978422. PMID 23899327.
Рисунок 2: Распределение родов грибов на разных участках тела
- ^ Ричардсон, М; Bowyer, P; Сабино, Р. (1 апреля 2019 г.). «Человеческое легкое и аспергиллы: вы то, чем вы вдыхаете?». Медицинская микология. 57 (Приложение_2): S145 – S154. Дои:10.1093 / mmy / myy149. ЧВК 6394755. PMID 30816978.
- ^ Кумар, Химаншу; Кавай, Таро; Акира, Шизуо (2011). «Распознавание патогенов врожденной иммунной системой». Международные обзоры иммунологии. 30 (1): 16–34. Дои:10.3109/08830185.2010.529976. PMID 21235323.
- ^ Sha, Q .; Чыонг-Тран, AQ; Плитт, младший; Бек, штат Луизиана; Шлеймер, Р.П. (2004). «Активация эпителиальных клеток дыхательных путей агонистами толл-подобных рецепторов». Американский журнал респираторной клетки и молекулярной биологии. 31 (3): 358–64. CiteSeerX 10.1.1.314.5790. Дои:10.1165 / rcmb.2003-0388OC. PMID 15191912.
- ^ Кумар, Амрита; Ву, Хуэйся; Collier-Hyams, Lauren S; Хансен, Джейсон М; Ли, Тэнго; Ямоа, Косж; Пан, Чжэнь-Цян; Джонс, Дин П.; Нейш, Эндрю S (2007). «Комменсальные бактерии модулируют кулин-зависимую передачу сигналов посредством генерации активных форм кислорода». Журнал EMBO. 26 (21): 4457–66. Дои:10.1038 / sj.emboj.7601867. ЧВК 2063476. PMID 17914462.
- ^ Хуанг, Ивонн Дж .; Ким, Евгения; Кокс, Майкл Дж .; Brodie, Eoin L .; Браун, Рон; Винер-Крониш, Жанин П .; Линч, Сьюзен В. (2010). «Постоянная и разнообразная микробиота дыхательных путей, присутствующая во время обострений хронической обструктивной болезни легких». OMICS: журнал интегративной биологии. 14 (1): 9–59. Дои:10.1089 / omi.2009.0100. ЧВК 3116451. PMID 20141328.
- ^ Кокс, Майкл Дж .; Allgaier, Мартин; Тейлор, Байрон; Baek, Marshall S .; Хуанг, Ивонн Дж .; Дейли, Ребекка А .; Караоз, Улас; Андерсен, Гэри Л .; и другие. (2010). Ратнер, Адам Дж. (Ред.). "Микробиота дыхательных путей и изобилие патогенов у пациентов с муковисцидозом, стратифицированным по возрасту". PLOS One. 5 (6): e11044. Bibcode:2010PLoSO ... 511044C. Дои:10.1371 / journal.pone.0011044. ЧВК 2890402. PMID 20585638.
- ^ а б Шенк, LP; Surette, MG; Bowdish, DM (ноябрь 2016 г.). «Состав и иммунологическое значение микробиоты верхних дыхательных путей». Письма FEBS. 590 (21): 3705–3720. Дои:10.1002/1873-3468.12455. ЧВК 7164007. PMID 27730630.
- ^ Воллина, У (2017). «Микробиом при атопическом дерматите». Клиническая, косметическая и исследовательская дерматология. 10: 51–56. Дои:10.2147 / ccid.s130013. ЧВК 5327846. PMID 28260936.
- ^ Uhlemann, AC; Отто, М; Lowy, FD; ДеЛео, Франция (январь 2014 г.). «Эволюция метициллин-резистентного Staphylococcus aureus, связанного с сообществом и здравоохранением». Инфекция, генетика и эволюция. 21: 563–74. Дои:10.1016 / j.meegid.2013.04.030. ЧВК 3884050. PMID 23648426.
внешняя ссылка
| Викивиды имеет информацию, относящуюся к Микробиота |