WikiDer > RIG-I-подобный рецептор
RIG-I-подобные рецепторы (рецепторы, индуцируемые ретиноевой кислотой, ген I-подобные, RLR) являются разновидностью внутриклеточный рецептор распознавания образов участвует в признании вирусы посредством врожденная иммунная система.[1][2] RIG-I (ген I, индуцируемый ретиноевой кислотой, также известный как DDX58) является наиболее охарактеризованным рецептором в семействе RIG-I-подобных рецепторов (RLR). Вместе с MDA5 (дифференцировка меланомы 5) и LGP2 (лаборатория генетики и физиологии 2), это семейство рецепторов распознавания цитоплазматических паттернов (PRR) является дозорным для внутриклеточной вирусной РНК, которая является продуктом вирусной инфекции. Рецепторы RLR обеспечивают передовую защиту от вирусных инфекций в большинстве тканей.
Лиганды RLR
Рецептор RIG-I предпочитает связывать короткие (<2000 п.н.) одно- или двухцепочечные РНК несущие не закрытый 5’-трифосфат и дополнительные мотивы, такие как мотивы РНК, богатые полиуридином.[3][4] RIG-I вызывает иммунный ответ на вирусы РНК из различных семейств, включая парамиксовирусы (например, корь), рабдовирусы (например, вирус везикулярного стоматита) и ортомиксовирусы (например. грипп А).[5][6][7][8][9] MDA5 лиганды плохо охарактеризованы, но предпочтение отдается длительным двухцепочечная РНК (> 2000 п.н.), например, репликативная форма пикорнавирус РНК, обнаруженная в клетках, инфицированных пикорнавирусом.[10][11] LGP2 связывается с двухцепочечной РНК с тупым концом переменной длины,[12][13] а также с РНК-связанным MDA5 для регулирования нить формирование.[14] Последнее связано с распознаванием LGP2 пикорнавирусов (например, вируса энцефаломиокардита) согласно MDA5.[15]
Конструктивные особенности
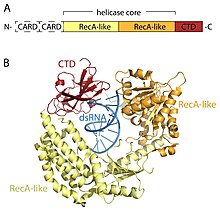
Рецепторы RLR являются членами МЕРТВЫЙ ящик (SF2) геликазы (несмотря на то, что содержат мотив DExD / H, а не мотив DEAD, характерный для этого семейства) и имеют общую архитектуру домена. Все они содержат каталитическое ядро геликазы, состоящее из двух RecA-подобные домены. Ядро каталитической геликазы содержит по крайней мере 9 высококонсервативных мотивов последовательности, которые координируют связывание АТФ и РНК и гидролиз АТФ для раскручивания РНК. С-концевой домен (CTD; ИнтерПро: IPR021673) следует за ядром геликазы, и этот домен также связывает вирусную РНК. Четкие петли связывания РНК внутри CTD трех RLR определяют тип РНК, с которой они могут связываться.[16] Помимо ядра геликазы и CTD, RIG-I и MDA5 имеют две N-концевые карты CARD (caspase активные домены рекрутинга), которые необходимы для инициирования передачи сигналов в нисходящем направлении. LGP2 не похож как на RIG-I, так и на MDA5, поскольку он лишен сигнальных доменов CARD и вместо этого участвует как положительный и отрицательный регулятор RIG-I и MDA5.[14][17][18][19][20][15][21]
Активация сигнализации
В неинфицированных клетках, в которых отсутствует вирусная РНК, RIG-I существует в неактивной конформации, в которой домены CARD замаскированы из-за их взаимодействия с CTD.[22] После связывания РНК, RIG-I переходит в конформацию, в которой домены CARD открыты и «доступны» для передачи сигналов. Напротив, картам MDA5 CARD не мешает отсутствие вирусной РНК.[23] В качестве гарантии для активации RLR открытые карты RIG-I и MDA5 могут подвергаться посттрансляционные модификации (например. убиквитинирование, фосфорилирование), которые либо положительно, либо отрицательно регулируют передачу сигналов ниже по течению.
Передача антивирусных сигналов RIG-I
В активированном состоянии открытые домены RIG-I CARD взаимодействуют с доменами CARD MAVS (митохондриальный противовирусный сигнальный белок, также известный как IPS-1, VISA или Cardif), который находится на внешней поверхности митохондрии. Это событие связывания важно для передачи сигналов, поскольку оно заставляет MAVS формировать большие функциональные агрегаты, в которых TRAF3 (Фактор 3, связанный с рецептором TNF), а затем IKKε/TBK1 (I-каппа-B киназа-эпсилон / TANK-связывающая киназа 1) задействованы. Комплекс IKKε / TBK1 приводит к активации факторы транскрипции регуляторный фактор интерферона 3 (IRF3) и IRF7 которые побуждают тип I (в том числе IFNα и IFNβ) и интерфероны III типа (IFN). IFN типа I связывают рецепторы IFN типа I на поверхности клетки, которая их продуцирует, а также другие типы клеток, которые экспрессируют рецептор, для активации JAK-STAT (Янус-киназа / преобразователи сигналов и активаторы транскрипции) передача сигналов. Это приводит к появлению сотен гены, стимулированные интерфероном (ISG), которые усиливают ответ IFN. В целом это вызывает гибель инфицированных клеток, защиту окружающих клеток и активацию антиген-специфического противовирусного иммунного ответа. В совокупности этот скоординированный противовирусный иммунный ответ контролирует вирусную инфекцию.
Регулирование
Поскольку пролонгированная продукция IFN связана с заболеванием человека, передача сигналов RLR должна строго регулироваться. Одним из различных способов достижения этого является посттрансляционная модификация или мечение сигнальных белков RLR хозяина с помощью фосфата (известного как фосфорилирование) или убиквитин (известный как убиквитинирование). Эти теги также могут быть удалены, что добавляет дополнительный регуляторный уровень к передаче сигналов RLR. Эти посттрансляционные модификациии их удаление преобладают в передаче сигналов RLR и даже регулируют сам рецептор RIG-I. Наиболее известно, что домен RIG-I CARD фосфорилируется протеинкиназа C-α (PKC-α) и PKC-β в состоянии покоя отрицательно регулируют передачу сигналов.[24][25][26] При вирусной инфекции RIG-I дефосфорилированный от PP1α и PP1γ,[27] разрешая убиквитинирование домена RIG-I CARD лигазой E3 TRIM25 для активации антивирусного иммунного ответа, опосредованного RLR.[28] Учитывая, что посттрансляционные модификации настолько важны для активации передачи сигналов RLR, неудивительно, что они прямо или косвенно нацелены на вирусы, такие как грипп А.[29] и корь,[30] соответственно, для подавления сигнализации.
Вирусный захват передачи сигналов RLR
Вирусы разработали способы подорвать передачу сигналов RLR, чтобы увеличить свое выживание. Например, вирус гриппа А и вирус Западного Нила (WNV) используют свои белки NS1 (неструктурный белок 1), чтобы блокировать убиквитинирование RIG-I с помощью TRIM25 или вызывать деградацию RIG-I, соответственно, что, в свою очередь, ингибирует продукцию IFN.[29][31] Этот результат также достигается за счет гепатит С (HCV) белок NS3 / 4A путем расщепления части MAVS,[32] и вирус ящура (FMDV) лидерная протеаза (Lpro), которая расщепляет LGP2.[33] Точно так же вирус денге (DENV) использует свои белки NS2B3, NS2A и NS4B для связывания IKKε и предотвращения фосфорилирования IRF3.[34][35] и его белок NS4A, согласно вирус Зика, чтобы связать MAVS, чтобы заблокировать связывание рецептора RLR.[36][37] Другой яркий пример - это белки парамиксовируса V, которые напрямую связывают различные RLR или сигнальные белки, расположенные ниже по течению, включая MDA5, LGP2 и СТАТ,[38][39][40] или белки, такие как PP1α и PP1γ[30] которые негативно регулируют передачу сигналов RLR.
Смотрите также
использованная литература
![]() Эта статья была адаптирована из следующего источника под CC BY 4.0 лицензия (2019) (отчеты рецензента): «РИГ-Я как рецепторы» (PDF), WikiJournal of Science, 2 (1): 1, 2019, Дои:10.15347 / WJS / 2019.001, ISSN 2470-6345, Викиданные Q62604415
Эта статья была адаптирована из следующего источника под CC BY 4.0 лицензия (2019) (отчеты рецензента): «РИГ-Я как рецепторы» (PDF), WikiJournal of Science, 2 (1): 1, 2019, Дои:10.15347 / WJS / 2019.001, ISSN 2470-6345, Викиданные Q62604415
- ^ Махла Р.С., Редди М.С., Прасад Д.В., Кумар Х. (сентябрь 2013 г.). «Подслащенные PAMP: роль сахарных комплексов PAMP в врожденном иммунитете и биологии вакцины». Границы иммунологии. 4: 248. Дои:10.3389 / fimmu.2013.00248. ЧВК 3759294. PMID 24032031.
- ^ Офферманнс С., Розенталь В. (14 августа 2008 г.). Энциклопедия молекулярной фармакологии, том 1. Springer. ISBN 9783540389163. Получено 30 августа 2011.
Два других семейства PRR, NOD-подобные рецепторы (NLR) и RIG-подобные геликазы (RLH) представляют собой растворимые рецепторы, присутствующие в цитозоле, и действуют как сенсоры для обнаружения различных вирусных и бактериальных продуктов.
- ^ Като Х, Такеучи О, Микамо-Сато Э, Хираи Р., Каваи Т., Мацусита К. и др. (Июль 2008 г.). «Зависимое от длины распознавание двухцепочечных рибонуклеиновых кислот геном-I, индуцируемым ретиноевой кислотой, и геном 5, связанным с дифференцировкой меланомы». Журнал экспериментальной медицины. 205 (7): 1601–10. Дои:10.1084 / jem.20080091. ЧВК 2442638. PMID 18591409.
- ^ Сайто Т., Оуэн Д.М., Цзян Ф., Маркотриджиано Дж., Гейл М. (июль 2008 г.). «Врожденный иммунитет, индуцированный зависимым от состава RIG-I распознаванием РНК вируса гепатита С». Природа. 454 (7203): 523–7. Bibcode:2008Натура.454..523S. Дои:10.1038 / природа07106. ЧВК 2856441. PMID 18548002.
- ^ Баум А., Сачиданандам Р., Гарсия-Састре А. (сентябрь 2010 г.). «Предпочтение RIG-I коротким вирусным молекулам РНК в инфицированных клетках выявлено секвенированием следующего поколения». Труды Национальной академии наук Соединенных Штатов Америки. 107 (37): 16303–8. Bibcode:2010PNAS..10716303B. Дои:10.1073 / pnas.1005077107. ЧВК 2941304. PMID 20805493.
- ^ Гитлин Л., Барчет В., Гилфиллан С., Селла М., Бейтлер Б., Флавелл Р.А. и др. (Май 2006 г.). «Важная роль mda-5 в ответах IFN типа I на полирибоинозиновые: полирибоцитидиловую кислоту и пикорнавирус энцефаломиокардита». Труды Национальной академии наук Соединенных Штатов Америки. 103 (22): 8459–64. Bibcode:2006PNAS..103.8459G. Дои:10.1073 / pnas.0603082103. ЧВК 1464000. PMID 16714379.
- ^ Hornung V, Ellegast J, Kim S, Brzózka K, Jung A, Kato H и др. (Ноябрь 2006 г.). «5'-Трифосфатная РНК является лигандом для RIG-I». Наука. 314 (5801): 994–7. Bibcode:2006Научный ... 314..964H. Дои:10.1126 / наука.1132505. PMID 17038590.
- ^ Ван Х, Рю WS (июль 2010 г.). «Полимераза вируса гепатита B блокирует передачу сигналов рецептора распознавания образов посредством взаимодействия с DDX3: последствия для уклонения от иммунитета». Патогены PLOS. 6 (7): e1000986. Дои:10.1371 / journal.ppat.1000986. ЧВК 2904777. PMID 20657822.
- ^ Schlee M, Roth A, Hornung V, Hagmann CA, Wimmenauer V, Barchet W. и др. (Июль 2009 г.). «Для распознавания 5'-трифосфата с помощью RIG-I-геликазы требуется короткая тупая двухцепочечная РНК, содержащаяся в панхандле вируса с отрицательной цепью». Иммунитет. 31 (1): 25–34. Дои:10.1016 / j.immuni.2009.05.008. ЧВК 2824854. PMID 19576794.
- ^ Feng Q, Hato SV, Langereis MA, Zoll J, Virgen-Slane R, Peisley A, et al. (Ноябрь 2012 г.). «MDA5 обнаруживает репликативную форму двухцепочечной РНК в клетках, инфицированных пикорнавирусом». Отчеты по ячейкам. 2 (5): 1187–96. Дои:10.1016 / j.celrep.2012.10.005. ЧВК 7103987. PMID 23142662.
- ^ Като Х., Такеучи О, Сато С., Йонеяма М., Ямамото М., Мацуи К. и др. (Май 2006 г.). «Различная роль геликаз MDA5 и RIG-I в распознавании РНК-вирусов». Природа. 441 (7089): 101–5. Bibcode:2006Натура.441..101K. Дои:10.1038 / природа04734. PMID 16625202.
- ^ Ли X, Ранджит-Кумар CT, Brooks MT, Dharmaiah S, Herr AB, Kao C, Li P (май 2009 г.). «RIG-I-подобный рецептор LGP2 распознает концы двухцепочечной РНК». Журнал биологической химии. 284 (20): 13881–91. Дои:10.1074 / jbc.m900818200. ЧВК 2679488. PMID 19278996.
- ^ Мурали А., Ли Х, Ранджит-Кумар, CT, Бхардвадж К., Хольценбург А., Ли П., Као С.Ч. (июнь 2008 г.). «Структура и функция LGP2, геликазы DEX (D / H), которая регулирует ответ врожденного иммунитета». Журнал биологической химии. 283 (23): 15825–33. Дои:10.1074 / jbc.m800542200. ЧВК 2414291. PMID 18411269.
- ^ а б Брунс AM, Leser GP, Lamb RA, Horvath CM (сентябрь 2014 г.). «Датчик врожденного иммунитета LGP2 активирует противовирусную передачу сигналов, регулируя взаимодействие MDA5-РНК и сборку филаментов». Молекулярная клетка. 55 (5): 771–81. Дои:10.1016 / j.molcel.2014.07.003. ЧВК 4156907. PMID 25127512.
- ^ а б Сато Т., Като Х., Кумагаи Й., Йонеяма М., Сато С., Мацусита К. и др. (Январь 2010 г.). «LGP2 является позитивным регулятором противовирусных реакций, опосредованных RIG-I и MDA5». Труды Национальной академии наук Соединенных Штатов Америки. 107 (4): 1512–7. Bibcode:2010ПНАС..107.1512С. Дои:10.1073 / pnas.0912986107. ЧВК 2824407. PMID 20080593.
- ^ Такахаси К., Кумета Х., Цудуки Н., Нарита Р., Шигемото Т., Хираи Р. и др. (Июнь 2009 г.). «Структуры раствора цитозольного сенсора РНК С-концевых доменов MDA5 и LGP2: идентификация петли распознавания РНК в RIG-I-подобных рецепторах». Журнал биологической химии. 284 (26): 17465–74. Дои:10.1074 / jbc.m109.007179. ЧВК 2719387. PMID 19380577.
- ^ Чайлдс К.С., Рэндалл Р.Э., Гудборн С. (2013-05-09). «LGP2 играет важную роль в повышении чувствительности mda-5 к активации двухцепочечной РНК». PLOS One. 8 (5): e64202. Bibcode:2013PLoSO ... 864202C. Дои:10.1371 / journal.pone.0064202. ЧВК 3650065. PMID 23671710.
- ^ Комуро А., Хорват С.М. (декабрь 2006 г.). «РНК- и вируснезависимое ингибирование противовирусной передачи сигналов с помощью РНК-геликазы LGP2». Журнал вирусологии. 80 (24): 12332–42. Дои:10.1128 / jvi.01325-06. ЧВК 1676302. PMID 17020950.
- ^ Паризиэн Дж. П., Ленуар Дж. Дж., Мандхана Р., Родригес К. Р., Циан К., Брунс А. М., Хорват С. М. (июнь 2018 г.). «РНК-сенсор LGP2 ингибирует убиквитинлигазу TRAF, чтобы негативно регулировать передачу сигналов врожденного иммунитета». Отчеты EMBO. 19 (6): e45176. Дои:10.15252 / набр.201745176. ЧВК 5989757. PMID 29661858.
- ^ Сайто Т., Хираи Р., Лоо Ю.М., Оуэн Д., Джонсон С.Л., Синха С.К. и др. (Январь 2007 г.). «Регулирование врожденной противовирусной защиты через общий репрессорный домен в RIG-I и LGP2». Труды Национальной академии наук Соединенных Штатов Америки. 104 (2): 582–7. Bibcode:2007ПНАС..104..582С. Дои:10.1073 / pnas.0606699104. ЧВК 1766428. PMID 17190814.
- ^ Учикава Э., Летье М., Малет Х, Брунель Дж., Герлиер Д., Кьюсак С. (май 2016 г.). «Структурный анализ связывания дцРНК с антивирусными рецепторами распознавания образов LGP2 и MDA5». Молекулярная клетка. 62 (4): 586–602. Дои:10.1016 / j.molcel.2016.04.021. ЧВК 4885022. PMID 27203181.
- ^ Луо Д., Дин С. К., Вела А., Кольвей А., Линденбах Б. Д., Пайл А. М. (октябрь 2011 г.). «Структурное понимание распознавания РНК с помощью RIG-I». Ячейка. 147 (2): 409–22. Дои:10.1016 / j.cell.2011.09.023. ЧВК 3222294. PMID 22000018.
- ^ Berke IC, Modis Y (апрель 2012 г.). «MDA5 кооперативно образует димеры и чувствительные к АТФ филаменты при связывании двухцепочечной РНК». Журнал EMBO. 31 (7): 1714–26. Дои:10.1038 / emboj.2012.19. ЧВК 3321199. PMID 22314235.
- ^ Gack MU, Nistal-Villán E, Inn KS, García-Sastre A, Jung JU (апрель 2010 г.). «Опосредованная фосфорилированием негативная регуляция противовирусной активности RIG-I». Журнал вирусологии. 84 (7): 3220–9. Дои:10.1128 / jvi.02241-09. ЧВК 2838087. PMID 20071582.
- ^ Махарадж Н.П., Виз Э., Столл А., Гак М.Ю. (февраль 2012 г.). «Обычные протеинкиназы C-α (PKC-α) и PKC-β отрицательно регулируют передачу противовирусного сигнала RIG-I». Журнал вирусологии. 86 (3): 1358–71. Дои:10.1128 / jvi.06543-11. ЧВК 3264329. PMID 22114345.
- ^ Нисталь-Виллан Э., Гак М.Ю., Мартинес-Дельгадо Г., Махарадж Н.П., Inn KS, Ян Х. и др. (Июнь 2010 г.). «Отрицательная роль фосфорилирования серина 8 RIG-I в регуляции выработки интерферона-бета». Журнал биологической химии. 285 (26): 20252–61. Дои:10.1074 / jbc.m109.089912. ЧВК 2888438. PMID 20406818.
- ^ Виз Э., Ван М.К., Махарадж Н.П., Чен К., Чжоу С., Финберг Р.В., Гак М.Ю. (март 2013 г.). «Дефосфорилирование РНК-сенсоров RIG-I и MDA5 фосфатазой PP1 необходимо для передачи сигналов врожденного иммунитета». Иммунитет. 38 (3): 437–49. Дои:10.1016 / j.immuni.2012.11.018. ЧВК 3616631. PMID 23499489.
- ^ Gack MU, Shin YC, Joo CH, Urano T, Liang C, Sun L и др. (Апрель 2007 г.). «TRIM25 RING-finger E3 убиквитинлигаза важна для антивирусной активности, опосредованной RIG-I». Природа. 446 (7138): 916–920. Bibcode:2007Натура 446..916Г. Дои:10.1038 / природа05732. PMID 17392790.
- ^ а б Гак М.Ю., Альбрехт Р.А., Урано Т., Инн К.С., Хуанг И.С., Карнеро Э. и др. (Май 2009 г.). «Вирус гриппа А NS1 нацелен на убиквитинлигазу TRIM25, чтобы избежать распознавания вирусным РНК-сенсором хозяина RIG-I». Клеточный хозяин и микроб. 5 (5): 439–49. Дои:10.1016 / j.chom.2009.04.006. ЧВК 2737813. PMID 19454348.
- ^ а б Дэвис М.Э., Ван М.К., Ренник Л.Дж., Фулл Ф., Габлеске С., Месман А.В. и др. (Июль 2014 г.). «Антагонизм фосфатазы PP1 белком V вируса кори необходим для ускользания от MDA5 врожденного иммунитета». Клеточный хозяин и микроб. 16 (1): 19–30. Дои:10.1016 / j.chom.2014.06.007. ЧВК 4120867. PMID 25011105.
- ^ Zhang HL, Ye HQ, Liu SQ, Deng CL, Li XD, Shi PY, Zhang B (сентябрь 2017 г.). «Вирус Западного Нила NS1 противодействует выработке интерферона бета за счет нацеливания на RIG-I и MDA5». Журнал вирусологии. 91 (18). Дои:10.1128 / jvi.02396-16. ЧВК 5571242. PMID 28659477.
- ^ Ли XD, Сан Л., Сет РБ, Пинеда Дж., Чен З.Дж. (декабрь 2005 г.). «Протеаза вируса гепатита С NS3 / 4A отщепляет митохондриальный противовирусный сигнальный белок от митохондрий, чтобы избежать врожденного иммунитета». Труды Национальной академии наук Соединенных Штатов Америки. 102 (49): 17717–22. Дои:10.1073 / pnas.0508531102. ЧВК 1308909. PMID 16301520.
- ^ Родригес Пулидо М., Санчес-Апарисио М.Т., Мартинес-Салас Е., Гарсия-Састре А., Собрино Ф, Саис М. (июнь 2018 г.). «Врожденный иммунный сенсор LGP2 расщепляется протеазой Leader вируса ящура». Патогены PLOS. 14 (6): e1007135. Дои:10.1371 / journal.ppat.1007135. ЧВК 6042790. PMID 29958302.
- ^ Англеро-Родригес Ю.И., Пантоха П., Сариол, Калифорния (январь 2014 г.). «Вирус денге подрывает путь индукции интерферона через взаимодействие NS2B / 3 протеаза-IκB киназа эпсилон». Клиническая и вакцинная иммунология. 21 (1): 29–38. Дои:10.1128 / cvi.00500-13. ЧВК 3910921. PMID 24173023.
- ^ Далримпл Н.А., Чимика В., Макков Е.Р. (май 2015 г.). "Белки NS вируса денге ингибируют передачу сигналов RIG-I / MAVS путем блокирования фосфорилирования TBK1 / IRF3: NS4A вируса денге серотипа 1 является уникальным детерминантом вирулентности, регулирующим интерферон". мБио. 6 (3): e00553-15. Дои:10.1128 / mbio.00553-15. ЧВК 4436066. PMID 25968648.
- ^ He Z, Zhu X, Wen W, Yuan J, Hu Y, Chen J и др. (Август 2016 г.). «Вирус денге подрывает врожденный иммунитет хозяина, воздействуя на адаптерный белок MAVS». Журнал вирусологии. 90 (16): 7219–7230. Дои:10.1128 / jvi.00221-16. ЧВК 4984625. PMID 27252539.
- ^ Ма Дж., Кеткар Х., Гэн Т., Ло Э, Ван Л., Си Дж. И др. (2018-06-25). «Неструктурный белок 4A вируса Зика блокирует передачу сигналов RLR-MAVS». Границы микробиологии. 9: 1350. Дои:10.3389 / fmicb.2018.01350. ЧВК 6026624. PMID 29988497.
- ^ Андреева Дж., Чайлдс К.С., Янг Д.Ф., Карлос Т.С., Сток Н., Гудборн С., Рэндалл Р.Э. (декабрь 2004 г.). «Белки V парамиксовирусов связывают IFN-индуцируемую РНК-геликазу, mda-5, и ингибируют ее активацию промотора IFN-бета». Труды Национальной академии наук Соединенных Штатов Америки. 101 (49): 17264–9. Bibcode:2004PNAS..10117264A. Дои:10.1073 / pnas.0407639101. ЧВК 535396. PMID 15563593.
- ^ Чайлдс К., Сток Н., Росс С., Андреева Дж., Хилтон Л., Скиннер М. и др. (Март 2007 г.). «mda-5, но не RIG-I, является общей мишенью для белков парамиксовируса V». Вирусология. 359 (1): 190–200. Дои:10.1016 / j.virol.2006.09.023. PMID 17049367.
- ^ Родригес К.Р., Хорват С.М. (июль 2014 г.). «Взаимодействие белка парамиксовируса V с противовирусным сенсором LGP2 нарушает усиление передачи сигналов MDA5, но не имеет отношения к ингибированию передачи сигналов RLR, опосредованному LGP2». Журнал вирусологии. 88 (14): 8180–8. Дои:10.1128 / jvi.00737-14. ЧВК 4097766. PMID 24829334.
внешние ссылки
- PTHR14074: Геликаза с доменом смерти (фильтр для человека)