WikiDer > Метил бисульфат
 | |
 | |
| Имена | |
|---|---|
| Другие имена Метилсульфат; Метилсерная кислота; Метилгидросульфат; Монометилсульфат; Метилсульфат | |
| Идентификаторы | |
3D модель (JSmol) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.000.834 |
| Номер ЕС |
|
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| CЧАС4О4S | |
| Молярная масса | 112.10 г · моль−1 |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
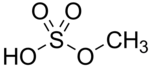
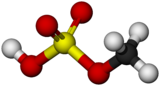
Метил бисульфат химическое соединение с молекулярной формулой CH4О4S. Это соединение является моно-метил сложный эфир из серная кислота. Значение бисульфата метила заключается в том, что он является промежуточным звеном в гидролизе важного реагента. диметилсульфат, (CH3)2ТАК4:[1]
- (CH3)2ТАК4 + H2O → (CH3) HSO4 + CH3ОЙ
Метилбисульфат - сильная кислота:
- (CH3) HSO4 → (CH3)ТАК4− + H+
Метилбисульфат стал известен общественности в 1993 году с открытием, что определенные соединения ртути катализируют преобразование превращения метана в метилбисульфат с хорошими выходами и отличной селективностью в концентрированной серной кислоте.[2] Однако из-за токсичности и опасений по поводу использования ртути только в 1998 году были обнаружены комплексы платины, которые катализируют реакцию CH4 автор: SO3 и O2 что он оказался в центре внимания:[3][4][5]
- CH4 + ТАК3 + 1/2 О2 → (CH3) HSO4
Это открытие указывало на возможный метод повышения качества недорогого и широко доступного метана (натуральный газ) в метанол, который является более полезным химическим веществом и его легче транспортировать, чем метан. Предлагается осуществлять процесс через промежуточное соединение, содержащее Pt-CH3 группа.[6]
Метилбисульфат используется в качестве противоион в формулировка некоторых фармацевтических препаратов, где его обычно называют метилсульфат.[7]
Рекомендации
- ^ Робертсон, Р. Э .; Сугамон, С. (1966). «Гидролиз диметилсульфата и диэтилсульфата в воде». Канадский химический журнал. 44 (14): 1728–1730. Дои:10.1139 / v66-260.
- ^ Periana, R.A .; Таубе, Д.Дж .; Evitt, E.R .; Loffler, D.G .; Wentrcek, P.R .; Voss, G .; Масуда, Т. (1993). «Катализируемая ртутью высокопроизводительная система для окисления метана в метанол». Наука. 259 (5093): 340–343. Дои:10.1126 / SCIENCE.259.5093.340. PMID 17832346.
- ^ Христов, И. Х .; Зиглер, Т. (2003). «Возможная роль SO3 в качестве окислителя при функционализации метана с помощью каталитического процесса. Исследование функциональной теории плотности ". Металлоорганические соединения. 22 (8): 1668–1674. Дои:10.1021 / om020774j.
- ^ Periana, R.A .; Миринов, О .; Таубе, Д. Дж .; Гэмбл, S (2002). «Превращение метана в метилбисульфат с высоким выходом, катализируемое катионами йода». Химические коммуникации (20): 2376–2377. Дои:10.1039 / b205366g.
- ^ Вольф, Д. (1999). «Высокий выход метанола из метана путем активации связи C-H при низких температурах». Angewandte Chemie International Edition. 37 (24): 3351–3353. Дои:10.1002 / (SICI) 1521-3773 (19981231) 37:24 <3351 :: AID-ANIE3351> 3.0.CO; 2-U.
- ^ Periana, R.A .; Таубе, Д. Дж .; Gamble, S .; Taube, H .; Satoh, T .; Фуджи, Х. (1998). «Платиновые катализаторы высокопроизводительного окисления метана до производного метанола». Наука. 280 (5363): 560–564. Дои:10.1126 / science.280.5363.560. PMID 9554841.
- ^ Международные непатентованные наименования (МНН) фармацевтических субстанций. Всемирная организация здоровья.