WikiDer > Перициклическая реакция
В органическая химия, а перициклическая реакция это тип органическая реакция где переходное состояние молекулы имеет циклическую геометрию, реакция протекает в согласованный мода и облигационные орбитали участвующие в реакции перекрываются в непрерывном цикле в переходном состоянии. Перициклические реакции отличаются от линейные реакции, охватывающий большинство органических преобразований и проходящий через ациклическое переходное состояние, с одной стороны, и коаркатные реакции, которые проходят через дважды циклическое согласованное переходное состояние. Перициклические реакции обычно перестановка или же добавление реакции. Основные классы перициклических реакций приведены в таблице ниже (три наиболее важных класса выделены жирным шрифтом). Еные реакции и хелетропные реакции часто классифицируются как реакции группового переноса и циклоприсоединения / реверсии соответственно, в то время как диотропные реакции и реакции группового переноса (если исключены еновые реакции) встречаются редко.
| Имя | Изменения облигаций | |
|---|---|---|
| Сигма | число Пи | |
| Электроциклическая реакция | + 1 | − 1 |
| Циклоприсоединение (и циклореверсия) | + 2 | − 2 |
| Сигматропная реакция | 0 | 0 |
| Реакция группового переноса | 0 | 0 |
| Эне реакция | + 1 | − 1 |
| Хелетропная реакция | + 2 | − 1 |
| Диотропная реакция | 0 | 0 |
В общем, это считается равновесные процессы, хотя можно подтолкнуть реакцию в одном направлении, разработав реакцию, при которой продукт находится на значительно более низком уровне энергии; это связано с мономолекулярной интерпретацией Принцип Ле Шателье. Таким образом, возникает набор «ретро» перициклических реакций.
Механизм перициклической реакции
По определению, перициклические реакции протекают по согласованному механизму с участием одного циклического переходного состояния. Из-за этого до систематического понимания перициклических процессов через принцип сохранения орбитальной симметрии, они были в шутку названы «реакциями без механизма». Однако реакции, для которых можно использовать перициклические механизмы, часто имеют связанные ступенчатые механизмы, протекающие через радикальные или диполярные промежуточные соединения, которые также жизнеспособны. Некоторые классы перициклических реакций, такие как [2 + 2] реакции циклоприсоединения кетена, могут быть «спорными», потому что их механизм иногда не является окончательно согласованным (или может зависеть от реактивной системы). Более того, перициклические реакции также часто имеют аналоги, катализируемые металлами, хотя обычно они также не являются перициклическими технически, поскольку они протекают через промежуточные соединения, стабилизированные металлом, и поэтому не согласованы.
Несмотря на эти предостережения, теоретическое понимание перициклических реакций, вероятно, является одним из самых сложных и хорошо разработанных во всей органической химии. Понимание того, как орбитали взаимодействуют в ходе перициклического процесса, привело к Правила Вудворда – Хоффмана, простой набор критериев, позволяющих предсказать, является ли перициклический механизм реакции вероятным или благоприятным. Например, эти правила предсказывают, что [4 + 2] циклоприсоединение бутадиена и этилена в термических условиях, вероятно, является перициклическим процессом, в то время как [2 + 2] циклоприсоединение двух молекул этилена - нет. Они согласуются с экспериментальными данными, подтверждая упорядоченное согласованное переходное состояние для первого и многоступенчатый радикальный процесс для второго. Несколько эквивалентных подходов, описанных ниже, приводят к одним и тем же прогнозам.
В теория ароматических переходных состояний предполагает, что минимальная энергия переходное состояние для перициклического процесса ароматный, при этом выбор топологии реакции определяется числом участвующих электронов. Для реакций с участием (4п + 2) -электронные системы (2, 6, 10, ... электронов; нечетное число электронных пар), Hückel Предложены переходные состояния топологии, в которых реактивная часть реагирующей молекулы или молекул имеет орбитали, взаимодействующие в непрерывном цикле с четным числом узлов. Через 4п-электронные системы (4, 8, 12, ... электронов; четное число электронных пар) Мебиус предложены переходные состояния топологии, в которых реагирующие молекулы имеют орбитали, взаимодействующие в скрученный непрерывный цикл с нечетным числом узлов. Соответствующие (4п + 2) -электрон Мебиуса и 4п-электронные переходные состояния Хюккеля являются антиароматическими и поэтому сильно нежелательны. Теория ароматических переходных состояний приводит к особенно простой формулировке обобщенных правил Вудворда – Хоффмана: перициклическая реакция с участием нечетного числа электронных пар будет проходить через переходное состояние Хюккеля (четное число антарафациальных компонентов в терминологии Вудворда – Хоффмана),[1] в то время как перициклическая реакция с участием четного числа электронных пар будет проходить через переходное состояние Мёбиуса (нечетное число антарафациальных компонентов).
Эквивалентно перициклические реакции были проанализированы с диаграммы корреляции, которые отслеживают эволюцию молекулярных орбиталей (известных как «коррелирующие» молекулярные орбитали) реагирующих молекул по мере их перехода от реагентов к продуктам через переходное состояние на основе их свойств симметрии. Реакции благоприятны («разрешены»), если основное состояние реагентов коррелируют с основным состоянием продуктов, в то время как они неблагоприятны («запрещены»), если основное состояние реагентов коррелирует с возбужденным состоянием продуктов. Эта идея известна как сохранение орбитальной симметрии. Рассмотрение взаимодействий высших занятых и низших незанятых молекулярных орбиталей (пограничный орбитальный анализ) - еще один подход к анализу переходного состояния перициклической реакции.
Стрелка для перициклических реакций
Условные обозначения перициклических реакций имеют несколько иное значение, чем полярные (и радикальные) реакции. Для перициклических реакций часто нет очевидного движения электронов от источника, богатого электронами, в сток с низким содержанием электронов. Скорее электроны перераспределяются вокруг циклического переходного состояния. Таким образом, электроны могут выталкиваться в любом из двух направлений для перициклической реакции. Однако для некоторых перициклических реакций существует определенная поляризация заряда в переходном состоянии из-за асинхронности (образование и разрыв связи в переходном состоянии не происходят в одинаковой степени). Таким образом, одно направление может быть предпочтительнее другого, хотя, возможно, оба изображения формально верны. В случае реакции Дильса-Альдера, показанной ниже, резонансные аргументы ясно показывают направление поляризации. Однако в более сложных ситуациях могут потребоваться подробные вычисления для определения направления и степени поляризации.
Псевдоперициклические процессы
С перициклическими процессами тесно связаны реакции, которые псевдоперициклический. Хотя псевдоперициклическая реакция проходит через циклическое переходное состояние, две из задействованных орбиталей должны быть ортогональными и не могут взаимодействовать. Возможно, самый известный пример - это гидроборирование олефина. Хотя это, по-видимому, процесс передачи запрещенной группы по топологии Хюккеля с 4 электронами, пустая p-орбиталь и sp2 гибридизованные связи B – H ортогональны и не взаимодействуют. Следовательно, правила Вудворда-Хоффмана не применяются. (Тот факт, что гидроборирование, как полагают, происходит через начальное π-комплексообразование, также может иметь значение.)
В биохимии
Перициклические реакции также происходят в нескольких биологических процессах:
- Перестановка Клейзена из хоризматировать к префенат почти во всех прототрофный организмы
- [1,5]-сигматропный сдвиг в преобразовании прекоррин-8x к гидрогенобириновая кислота
- неферментативный, фотохимический электроциклический кольцо открытия и (1,7) сигматропный гидридный сдвиг в Витамин Д синтез
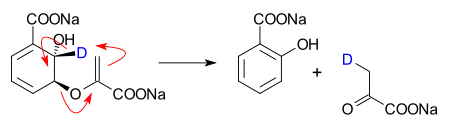
- Изохоризмат пируватлиаза катализированная конверсия изохоризмат в салицилат и пируват[2]
Смотрите также
Рекомендации
- ^ Можно показать, что количество узлов, которые встречаются в перекрывающихся орбиталях перициклического переходного состояния, и количество антарафациальных компонентов должны иметь одинаковую четность (независимо от знаковых соглашений, используемых для выполнения этих назначений).
- ^ Изохоризм пируват-лиаза: перициклический механизм реакции? Майкл С. ДеКлю, Ким К. Болдридж, Доминик Э. Кюнцлер, Питер Каст и Дональд Хилверт Варенье. Chem. Soc.; 2005; 127 (43) стр. 15002–15003; (Коммуникация) Дои:10.1021 / ja055871t