WikiDer > Перестановка Клейзена - Википедия
| Перестановка Клейзена | |
|---|---|
| Названный в честь | Райнер Людвиг Клайзен |
| Тип реакции | Реакция перестановки |
| Идентификаторы | |
| Портал органической химии | клайзен-перестановка |
| RSC ID онтологии | RXNO: 0000148 |
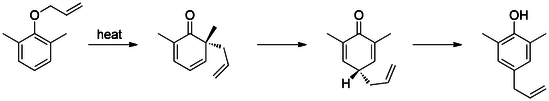
В Перестановка Клейзена это мощный углерод–Углерод связь-образующая химическая реакция, открытая Райнер Людвиг Клайзен. Обогрев аллил винил эфир инициирует [3,3] -сигматропная перегруппировка с образованием γ, δ-ненасыщенного карбонила.
Обнаруженная в 1912 году перегруппировка Клейзена является первым зарегистрированным примером [3,3] -сигматропной перегруппировки.[1][2][3] Написано много отзывов.[4][5][6][7]
Механизм
Перестановка Клейзена - это экзотермическийсогласованные (разрыв связи и рекомбинация) перициклический реакция. Правила Вудворда – Хоффмана демонстрируют супрафациальный стереоспецифический путь реакции. Кинетика первого порядка, и все превращение происходит через высокоупорядоченное циклическое переходное состояние и является внутримолекулярным. Кроссовер эксперименты исключить возможность перегруппировки через межмолекулярный механизм реакции и согласуются с внутримолекулярным процессом.[8][9]
Есть существенные эффекты растворителя наблюдается в перегруппировке Клайзена, где полярные растворители имеют тенденцию в большей степени ускорять реакцию. Растворители, связывающие водород, дали самые высокие константы скорости. Например, этиловый спиртсмеси растворителей с водой дают константы скорости в 10 раз выше, чем сульфолан.[10][11] Трехвалентные алюмоорганические реагенты, такие как триметилалюминий, было показано, что ускоряют эту реакцию.[12][13]
Вариации
Ароматическая перегруппировка Клейзена
Первая известная перегруппировка Клейзена - это [3,3] -сигматропная перегруппировка из аллил фенил эфир до промежуточного 1, что быстро таутомеризуется для орто-замещенный фенол.
Мета-замещение влияет на региоселективность этой перестановки.[14][15] Например, электроноакцепторные группы (такие как бромид) на мета-положение направить перестановку на орто-позиция (71% орто продукт), в то время как электронодонорные группы (такие как метокси), прямая перегруппировка в параграф-позиция (69% параграф товар). Кроме того, наличие орто заместители приводят исключительно к пара-замещенным продуктам перегруппировки (тандемная перегруппировка Клейзена и Коупа).[16]
Если альдегид или же карбоновая кислота занимает орто или же параграф позиции, аллильная боковая цепь перемещает группу, высвобождая ее как монооксид углерода или же углекислый газ, соответственно.[17][18]
Перегруппировка Беллуса-Клейзена
Перегруппировка Беллуса – Клайзена представляет собой реакцию аллиловых эфиров, аминов и тиоэфиров с кетенами с образованием γ, δ-ненасыщенных сложных эфиров, амидов и тиоэфиров.[19][20][21] Эта трансформация была случайно обнаружена Беллусом в 1979 году при синтезе ключевого промежуточного продукта инсектицида, пиретроида. Галогензамещенные кетены (R1, Р2) часто используются в этой реакции из-за их высокой электрофильности. Разработаны многочисленные восстановительные методы для удаления образующихся α-галогенэфиров, амидов и тиоэфиров.[22][23] Bellus-Claisen предлагает химикам-синтетикам уникальную возможность для стратегий расширения кольца.
Перегруппировка Эшенмозера – Клейзена
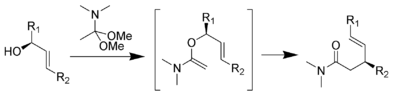
Перегруппировка Эшенмозера – Клейзена протекает при нагревании аллиловых спиртов в присутствии N,N-диметилацетамид диметилацеталь с образованием γ, δ-ненасыщенного амида. Это было разработано Альберт Эшенмозер в 1964 г.[24][25] Перегруппировка Eschenmoser-Claisen была использована в качестве ключевого шага в полном синтезе морфина.[26]
Механизм:[16]
Ирландия - перестановка Клейзена
Перестановка Ирландии – Клейзена - это реакция аллильный карбоксилат с сильным основанием (например, диизопропиламид лития) для получения γ, δ-ненасыщенной карбоновая кислота.[27][28][29] Перегруппировка протекает через силилкетенацеталь, который образуется при захвате енолята лития хлортриметилсиланом. Подобно перегруппировке Беллуса-Клейзена (см. Выше), перегруппировка Ирландия-Клейзена может происходить при комнатной температуре и выше. В E- и Z-конфигурированные силилкетен-ацетали приводят к анти- и син-реаранжированным продуктам соответственно.[30] В литературе есть многочисленные примеры энантиоселективных перегруппировок Ирландии-Клейзена, которые включают хиральные борные реагенты и использование хиральных вспомогательных веществ.[31][32]
Перестановка Джонсона-Клейзена
Перегруппировка Джонсона – Клейзена - это реакция аллильный алкоголь с ортоэфир дать γ, δ-ненасыщенный сложный эфир.[33] Слабые кислоты, такие как пропионовая кислота, использовались для катализатора этой реакции. Эта перестановка часто требует высоких температур (100–200 ° C) и может занять от 10 до 120 часов.[34] Однако нагревание с помощью микроволн в присутствии KSF-глины или пропионовой кислоты продемонстрировало резкое увеличение скорости реакции и выхода.[35][36]
Механизм:[16]
Перестановка фото-Клейзена
Перегруппировка Клайзена ариловых эфиров также может быть проведена как фотохимический реакция. Помимо традиционных орто продукт, полученный в термических условиях (продукт перегруппировки [3,3]), фотохимическое изменение также дает параграф продукт ([3,5] продукт), альтернативные изомеры аллильной группы (например, [1,3] и [1,5] продукты) и простая потеря простой эфирной группы, и даже может дополнительно перегруппировать алкиловые эфиры к аллиловым эфирам. Фотохимическая реакция протекает через ступенчатый процесс радикального расщепления с последующим образованием связи, а не как согласованный процесс. перициклическая реакция, что, таким образом, дает возможность для большего разнообразия возможных субстратов и изомеров продуктов.[37] Результаты [1,3] и [1,5] фото-перегруппировки Клейзена аналогичны результатам фото-фри перестановка сложных ариловых эфиров и родственных ацильных соединений.[38]
Гетеро-Клайзенс
Aza – Claisen
An иминий может служить одним из пи-связанных фрагментов в перегруппировке.[39]
Окисление хрома
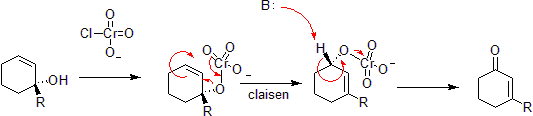
Хром может окислять аллиловые спирты до α, β-ненасыщенных кетонов на противоположной стороне ненасыщенной связи от спирта. Это происходит через согласованную реакцию гетероклейзена, хотя есть механистические различия, поскольку хром У атома есть доступ к d-орбиталям, которые допускают реакцию при менее ограниченном наборе геометрий.[40][41]
Реакция Чена – Маппа
Реакция Чена-Маппа, также известная как [3,3] -фосфоримидатная перегруппировка или реакция Штаудингера-Клейзена, устанавливает фосфит вместо спирта и использует преимущества Редукция Штаудингера чтобы преобразовать это в имин. Последующий Клайзен обусловлен тем фактом, что двойная связь P = O более энергетически выгодна, чем двойная связь P = N.[42]
Перестройка сверхчеловека
В Перестройка сверхчеловека (названный в честь Ларри Оверман) представляет собой перегруппировку Клейзена аллильных трихлорацетимидатов в аллильные трихлорацетамиды.[43][44][45]
Перегруппировка Овермана применима к синтезу диаминосоединений вицинола из 1,2-вицинальных аллиловых диолов.
Цвиттерионная перегруппировка Клейзена
В отличие от типичных перестановок Клейзена, требующих нагрева, цвиттерионный Перегруппировки Клейзена происходят при комнатной температуре или ниже. В ацил ионы аммония очень избирательны для Z-енолирует в мягких условиях.[46][47]
В природе
Фермент хоризматмутаза (EC 5.4.99.5) катализирует перегруппировку Клайзена хоризматировать к префенат, ключевое промежуточное звено в биосинтетический путь к синтезу фенилаланин и тирозин.[48]
Смотрите также
Рекомендации
- ^ Клайзен, Л. (1912). "Uber Umlagerung von Phenol-allyläthern в C-аллил-феноле". Chemische Berichte. 45 (3): 3157–3166. Дои:10.1002 / cber.19120450348.
- ^ Claisen, L .; Титце, Э. (1925). "Über den Mechanismus der Umlagerung der Phenol-allyläther". Chemische Berichte. 58 (2): 275. Дои:10.1002 / cber.19250580207.
- ^ Claisen, L .; Титце, Э. (1926). "Über den Mechanismus der Umlagerung der Phenol-allyläther. (2. Mitteilung)". Chemische Berichte. 59 (9): 2344. Дои:10.1002 / cber.19260590927.
- ^ Hiersemann, M .; Нуббемейер, У. (2007) Перестановка Клейзена. Wiley-VCH. ISBN 3-527-30825-3
- ^ Rhoads, S.J .; Раулинс, Н. Р. (1975). Перестановки Клейзена и Коупа. Орг. Реагировать. 22. С. 1–252. Дои:10.1002 / 0471264180.or022.01. ISBN 978-0471264187.
- ^ Зиглер, Ф. Э. (1988). «Термическая, алифатическая перегруппировка Клейзена». Chem. Ред. 88 (8): 1423–1452. Дои:10.1021 / cr00090a001.
- ^ Випф, П. (1991). «Перестановки Клейзена». Комплексный органический синтез. Компр. Орг. Синтезатор. 5. С. 827–873. Дои:10.1016 / B978-0-08-052349-1.00140-2. ISBN 978-0-08-052349-1.
- ^ Hurd, C.D .; Шмерлинг, Л. (1937). «Наблюдения за перегруппировкой аллил-ариловых эфиров». Варенье. Chem. Soc. 59: 107. Дои:10.1021 / ja01280a024.
- ^ Фрэнсис А. Кэри; Ричард Дж. Сандберг (2007). Продвинутая органическая химия: Часть A: Структура и механизмы. Springer. С. 934–935. ISBN 978-0-387-44897-8.
- ^ Клэйзен, Л. (1912). "Uber Umlagerung von Phenol-allyläthern в C-аллил-феноле". Chemische Berichte. 45 (3): 3157–3166. Дои:10.1002 / cber.19120450348.
- ^ Claisen, L .; Титце, Э. (1925). "Über den Mechanismus der Umlagerung der Phenol-allyläther". Chemische Berichte. 58 (2): 275. Дои:10.1002 / cber.19250580207.
- ^ Геринг, Х.Л .; Якобсон, Р. Р. (1958). "Кинетическое исследование перестройки орто-Клейзена1". Варенье. Chem. Soc. 80 (13): 3277. Дои:10.1021 / ja01546a024.
- ^ White, W. N .; Вольфарт, Э. Ф. (1970). "Перегруппировка о-Клайзена. VIII. Растворитель эффекты". J. Org. Chem. 35 (7): 2196. Дои:10.1021 / jo00832a019.
- ^ Белый, Уильям; и Слейтер, Карл, Уильям Н.; Слейтер, Карл Д. (1961). "The орто-Клейзен перестановка. V. Продукты перегруппировки аллила. м-X-фениловые эфиры ". Журнал органической химии. 26 (10): 3631–3638. Дои:10.1021 / jo01068a004.CS1 maint: несколько имен: список авторов (связь)
- ^ Гоццо, Фабио; Фернандес, Серджио; Родригес, Дениз; Эберлин, Маркос; и Марсайоли, Анита, Фабио Сезар; Фернандес, Серджио Антонио; Родригес, Дениз Кристина; Эберлин, Маркос Ногейра; Марсайоли, Анита Джоселин (2003). «Региоселективность в ароматических перегруппировках Клейзена». Журнал органической химии. 68 (14): 5493–5499. Дои:10.1021 / jo026385g. PMID 12839439.CS1 maint: несколько имен: список авторов (связь)
- ^ а б c Ласло Курти; Барбара Чако (2005). Стратегические применения названных реакций в органическом синтезе: предыстория и подробная механика: 250 названных реакций. Академическая пресса. ISBN 978-0-12-429785-2. Получено 27 марта 2013.
- ^ Адамс, Роджер (1944). Органические реакции, Том II. Нью-Йорк: John Wiley & Sons, Inc., стр. 11–12.
- ^ Claisen, L .; Эйслеб, О. (1913). "Uber die Umlagerung von Phenolallyläthern in die isomeren Allylphenole". Юстус Либигс Аннален дер Хеми. 401 (1): 90. Дои:10.1002 / jlac.19134010103.
- ^ Malherbe, R .; Беллус, Д. (1978). «Новый тип перегруппировки Клейзена с участием 1,3-диполярных интермедиатов. Предварительное сообщение». Helv. Чим. Acta. 61 (8): 3096–3099. Дои:10.1002 / hlca.19780610836.
- ^ Malherbe, R .; Rist, G .; Беллус, Д. (1983). «Реакции галокетенов с аллиловыми эфирами и тиоэфирами: новый тип перегруппировки Клайзена». J. Org. Chem. 48 (6): 860–869. Дои:10.1021 / jo00154a023.
- ^ Гонда, Дж. (2004). «Перестановка Беллуша – Клайзена». Энгью. Chem. Int. Эд. 43 (27): 3516–3524. Дои:10.1002 / anie.200301718. PMID 15293240.
- ^ Эдстром, Э (1991). «Неожиданный поворот в стереохимии трансаннулярных циклизаций. Стереоселективный синтез (±) -эпилупинина». Буквы Тетраэдра. 32 (41): 5709–5712. Дои:10.1016 / S0040-4039 (00) 93536-6.
- ^ Беллус (1983). «Реакции галокетенов с аллиловыми эфирами и тиоэфирами: новый тип перегруппировки Клайзена». Журнал органической химии. 48 (6): 860–869. Дои:10.1021 / jo00154a023.
- ^ Wick, A.E .; Феликс, Д .; Steen, K .; Эшенмозер, А. (1964). "CLAISEN'sche Umlagerungen bei Allyl- und Benzylalkoholen mit Hilfe von Acetalen des N, N-Dimethylacetamids. Vorläufige Mitteilung". Helv. Чим. Acta. 47 (8): 2425–2429. Дои:10.1002 / hlca.19640470835.
- ^ Wick, A.E .; Феликс, Д .; Gschwend-Steen, K .; Эшенмозер, А. (1969). "CLAISEN'sche Umlagerungen bei Allyl- und Benzylalkoholen mit 1-Dimethylamino-1-metxy-äthen". Helv. Чим. Acta. 52 (4): 1030–1042. Дои:10.1002 / hlca.19690520418.
- ^ Гийу, C (2008). «Диастереоселективный тотальный синтез (±) -кодеина». Chem. Евро. J. 14 (22): 6606–6608. Дои:10.1002 / chem.200800744. PMID 18561354.
- ^ Ирландия, R.E .; Мюллер, Р. Х. (1972). «Клейзеновская перегруппировка аллиловых эфиров». Журнал Американского химического общества. 94 (16): 5897. Дои:10.1021 / ja00771a062.
- ^ Ирландия, R.E .; Уиллард, А. К. (1975). «Стереоселективное образование енолятов сложных эфиров». Tetrahedron Lett. 16 (46): 3975–3978. Дои:10.1016 / S0040-4039 (00) 91213-9.
- ^ Ирландия, R.E .; Mueller, R.H .; Уиллард, А. К. (1976). «Перегруппировка енолята Клайзена сложного эфира. Стереохимический контроль посредством стереоселективного образования енолята». Журнал Американского химического общества. 98 (10): 2868. Дои:10.1021 / ja00426a033.
- ^ Ирландия, Р. Э. (1991). «Стереохимический контроль перегруппировки Клайзена сложного эфира енолята». 56 (2): 650–657. Дои:10.1021 / jo00002a030. Цитировать журнал требует
| журнал =(помощь) - ^ Эндерс, E (1996). «Асимметричные [3,3] -сигматропные перегруппировки в органическом синтезе». Тетраэдр: асимметрия. 7 (7): 1847–1882. Дои:10.1016/0957-4166(96)00220-0.
- ^ Кори, E (1991). «Высокоэнантиоселективная и диастереоселективная перегруппировка Ирландии-Клейзена ахиральных аллиловых эфиров». Журнал Американского химического общества. 113 (10): 4026–4028. Дои:10.1021 / ja00010a074.
- ^ Джонсон, Уильям Саммер; Вертеманн, Люциус; Бартлетт, Уильям Р .; Brocksom, Тимоти Дж .; Ли, Цунг-Ти; Фолкнер, Д. Джон; Петерсен, Майкл Р. (1 февраля 1970 г.). «Простая стереоселективная версия перегруппировки Клайзена, приводящая к транс-тризамещенным олефиновым связям. Синтез сквалена». Журнал Американского химического общества. 92 (3): 741–743. Дои:10.1021 / ja00706a074. ISSN 0002-7863.
- ^ Фернандес, Р. А. (2013). "Ортоэфирная перегруппировка Джонсона-Клайзена в синтезе биоактивных молекул, натуральных продуктов и синтетических промежуточных продуктов - последние достижения". Европейский журнал органической химии. 2014 (14): 2833–2871. Дои:10.1002 / ejoc.201301033.
- ^ Хубер, Р. С. (1992). «Ускорение перегруппировки Клайзена ортоэфира с помощью термолиза в микроволновой печи, катализируемого глиной: быстрый путь к бициклическим лактонам». Журнал органической химии. 57 (21): 5778–5780. Дои:10.1021 / jo00047a041.
- ^ Шрикришна, А (1995). «Применение метода микроволнового нагрева для быстрого синтеза γ, δ-ненасыщенных сложных эфиров». Тетраэдр. 51 (6): 1809–1816. Дои:10.1016/0040-4020(94)01058-8.
- ^ Галиндо, Франциско (2005). "Фотохимическая перегруппировка ароматических эфиров: обзор реакции Photo-Claisen". Журнал фотохимии и фотобиологии C: Обзоры фотохимии. 6: 123–138. Дои:10.1016 / j.jphotochemrev.2005.08.001.
- ^ ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "фото-фри перестановка". Дои:10.1351 / goldbook.P04614
- ^ Курт, М. Дж .; Деккер, О. Х. У. (1985). «Энантиоселективный препарат 3-замещенных 4-пентеновых кислот посредством перегруппировки Клайзена». J. Org. Chem. 50 (26): 5769–5775. Дои:10.1021 / jo00350a067.
- ^ Dauben, W. G .; Мично, Д. М. (1977). «Прямое окисление третичных аллиловых спиртов. Простой и эффективный метод алкилирующего карбонильного транспозиции». J. Org. Chem. 42 (4): 682. Дои:10.1021 / jo00424a023.
- ^ «(R) - (+) - 3,4-Диметилциклогекс-2-ен-1-он». Органический синтез. 82: 108. 2005. Дои:10.15227 / orgsyn.082.0108.
- ^ Chen, B .; Мапп, А. (2005). «Термические и каталитические [3,3] -фосфоримидатные перегруппировки». Журнал Американского химического общества. 127 (18): 6712–6718. Дои:10.1021 / ja050759g. PMID 15869293.
- ^ Оверман, Л. Э. (1974). «Катализируемая термическими и ионами ртути [3,3] -сигматропная перегруппировка аллильных трихлорацетимидатов. 1,3-Транспозиция спиртовых и аминных функций». Журнал Американского химического общества. 96 (2): 597–599. Дои:10.1021 / ja00809a054.
- ^ Оверман, Л. Э. (1976). «Общий метод синтеза аминов путем перегруппировки аллильных трихлорацетимидатов. 1,3-Транспозиция спиртовых и аминных функций». Журнал Американского химического общества. 98 (10): 2901–2910. Дои:10.1021 / ja00426a038.
- ^ «Аллильно транспонированные амины из аллильных спиртов: 3,7-диметил-1,6-октадиен-3-амин». Органический синтез. 58: 4. 1978. Дои:10.15227 / orgsyn.058.0004.
- ^ Yu, C.-M .; Choi, H.-S .; Lee, J .; Jung, W.-H .; Ким, Х.-Дж. (1996). «Саморегулируемая молекулярная перегруппировка: диастереоселективный цвиттерионный аза-Клайзен протокол». J. Chem. Soc., Perkin Trans. 1 (2): 115–116. Дои:10.1039 / p19960000115.
- ^ Нуббемейер, У. (1995). «1,2-Асимметричная индукция в цвиттерионной перегруппировке Клейзена аллиламинов». J. Org. Chem. 60 (12): 3773–3780. Дои:10.1021 / jo00117a032.
- ^ Ганем, Б. (1996). «Механизм перестановки Клейзена: снова дежавю». Энгью. Chem. Int. Эд. Англ. 35 (9): 936–945. Дои:10.1002 / anie.199609361.