WikiDer > Фикоцианин
| Белок фикобилисомы | |||||||||
|---|---|---|---|---|---|---|---|---|---|
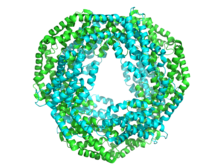
 Аллофикоцианин 12-мерный PDB 1все | |||||||||
| Идентификаторы | |||||||||
| Символ | Фикобилисома | ||||||||
| Pfam | PF00502 | ||||||||
| ИнтерПро | IPR001659 | ||||||||
| SCOP2 | 1cpc / Объем / СУПФАМ | ||||||||
| |||||||||
Фикоцианин это пигмент-белковый комплекс из светособирающих фикобилипротеин семья, вместе с аллофикоцианин и фикоэритрин.[1] Это вспомогательный пигмент к хлорофилл. Все фикобилипротеины растворимы в воде, поэтому они не могут существовать внутри мембраны, как каротиноиды может. Вместо этого фикобилипротеины агрегируют с образованием кластеров, которые прикрепляются к мембране, называемой фикобилисомы. Фикоцианин - это характерный светло-голубой цвет, поглощающий оранжевый и красный свет, особенно около 620 нм (в зависимости от того, какой это конкретный тип), и излучает флуоресценцию около 650 нм (также в зависимости от типа). Аллофикоцианин поглощает и излучает на более длинных волнах, чем фикоцианин C или фикоцианин R. Фикоцианины обнаруживаются в Цианобактерии (также называемый сине-зеленые водоросли). Фикобилипротеины обладают флуоресцентными свойствами, которые используются в иммуноанализ комплекты. Фикоцианин от греческого фико смысл "водоросли" и цианин происходит от английского слова «голубой", что условно означает оттенок сине-зеленого (близкий к" аква ") и происходит от греческого"кианос"что означает несколько другой цвет:" темно-синий ". Продукт фикоцианин, производимый Афанизоменон flos-aquae и Спирулина, например, используется в пищевой промышленности в качестве натурального красителя «Lina Blue» или «EXBERRY Shade Blue» и содержится в сладостях и мороженом. Кроме того, флуоресцентное обнаружение пигментов фикоцианина в образцах воды является полезным методом мониторинга биомассы цианобактерий.[2]
Фикобилипротеины состоят из двух субъединиц (альфа и бета), имеющих белковый каркас, с которым ковалентно связаны 1-2 линейных тетрапиррольных хромофора.
C-фикоцианин часто встречается в цианобактериях, которые процветают вокруг горячих источников, так как он может быть стабильным примерно до 70 ° C, с идентичным спектроскопическим (поглощающим свет) поведением при 20 и 70 ° C. Термофилы содержат немного разные аминокислотные последовательности, что делает их стабильными в этих более высоких условиях. Молекулярная масса составляет около 30 000 Да. Было показано, что стабильность этого белка invitro при этих температурах значительно ниже. Фотоспектральный анализ белка после 1 мин выдержки в условиях 65 ° C в очищенном состоянии показал 50% потерю третичной структуры.
Структура
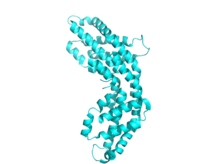
Фикоцианин разделяет общую структурную тему со всеми фикобилипротеины.[3] Структура начинается со сборки мономеров фикобилипротеина, которые представляют собой гетеродимеры, состоящие из субъединиц α и β, и их соответствующих хромофоры связано через тиоэфир связь.
Каждая субъединица обычно состоит из восьми α-спирали. Мономеры спонтанно объединяются с образованием кольцевых тримеров (αβ)3, который имеет вращательная симметрия и центральный канал. Тримеры объединяются в пары с образованием гексамеров (αβ)6, иногда с дополнительными линкерными белками. Каждый стержень фикобилисомы обычно содержит два или более гексамера фикоцианина. Несмотря на общее сходство в структуре и сборке фикобилипротеинов, существует большое разнообразие конформаций гексамеров и палочек, даже если рассматривать только фикоцианины. В более крупном масштабе фикоцианины также различаются по Кристальная структура, хотя биологическая значимость этого спорна.
Например, структура C-фикоцианина из Синехококк вулкан был улучшен до 1.6 Ангстрем разрешающая способность.[4] Мономер (αβ) состоит из 332 аминокислот и 3 тиосвязанных фикоцианобилин (Печатная плата) кофактор молекулы. Обе α- и β-субъединицы имеют PCB в аминокислоте 84, но β-субъединица также имеет дополнительный PCB в положении 155. Этот дополнительный PCB обращен к внешней стороне тримерного кольца и, следовательно, участвует в передаче энергии между стержнями в комплексе фикобилисом. Помимо кофакторов, существует множество предсказуемых нековалентных взаимодействий с окружающим растворителем (водой), которые, как предполагается, вносят вклад в структурную стабильность.
R-фикоцианин II (R-PC II) содержится в некоторых Синехококк разновидность.[5] R-PC II считается первым PEB, содержащим фикоцианин, который происходит от цианобактерий.[5] Его очищенный белок состоит из альфа- и бета-субъединиц в равных количествах.[5] R-PC II содержит ПХБ в бета-84 и фикоэритробиллин (ФЭБ) в альфа-84 и бета-155.[5]
По состоянию на 7 марта 2018 г. насчитывается 44 кристаллических структуры фикоцианина, депонированных в Банк данных белков.[6]
Спектральные характеристики
C-фикоцианин имеет единственный пик поглощения при ~ 621 нм,[7][8] незначительно варьируется в зависимости от организма и условий, таких как температура, pH и концентрация белка in vitro.[9][10] Его максимум выбросов составляет ~ 642 нм.[7][8] Это означает, что пигмент поглощает оранжевый свет и излучает красноватый свет. R-фикоцианин имеет максимумы поглощения при 533 и 544 нм.[5] Максимум флуоресценции R-фикоцианина составляет 646 нм.[5]
| Свойство | C-фикоцианин | R-фикоцианин |
|---|---|---|
| Максимум поглощения (нм) | 621 | 533, 544 |
| Максимальное излучение (нм) | 642 | 646 |
| Коэффициент экстинкции (ε) | 1,54x106 M−1см−1 | - |
| Квантовый выход | 0.81 | - |
Экологическая значимость
Фикоцианин производится многими фотоавтотрофный цианобактерии.[11] Даже если цианобактерии имеют большие концентрации фикоцианина, продуктивность в океане по-прежнему ограничена из-за условий освещения.[11]
Фикоцианин имеет экологическое значение, указывая на цветение цианобактерий. Обычно хлорофилл а используется для обозначения количества цианобактерий, однако, поскольку он присутствует в большом количестве групп фитопланктона, это не идеальный показатель.[12] Например, в исследовании в Балтийском море фикоцианин использовался как маркер для нитчатые цианобактерии во время ядовитого летнего цветения.[12] Некоторые нитчатые организмы в Балтийском море включают: Nodularia spumigena и Aphanizomenon flosaquae.
Важная цианобактерия под названием спирулина (Arthrospira plantensis) - это микроводоросли, производящие C-PC.[13]
Существует множество различных методов производства фикоцианина, включая фотоавтотрофное, миксотрофное, гетеротрофное и рекомбинантное производство.[14] Фотоавтотрофное производство фикоцианина - это то место, где культуры цианобактерий выращивают в открытых прудах в субтропических или тропических регионах.[14] Миксотрофное производство водорослей - это выращивание водорослей на культурах, имеющих источник органического углерода, например глюкоза.[14] Использование миксотрофного производства обеспечивает более высокие темпы роста и более высокую биомассу по сравнению с простым использованием фотоавтотрофных культур.[14] В миксотрофной культуре сумма гетеротрофного и автотрофного роста по отдельности равнялась миксотрофному росту.[15] Гетеротрофное производство фикоцианина не ограничено светом, согласно его определению.[14] Galdieria sulphuraria одноклеточный родофит который содержит большое количество C-PC и небольшое количество аллофикоцианин.[14] G. sulphuraria является примером гетеротрофного производства C-PC, потому что его среда обитания - горячие, кислые источники и для роста используется ряд источников углерода.[14] Рекомбинантное производство C-PC - еще один гетеротрофный метод, включающий генную инженерию.[14]
Лишайниковые грибы и цианобактерии часто имеют симбиотические отношения, и поэтому маркеры фикоцианина могут использоваться для определения экологического распределения цианобактерий, связанных с грибами. Как показано в очень специфической связи между Личина виды и Ривулярия штаммов фикоцианин имеет достаточное филогенетическое разрешение, чтобы разрешить эволюционную историю группы на северо-западе Атлантический океан прибрежная окраина.[16]
Биосинтез
Два гена cpcA и cpcB, расположенные в опероне cpc и транслируемые с одного и того же транскрипта мРНК, кодируют α- и β-цепи C-PC соответственно.[17] Дополнительные элементы, такие как линкерные белки и ферменты, участвующие в синтезе фикобилина и фикобилипротеины, часто кодируются генами в соседних кластерах генов, а оперон cpc Arthrospira platensis также кодирует линкерный белок, участвующий в сборке комплексов C-PC.[18] У красных водорослей гены фикобилипротеина и линкерного белка расположены в пластидном геноме.[19]
Фикоцианобилин синтезируется из гема и вставляется в апо-белок C-PC с помощью трех ферментативных стадий.[20] Циклический гем окисляется до линейного биливердина IXα гемоксигеназой и далее превращается в 3Z-фикоцианобилин, доминирующий изомер фикоцианобилина, с помощью 3Z-фикоцианобилин: ферредоксин оксидоредуктазы. Вставка 3Z-фикоцианобилина в апо-белок C-PC посредством образования тиоэфирной связи катализируется фикоцианобилинлиазой.[21]
Промотор для оперона cpc расположен в вышестоящей области длиной 427 пар оснований от гена cpcB. В A. platensis, 6 предполагаемых промоторных последовательностей были идентифицированы в этом районе, причем четыре из них показывают экспрессию зеленого флуоресцентного белка при трансформации в Кишечная палочка.[22] Также было продемонстрировано присутствие других положительных элементов, таких как светоотражающие элементы в той же области.[23]
Множественные последовательности промотора и ответного элемента в опероне cpc позволяют цианобактериям и красным водорослям регулировать свою экспрессию в ответ на множество условий окружающей среды. Экспрессия генов cpcA и cpcB регулируется светом. Низкая интенсивность света стимулирует синтез CPC и других пигментов, в то время как синтез пигмента подавляется при высокой интенсивности света.[24] Также было показано, что температура влияет на синтез, при этом конкретные концентрации пигментов демонстрируют четкий максимум при 36 ° C у Arthronema africanum, цианобактерии с особенно высоким содержанием C-PC и APC.[25]
Ограничение содержания азота и железа вызывает разложение фикобилипротеинов. Источники органического углерода стимулируют синтез C-PC у Anabaena spp., Но, по-видимому, почти не оказывают отрицательного эффекторного эффекта на A. platensis.[26][27] У родофитов Cyanidium caldarium и Galdieria sulphuraria выработка C-PC подавляется глюкозой, но стимулируется гемом.[28]
Биотехнологии
Экстракты чистого фикоцианина можно выделить из водорослей. Основной порядок сегрегации следующий. Разрыв клеточной стенки механическими силами (замораживание-оттаивание) или химическими агентами (ферменты). Тогда C-PC изолируется с помощью центрифугирование и очищен осаждение сульфатом аммония или же хроматография -либо ион или же гель-фильтрация. После этого образец получает замороженные и сушеные.[14]
.
Приложения
Фикоцианин можно использовать во многих практиках, особенно в медицине и пищевых продуктах. Его также можно использовать в генетике, где он действует как трассирующий из-за его естественной флуоресценции.[29]
Лекарство
Эта секция нужно больше медицинские справки за проверка или слишком сильно полагается на основные источники. (Март 2018 г.) |
Антиоксидантное и противовоспалительное
Фикоцианин обладает как антиоксидантными, так и противовоспалительными свойствами.[30][31][32] Пероксильные, гидроксильные и алкоксильные радикалы являются окислителями, поглощаемыми C-PC. С-ПК, однако, сильнее влияет на пероксильные радикалы. C-PC является антиоксидантом, связывающим металл, поскольку он предотвращает перекисное окисление липидов.[33] Пероксильные радикалы стабилизируются хромофором (субъединица C-PC).[34] Чтобы удалить гидроксильные радикалы, это необходимо делать при слабом освещении и с высокими уровнями C-PC.[35] Гидроксильные радикалы обнаруживаются в воспаленных частях тела.[33] C-PC, являясь антиоксидантом, улавливает эти вызывающие повреждение радикалы, следовательно, является противовоспалительным агентом.
Нейропротекция
Избыток кислорода в головном мозге порождает реактивные формы кислорода (АФК). АФК вызывает повреждение нейронов мозга, что приводит к инсультам. C-фикоцианин поглощает перекись водорода, один из видов АФК, изнутри астроцит, снижая окислительный стресс.[36] Астроциты также увеличивают производство факторов роста, таких как BDNF и NDF, следовательно, усиливают регенерацию нервов. C-PC также предотвращает астроглиоз и глиальное воспаление.[36][37]
Гепатопротекция
C-фикоцианин обладает защитой от гепатотоксичности.[30][38] Vadiraja et al. (1998) обнаружили увеличение сывороточная глутаминовая пировиноградная трансаминаза (SGPT) когда C-PC лечится от гептатоксинов, таких как Тетрахлорметан (CCl4) или R - (+) - пулегон. C-PC защищает печень с помощью Цитохром-P450 система.[38] Он может нарушить выработку ментофурана или нарушить образование α, β-ненасыщенного-γ-кетоальдегида. Оба они являются ключевыми компонентами системы цитохрома P-450, которая продуцирует реактивный метаболит, который производит токсины при связывании с тканями печени. Другой возможный механизм защиты с помощью C-PC может заключаться в удалении реактивных метаболитов (или свободных радикалов, если причиной является CCl4).
Противораковые
C-фикоцианин (C-PC) обладает противораковым действием. Рак возникает, когда клетки продолжают бесконтрольно расти. Было обнаружено, что C-PC предотвращает рост клеток.[39] C-PC останавливает образование опухоли до S-фазы. Синтез ДНК не осуществляется из-за попадания опухолевой клетки в G0, что не приводит к пролиферации опухоли.[40] Кроме того, C-PC вызывает апоптоз. Когда клетки обрабатываются C-PC, образуются ROS (радикальные формы кислорода). Эти молекулы снижают продукцию BCl-2 (регулятора апоптоза). Здесь BCl-2 ингибирует белки, называемые каспазами. Каспазы являются частью пути апоптоза. Когда BCl-2 уменьшается, экспрессия каспаз увеличивается. В результате происходит апоптоз.[41][40] Одного C-PC недостаточно для лечения рака, он должен работать с другими лекарствами, чтобы преодолеть природу устойчивости опухолевых клеток.
Еда
C-фикоцианин (C-PC) может использоваться как натуральный синий пищевой краситель.[42] Этот пищевой краситель можно использовать только для продуктов, приготовленных при низкой температуре, поскольку он не может сохранять синий цвет при высоких температурах, если в него не добавлены консерванты или сахар.[42][43] Тип сахара не имеет значения, C-PC стабилен при высоком содержании сахара. Зная это, C-PC можно использовать для многих видов продуктов, одним из которых являются сиропы. C-PC можно использовать для сиропов от зеленого до синего цвета. Он может иметь разные зеленые оттенки, добавляя желтые пищевые красители.
Рынок
Ожидается, что рынок фикоцианина будет расти в период 2019-2028 годов, поскольку синий пигмент фикоцианина получил одобрение FDA в 2013 году, что открыло множество возможностей для этого рынка, и ожидается, что он достигнет 1 миллиарда долларов США в течение прогнозного периода 2019-2028 годов.[44]
Рекомендации
- ^ Глейзер А.Н. (январь 1989 г.). «Световоды. Направленная передача энергии в фотосинтетической антенне». Журнал биологической химии. 264 (1): 1–4. PMID 2491842.
- ^ Бриент Л., Ленгрон М., Бертран Э, Роллан Д., Сипель А, Штейнманн Д., Боден И., Легеас М., Ле Рузик Б., Борман М. (февраль 2008 г.). «Зонд фикоцианина как инструмент для мониторинга цианобактерий в пресноводных водоемах». Журнал экологического мониторинга. 10 (2): 248–55. Дои:10.1039 / b714238b. PMID 18246219.
- ^ Ван XQ, Ли Л.Н., Чанг В.Р., Чжан Дж. П., Гуй Л.Л., Гуо Б.Дж., Лян округ Колумбия (июнь 2001 г.). "Структура C-фикоцианина из Spirulina platensis при разрешении 2,2 A: новая моноклинная кристаллическая форма фикобилипротеинов в фикобилисомах". Acta Crystallographica Раздел D. 57 (Pt 6): 784–92. Дои:10.1107 / S0907444901004528. PMID 11375497.
- ^ Адир Н., Вайнер Р., Лернер Н. (декабрь 2002 г.). «Уточненная структура c-фикоцианина из цианобактерии Synechococcus vulcanus при 1,6 A: понимание роли молекул растворителя в термостабильности и структуре кофакторов». Biochimica et Biophysica Acta. 1556 (2–3): 168–74. Дои:10.1016 / с0005-2728 (02) 00359-6. PMID 12460674.
- ^ а б c d е ж Онг Л.Дж., Глейзер А.Н. (май 1987 г.). «R-фикоцианин II, новый фикоцианин, встречающийся в морских видах Synechococcus. Идентификация конечного акцептора энергии билина в фикоцианинах». Журнал биологической химии. 262 (13): 6323–7. PMID 3571260.
- ^ "Текстовый поиск: фикоцианин". RCSB PDB. Получено 13 марта 2018.
- ^ а б «C - PC (C - фикоцианин)». АнаСпек.
- ^ а б Писарро С.А., Зауэр К. (май 2001 г.). «Спектроскопическое исследование светособирающего белка C-фикоцианина, связанного с бесцветными линкерными пептидами». Фотохимия и фотобиология. 73 (5): 556–63. Дои:10.1562 / 0031-8655 (2001) 073 <0556: ssotlh> 2.0.co; 2. PMID 11367580.
- ^ Глейзер А.Н., Фанг С., Браун Д.М. (август 1973 г.). «Спектроскопические свойства C-фикоцианина и его альфа- и бета-субъединиц». Журнал биологической химии. 248 (16): 5679–85. PMID 4198883.
- ^ Stanier RY, Kunisawa R, Mandel M, Cohen-Bazire G (июнь 1971 г.). «Очистка и свойства одноклеточных сине-зеленых водорослей (отряд Chroococcales)». Бактериологические обзоры. 35 (2): 171–205. Дои:10.1128 / MMBR.35.2.171-205.1971. ЧВК 378380. PMID 4998365.
- ^ а б Бухвайц М (2016). «Натуральные решения для синих цветов в продуктах питания». В Carle R, Schweiggert RM (ред.). Справочник по натуральным пигментам в продуктах питания и напитках. С. 355–384. Дои:10.1016 / b978-0-08-100371-8.00017-8. ISBN 978-0-08-100371-8.
- ^ а б Возняк М., Брадтке К.М., Дарецкий М., Кренжел А. (март 2016 г.). «Эмпирическая модель для оценки концентрации фикоцианина как индикатора цветения цианобактерий в оптически сложных прибрежных водах Балтийского моря». Дистанционное зондирование. 8 (3): 212. Bibcode:2016RemS .... 8..212Вт. Дои:10.3390 / RS8030212.
- ^ Куддус, М., Сингх, П., Томас, Г., и Аль-Хазими, А. (2013). Последние разработки в области производства и биотехнологического применения C-фикоцианина. BioMed Research International, 2013.
- ^ а б c d е ж грамм час я Куддус М., Сингх П., Томас Г., Аль-Хазими А. (2013). «Последние разработки в области производства и биотехнологического применения C-фикоцианина». BioMed Research International. 2013: 742859. Дои:10.1155/2013/742859. ЧВК 3770014. PMID 24063013.
- ^ Маркес Ф.Дж., Сасаки К., Какизоно Т., Нисио Н., Нагаи С. (1993). «Характеристики роста Spirulina platensis в миксотрофных и гетеротрофных условиях». Журнал ферментации и биоинженерии. 76 (5): 408–410. Дои:10.1016 / 0922-338x (93) 90034-6.
- ^ Ортис-Альварес Р., де Лос Риос А., Фернандес-Мендоса Ф., Торральба-Бурриал А., Перес-Ортега С. (16 июля 2015 г.). «Экологическая специализация двух видов морских цианоличников, специфичных для фотобионтов, из рода Lichina». PLOS ONE. 10 (7): e0132718. Bibcode:2015PLoSO..1032718O. Дои:10.1371 / journal.pone.0132718. ЧВК 4504470. PMID 26181436.
- ^ Лю Дж, Чжан X, Суй З, Чжан X, Мао Y (март 2005 г.). «Клонирование и характеристика оперона c-фикоцианина из цианобактерии Arthrospira platensis FACHB341». Журнал прикладной психологии. 17 (2): 181–185. Дои:10.1007 / s10811-005-6418-2. S2CID 548831.
- ^ Гуань X, Цинь С., Су З., Чжао Ф, Ге Б, Ли Ф, Тан X (июль 2007 г.). «Комбинированный биосинтез флуоресцентного цианобактериального голо-альфа-фикоцианина в Escherichia coli с использованием одного вектора экспрессии». Прикладная биохимия и биотехнология. 142 (1): 52–9. Дои:10.1007 / s12010-007-8000-7. PMID 18025568. S2CID 38038885.
- ^ Охта Н., Мацудзаки М., Мисуми О, Миягишима С.И., Нодзаки Х., Танака К., Син-И Т., Кохара Ю., Куроива Т. (апрель 2003 г.). «Полная последовательность и анализ пластидного генома одноклеточной красной водоросли Cyanidioschyzon merolae». ДНК исследования. 10 (2): 67–77. Дои:10.1093 / dnares / 10.2.67. PMID 12755171.
- ^ Тули А.Дж., Цай Ю.А., Глейзер А.Н. (сентябрь 2001 г.). «Биосинтез флюоресцентной цианобактериальной холо-альфа-субъединицы C-фикоцианина в гетерологичном хозяине». Труды Национальной академии наук Соединенных Штатов Америки. 98 (19): 10560–5. Bibcode:2001ПНАС ... 9810560Т. Дои:10.1073 / pnas.181340998. ЧВК 58505. PMID 11553806.
- ^ Эриксен NT (август 2008 г.). «Производство фикоцианина - пигмента с применением в биологии, биотехнологии, продуктах питания и медицине». Прикладная микробиология и биотехнология. 80 (1): 1–14. Дои:10.1007 / s00253-008-1542-у. PMID 18563408. S2CID 9638809.
- ^ Го Н, Чжан X, Лу И, Сон X (март 2007 г.). «Анализ факторов, влияющих на интенсивность запуска в вышестоящей последовательности гена субъединицы фикоцианина бета от Arthrospira platensis с помощью сайт-направленного мутагенеза». Письма о биотехнологии. 29 (3): 459–64. Дои:10.1007 / s10529-006-9266-5. PMID 17242853. S2CID 23575772.
- ^ Лу И, Чжан Х (15 апреля 2005 г.). «Вышестоящая последовательность гена субъединицы фикоцианина β из Arthrospira platensis регулирует экспрессию гена gfp в ответ на интенсивность света». Электронный журнал биотехнологии. 8 (1). Дои:10.2225 / vol8-issue1-fulltext-9.
- ^ Ленивец Дж. К., Вибе М. Г., Эриксен Н. Т. (январь 2006 г.). «Накопление фикоцианина в гетеротрофных и миксотрофных культурах ацидофильной красной водоросли Galdieria sulphuraria». Ферментные и микробные технологии. 38 (1–2): 168–175. Дои:10.1016 / j.enzmictec.2005.05.010.
- ^ Чанева Г., Фурнаджиева С., Минкова К., Лукавский Ю. (23 марта 2007 г.). «Влияние света и температуры на цианобактерию Arthronema africanum - перспективный штамм, продуцирующий фикобилипротеины». Журнал прикладной психологии. 19 (5): 537–544. Дои:10.1007 / s10811-007-9167-6. S2CID 32093759.
- ^ Венугопал В., Прасанна Р., Суд А., Джайсвал П., Кошик Б.Д. (2006). «Стимуляция накопления пигмента у штаммов Anabaena azollae: влияние интенсивности света и сахаров». Folia Microbiologica. 51 (1): 50–6. Дои:10.1007 / bf02931450. PMID 16821712. S2CID 22719533.
- ^ Нараян М.С., Манодж Г.П., Вачравелу К., Бхагьялакшми Н., Махадевасвами М. (ноябрь 2005 г.). «Использование глицерина в качестве источника углерода для роста, производства пигментов и липидов у Spirulina platensis». Международный журнал пищевых наук и питания. 56 (7): 521–8. Дои:10.1080/09637480500410085. PMID 16503562. S2CID 2352249.
- ^ Трокслер Р.Ф., Эрхардт М.М., Браун-Мейсон А.С., Оффнер Г.Д. (декабрь 1981 г.). «Первичная структура фикоцианина из одноклеточного родофита Cyanidium caldarium. II. Полная аминокислотная последовательность бета-субъединицы». Журнал биологической химии. 256 (23): 12176–84. PMID 7028751.
- ^ «Фикоцианин из водорослей и их применения». Oilgae.
- ^ а б Ромай С., Арместо Дж., Ремирес Д., Гонсалес Р., Ледон Н., Гарсия I. (январь 1998 г.). «Антиоксидантные и противовоспалительные свойства C-фикоцианина из сине-зеленых водорослей». Исследование воспаления. 47 (1): 36–41. Дои:10.1007 / с000110050256. PMID 9495584. S2CID 672069.
- ^ Ромай С., Гонсалес Р., Ледон Н., Ремирес Д., Римбау В. (июнь 2003 г.). «C-фикоцианин: билипротеин с антиоксидантным, противовоспалительным и нейропротекторным действием». Современная наука о белках и пептидах. 4 (3): 207–16. Дои:10.2174/1389203033487216. PMID 12769719.
- ^ Romay CH, Armesto J, Remirez D, Gonzalez R, Ledon N, Garcia I (1998). «Антиоксидантные и противовоспалительные свойства C-фикоцианина из сине-зеленых водорослей». Исследование воспаления. 47 (1): 36–41. Дои:10.1007 / с000110050256. PMID 9495584. S2CID 672069.
- ^ а б Ромай К., Ледон Н., Гонсалес Р. (август 1998 г.). «Дальнейшие исследования противовоспалительной активности фикоцианина на некоторых моделях воспаления на животных». Исследование воспаления. 47 (8): 334–338. Дои:10.1007 / с000110050338. PMID 9754867. S2CID 24249892.
- ^ Пател А., Мишра С. и Гош П. К. (2006). Антиоксидантный потенциал C-фикоцианина, выделенного из цианобактерий видов Lyngbya, Phormidium и Spirulina spp.
- ^ Чжоу З. П., ЛИУ, Чен XL, Ван Дж. Х, Чен М., Чжан Ю. З., Чжоу BC (2005). «Факторы, влияющие на антиоксидантную активность C-фикоцианинов из Spirulina Platensis». Журнал пищевой биохимии. 29 (3): 313–322. Дои:10.1111 / j.1745-4514.2005.00035.x.
- ^ а б Мин, С. К., Пак, Дж. С., Луо, Л., Квон, Ю. С., Ли, Х. К., Шим, Х. Дж., ... и Шин, Х. С. (2015). Оценка влияния C-фикоцианина на опосредованную астроцитами нейрозащиту от окислительного повреждения головного мозга с использованием 2D и 3D модели ткани астроцитов. Научные отчеты, 5, 14418.
- ^ Лю, К., Хуанг, Ю., Чжан, Р., Цай, Т., и Цай, Ю. (2016). Медицинское применение C-фикоцианина, полученного из Spirulina platensis. Доказательная дополнительная и альтернативная медицина, 2016 г.
- ^ а б Вадираджа ББ, Гайквад Н.В., Мадьястха К.М. (1998). «Гепатопротекторный эффект C-фикоцианина: защита от четыреххлористого углерода и гепатотоксичности, опосредованной R - (+) - пулегоном, у крыс». Сообщения о биохимических и биофизических исследованиях. 249 (2): 428–431. Дои:10.1006 / bbrc.1998.9149. PMID 9712713.
- ^ Баша О.М., Хафез Р.А., Эль-Аюти Ю.М., Махрус К.Ф., Бариди М.Х., Салама А.М. (2008). «C-фикоцианин подавляет пролиферацию клеток и может вызывать апоптоз в клетках HepG2 человека» (PDF). Египетский журнал иммунологии. 15 (2): 161–7. PMID 20306699. S2CID 42395208.
- ^ а б Лю, Цянь; Хуанг, Инхун; Чжан, Жунхуа; Цай, Тяньге; Цай, Ю (2016). "Медицинское применение Спирулина platensis Полученный C-фикоцианин ". Доказательная дополнительная и альтернативная медицина. 2016: 1–14. Дои:10.1155/2016/7803846. ЧВК 4879233. PMID 27293463.
- ^ Пардхасаради Б.В., Али А.М., Кумари А.Л., Редданна П., Хар А. (ноябрь 2003 г.). «Опосредованный фикоцианином апоптоз в опухолевых клетках AK-5 включает подавление Bcl-2 и образование ROS». Молекулярная терапия рака. 2 (11): 1165–70. PMID 14617790.
- ^ а б Мартелли Дж., Фолли С., Визай Л., Даглия М., Феррари Д. (январь 2014 г.). «Повышение термической стабильности синего красителя C-фикоцианина из Spirulina platensis для применения в пищевой промышленности». Биохимия процесса. 49 (1): 154–159. Дои:10.1016 / j.procbio.2013.10.008.
- ^ Чайклахан Р., Чирасуван Н., Буннаг Б. (апрель 2012 г.). «Стабильность фикоцианина, экстрагированного из Spirulina sp .: Влияние температуры, pH и консервантов». Биохимия процесса. 47 (4): 659–664. Дои:10.1016 / j.procbio.2012.01.010.
- ^ «Рынок фикоцианина достигнет 1 миллиарда долларов, говорит Fact.MR». 20 января 2020.
дальнейшее чтение
- Барсанти Л. (2008). «Странности и курьезы в мире водорослей». В Evangelista V, Barsanti L, Frassanito AM, Passarelli V, Gualtieri P (ред.). Токсины водорослей: природа, возникновение, влияние и обнаружение. НАТО «Наука ради мира и безопасности». Серия А: Химия и биология. Дордрехт: Спрингер. С. 353–391. Дои:10.1007/978-1-4020-8480-5_17. ISBN 978-1-4020-8479-9.