WikiDer > Синтез индола по Фишеру
| Синтез индола по Фишеру | |
|---|---|
| Названный в честь | Герман Эмиль Фишер |
| Тип реакции | Реакция образования кольца |
| Идентификаторы | |
| Портал органической химии | синтез фишера-индола |
| RSC ID онтологии | RXNO: 0000064 |
В Синтез индола по Фишеру это химическая реакция что производит ароматный гетероцикл индол из (заменено) фенилгидразин и альдегид или же кетон под кислый условия.[1][2] Реакция была открыта в 1883 г. Эмиль Фишер. Сегодня противомигрень наркотики триптан class часто синтезируются этим методом.
Выбор кислотного катализатора очень важен. Кислоты Бренстеда Такие как HCl, ЧАС2ТАК4, полифосфорная кислота и п-толуолсульфоновая кислота были успешно использованы. Кислоты Льюиса Такие как трифторид бора, хлорид цинка, хлорид железа, и хлорид алюминия также являются полезными катализаторами этой реакции.
Опубликовано несколько обзоров.[3][4][5]
Механизм реакции
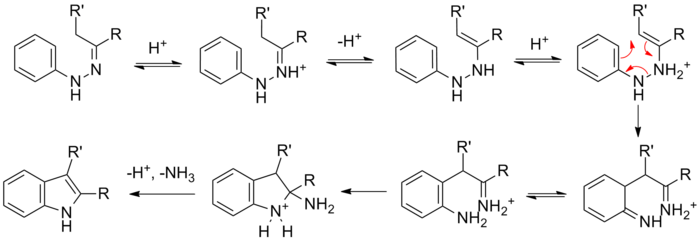
Реакция (замещенного) фенилагидразин с карбонил (альдегид или кетон) первоначально образует фенилгидразон который изомеризуется к соответствующему енамин (или «ен-гидразин»). После протонирование, циклический [3,3] -сигматропная перегруппировка происходит создание я добываю. Образующийся имин образует циклический аминоацеталь (или же аминальный), который под действием кислоты катализ устраняет NH3с получением энергетически выгодного ароматического индола.
Исследования изотопного мечения показывают, что арильный азот (N1) исходного фенилгидразина включается в полученный индол.[6][7]
Модификация Бухвальда
Через палладий-катализируемая реакция, синтез индола Фишера может осуществляться перекрестным связыванием арилбромидов и гидразонов.[8] Этот результат подтверждает ранее предложенную промежуточность гидразоновых промежуточных продуктов в классическом синтезе индола Фишера. Эти N-арилгидразоны подвергаются обмену с другими кетонами, что расширяет возможности этого метода.
Заявление
- Индометацин подготовка.
- Триптан синтез
- Иприндол синтез (фенилгидразин + Suberone → 2,3-Циклогептеноиндол).
Смотрите также
- Синтез индола Бартоли
- Синтез индола Яппа-Клингеманна
- Синтез индола Леймгрубера-Батчо
- Ларок синтез индола
Связанные реакции
Рекомендации
- ^ Fischer, E .; Журдан, Ф. (1883). "Ueber die Hydrazine der Brenztraubensäure". Berichte der Deutschen Chemischen Gesellschaft. 16 (2): 2241–2245. Дои:10.1002 / cber.188301602141.
- ^ Fischer, E .; Гесс, О. (1884). "Synthese von Indolderivaten". Berichte der Deutschen Chemischen Gesellschaft. 17 (1): 559–568. Дои:10.1002 / cber.188401701155.
- ^ Ван Орден, Р. Б .; Линдвалл, Х. Г. (1942). «Индол». Химические обзоры. 30 (1): 69–96. Дои:10.1021 / cr60095a004.
- ^ Робинсон, Б. (1963). "Синтез индола Фишера". Химические обзоры. 63 (4): 373–401. Дои:10.1021 / cr60224a003.
- ^ Робинсон, Б. (1969). «Исследования по синтезу индола Фишера». Химические обзоры. 69 (2): 227–250. Дои:10.1021 / cr60258a004.
- ^ Allen, C.F.H .; Уилсон, К. В. (1943). "Использование N15 как индикаторный элемент в химических реакциях. Механизм синтеза индола Фишера ». Журнал Американского химического общества. 65 (4): 611–612. Дои:10.1021 / ja01244a033.
- ^ Clusius, K .; Вайссер, Х. Р. (1952). "Reaktionen mit 15Н. III. Zum Mechanismus der Fischer'schen Indolsynthese ". Helvetica Chimica Acta. 35 (1): 400–406. Дои:10.1002 / hlca.19520350151.
- ^ Wagaw, S .; Yang, B.H .; Бухвальд, С. Л. (1998). «Катализируемая палладием стратегия для получения индолов: новый подход к синтезу индола Фишера». Журнал Американского химического общества. 120 (26): 6621–6622. Дои:10.1021 / ja981045r.