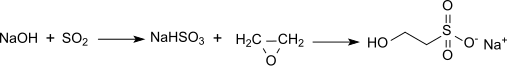WikiDer > Изетионовая кислота
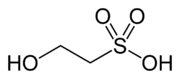 | |
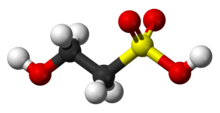 Изетионовая кислота | |
| Имена | |
|---|---|
| Название ИЮПАК 2-гидроксиэтансульфоновая кислота | |
| Идентификаторы | |
3D модель (JSmol) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.003.169 |
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C2ЧАС6О4S | |
| Молярная масса | 126,13 г / моль |
| Плотность | 1,63 г / см3 |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Изетионовая кислота является сероорганическое соединение содержащий алкилсульфоновая кислота находится в бета-версии гидроксильная группа. Его открытие обычно приписывают Генрих Густав Магнус, который приготовил его действием твердого триоксид серы на этиловый спирт в 1833 г.[1]Это белый вода твердое вещество, используемое в производстве определенных поверхностно-активные вещества и в промышленном производстве таурин. Чаще всего он доступен в форме натриевой соли (изетионат натрия).
Синтез
Его первоначальный синтез по реакции триоксид серы на этиловый спирт,[1] был в значительной степени превзойден. Он может быть получен гидролизом карбилсульфат, который получают сульфированием этилен.
Однако наиболее распространенным путем является реакция окись этилена с водным бисульфит натрия, что дает натриевую соль (изетионат натрия):
Реакции
Изетионовая кислота используется в качестве исходного материала при промышленном производстве таурин.
Дегидратация изетионовой кислоты дает винилсульфоновая кислота.[2]
Производные
Жирная кислота сложные эфиры изетионовой кислоты (такой как лауроилизетионат натрия и кокоилизетионат натрия) используются как биоразлагаемый анионный поверхностно-активные вещества.[3] Эти материалы намного мягче для кожи, чем другие поверхностно-активные вещества на основе сульфатов (т.е. лаурилсульфат натрия)[4] что делает их популярными для использования в косметике, шампунях и кусках мыла типа Dove.
Изетионовая кислота также используется в качестве противоион в некоторых фармацевтических составы, в том числе противомикробные препараты гексамидин и пентамидин.[5]
Биологическое значение
Исследования, проведенные на срезах сердца собак, показали, что сердечная ткань может преобразовывать таурин до изетионовой кислоты дальнейшие эксперименты показали, что эта ткань может синтезировать таурин из цистин.[6]
Смотрите также
Рекомендации
- ^ а б Магнус, Г. (1833). "Ueber die Weinschwefelsäure, ihren Einfluss auf die Aetherbildung, und über zwei neue Säuren ähnlicher Zusammensetzung" (PDF). Annalen der Physik und Chemie. 103 (2): 367–388. Дои:10.1002 / andp.18331030213. ISSN 0003-3804.
- ^ Коссвиг, Курт (2000). «Сульфоновые кислоты алифатические». Энциклопедия промышленной химии Ульмана. Wiley-VCH. Дои:10.1002 / 14356007.a25_503. ISBN 3-527-30673-0.
- ^ Петтер, П. Дж. (1984). «Сульфоалкиламиды и сложные эфиры жирных кислот в качестве косметических поверхностно-активных веществ». Международный журнал косметической науки. 6 (5): 249–260. Дои:10.1111 / j.1467-2494.1984.tb00382.x. ISSN 0142-5463.
- ^ Тупкер, Р. А .; Bunte, E.E .; Фидлер, В .; Wlechers, J. W .; Коэнраадс, П. Дж. (1999). «Оценка раздражительности анионных детергентов с использованием одноразовых окклюзионных, многократных окклюзионных и многократных открытых тестов». Контактный дерматит. 40 (6): 316–322. Дои:10.1111 / j.1600-0536.1999.tb06082.x. ISSN 0105-1873.
- ^ Wicho, H, ed. (2009). Австрия-Codex Stoffliste (на немецком языке) (42-е изд.). Вена: Österreichischer Apothekerverlag.
- ^ У. О. Рид и Дж. Д. Велти (1961). «Синтез таурина и изетионовой кислоты кусочками сердца собаки». Журнал биологической химии. 237: 1521–1522.