WikiDer > Гидроксид лантана
Эта статья поднимает множество проблем. Пожалуйста помоги Улучши это или обсудите эти вопросы на страница обсуждения. (Узнайте, как и когда удалить эти сообщения-шаблоны) (Узнайте, как и когда удалить этот шаблон сообщения)
|
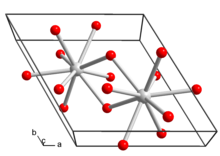 __ Ла3+ __ ОЙ− | |
| Имена | |
|---|---|
| Название ИЮПАК Гидроксид лантана (III) | |
| Идентификаторы | |
| ChemSpider | |
| ECHA InfoCard | 100.034.994 |
| Номер ЕС |
|
PubChem CID |
|
| UNII | |
| |
| Характеристики | |
| Ла (ОН)3 | |
| Молярная масса | 189,93 г / моль |
| Kзр= 2.00·10−21 | |
| Структура | |
| шестиугольник | |
| P63/ м, № 176 | |
а = 6,547 Å, c = 3,854 Å | |
| Опасности | |
| Главный опасности | Раздражающий |
| R-фразы (устарело) | R36 / 37 |
| S-фразы (устарело) | S26, S22, S37 / 39 |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Негорючий |
| Родственные соединения | |
Другой анионы | Хлорид лантана (III) |
Другой катионы | Гидроксид церия (III) Гидроксид скандия (III) Иттрия (III) гидроксид Гидроксид актиния (III) |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Гидроксид лантана является Ла (ОН)
3, а гидроксид из редкоземельный элемент лантан.
Синтез
Гидроксид лантана можно получить, добавляя щелочь Такие как аммиак к водным растворам соли лантана Такие как нитрат лантана. В результате получается гелеобразный осадок которые затем можно сушить на воздухе.[1]
В качестве альтернативы он может быть произведен реакция гидратации (добавление воды) в оксид лантана.[2]
Характеристики
Гидроксид лантана не очень сильно реагирует с щелочными веществами, однако плохо растворяется в кислых растворах.[1] При температурах выше 330 ° C он разлагается на гидроксид лантана, LaOOH, который при дальнейшем нагревании разлагается на оксид лантана.[3]
Гидроксид лантана кристаллизуется в гексагональная кристаллическая система. Каждый ион лантана в кристаллической структуре окружен девятью гидроксид-ионами в трехгранная тригональная призма.[4]
Рекомендации
- ^ а б Е.В. Школьников: Термодинамическая характеристика амфотерии гидроксидов и оксидов элементов подгруппы скандия в водных средах, в: Российский журнал прикладной химии, 2009, 82 (2), S. 2098–2104.
- ^ Цзявэнь Дин, Яньли Ву, Вейли Сун, Юнсю Ли: Получение La (OH)3 и Ла2О3 с морфологией стержня простой гидратацией La2О3, в: Журнал редких земель, 2006 Август, 24 (4), с. 440-442; Дои:10.1016 / S1002-0721 (06) 60139-7.
- ^ Майкл Э. Браун, Патрик Кент Галлахер: Справочник по термическому анализу и калориметрии, S. 482; ISBN 978-0-44453123-0.
- ^ Beall, G.W .; Milligan, W.O .; Уолкотт, Герберт А. (1977). «Структурные тенденции в тригидроксидах лантаноидов». Журнал неорганической и ядерной химии. 39 (1): 65–70. Дои:10.1016 / 0022-1902 (77) 80434-Х.
внешняя ссылка
- «Лантан - Информация об элементе, свойства и использование - Периодическая таблица». rsc.org.
- Внешний паспорт безопасности материалов 1
- Внешний паспорт безопасности материала 2
- MSDS оксида лантана
| Этот неорганический сложный–Связанная статья является заглушка. Вы можете помочь Википедии расширяя это. |



![{ displaystyle mathrm {La (OH) _ {3} { xrightarrow [{- H_ {2} O}] {330 ^ {o} C}} LaOOH}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/950dafbdca1b182a25236f9c2beab44f63f5be62)
![{ displaystyle mathrm {2 LaOOH { xrightarrow [{- H_ {2} O}] { Delta}} La_ {2} O_ {3}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/fcf068415d4e63b6e97eeae2941dfdf7d8b69b9d)