WikiDer > Альдегид Цинкке
Альдегиды Цинкке, или же 5-аминопента-2,4-диенали, являются продуктом реакции соли пиридиния с двумя эквивалентами любого вторичного амина с последующим основным гидролизом. Использование вторичных аминов (в отличие от первичных аминов) позволяет Реакция Цинке принимает другую форму, образуя альдегиды Цинкке, в которых пиридиновое кольцо открыто с концом иминий группа гидролизуется до альдегид. Об использовании динитрофенильной группы для активации пиридина впервые сообщил Теодор Зинке.[1][2][3] Использование цианоген бромид об активации пиридина независимо сообщил W. König:[4]
Были рассмотрены синтез и применение альдегидов Цинкке.[5][6][7]
Вариант Реакция Цинке был применен в синтезе романа индолы:[8]
с цианоген бромид опосредованная активация пиридина (метод Кёнига).[4]
Совсем недавно была проведена интересная перегруппировка альдегидов Цинкке в Z-ненасыщенные амиды были обнаружены случайно при попытке внутримолекулярная реакция Дильса-Альдера.[9] Перестановка дает Z-продукт стереоспецифично. В последующей работе были использованы аллильные амины, которые дали продукты перегруппировки / внутримолекулярный Дильс-Альдер каскад.[10] Также обсуждались детали механизма, однако дальнейшие исследования в сотрудничестве с группа Houk выявил необычный и неожиданный механизм на основе вычислительных исследований. Новый механизм предполагает формирование винила. кетен.[11]
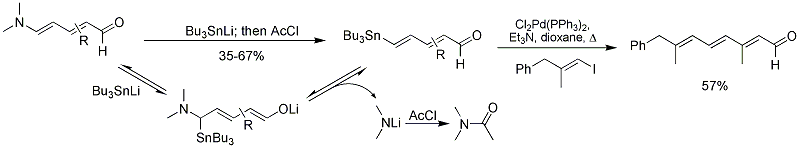
Группа Vanderwal также сообщила о синтезе 4-станнилдиеналей из альдегидов Цинкке путем добавления трибутилстаннил-аниона и гашения ацетилхлоридом.[12] Продукты являются полезными субстратами для Кросс-муфта Стилла реакции с образованием интересных полиеновых структур.
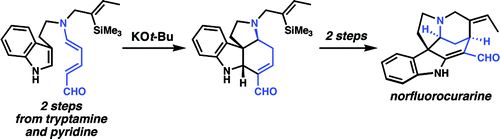
В 2009, группа Вандерваль сообщили о другой интересной перегруппировке альдегидов Цинкке. Альдегиды Цинкке, производные триптамина, нагревают с сильным основанием, чтобы получить перегруппированные Enal как показано ниже. Эта реакция была ключевым этапом в их полном синтезе норфторокурарина, Стрихнос алкалоид.[13] Эта стратегия также была использована в кратком синтезе стрихнин, который стал самым коротким синтезом стрихнина, о котором сообщалось на сегодняшний день, всего с шестью линейными шагами.[14] Эта работа была освещена в блоге Полностью синтетический.
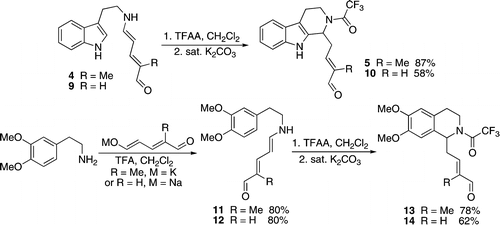
Также в 2009 г. появились первые сообщения о том, что альдегиды Цинкке подверглись испытанию. Реакция Пикте-Шпенглера появился из группы Кристиана Маразано.[15] Эта реакция дала тетрагидро-β-карболин или же тетрагидроизохинолин ядро присутствует во многих алкалоид природных продуктов, и был применен для создания известного промежуточного продукта в предыдущем полном синтезе.
Одним из недостатков синтеза альдегида Цинкке является потребность в 2 эквивалентах амина в начальной реакции раскрытия пиридинового цикла. Это вызывает особую озабоченность в случае сложных вторичных аминов, необходимых для синтеза природных продуктов. Группа Маразано недавно нашла альтернативный синтез путем конденсации на различных глутакональдегид производные с использованием TFA. Это решение значительно упростило производство и очистку сложных альдегидов Цинкке.[16]
Рекомендации
- ^ Zincke, Th.; Heuser, G .; Моллер, В. (1904). "Ueber Dinitrophenylpyridiniumchlorid und dessen Umwandlungsproducte". Юстус Либигс Аннален дер Хеми (на немецком). 333 (2–3): 296–345. Дои:10.1002 / jlac.19043330212.
- ^ Zincke, Th.; Heuser, G .; Моллер, В. (1904). "Ueber Dinitrophenylpyridiniumchlorid und dessen Umwandlungsproducte". Юстус Либигс Аннален дер Хеми (на немецком). 330 (2): 361–374. Дои:10.1002 / jlac.19043300217.
- ^ Zincke, Th.; Вайспфеннинг, Г. (1913). "Uber Dinitrophenylisochinoliniumchlorid und dessen Umwandlungsprodukte". Юстус Либигс Аннален дер Хеми (на немецком). 396 (1): 103–131. Дои:10.1002 / jlac.19133960107.
- ^ а б Кениг, В. (1904). "Über eine neue, vom Pyridin Derivierende Klasse von Farbstoffen". J. Prakt. Chem. (на немецком). 69 (1): 105–137. Дои:10.1002 / prac.19040690107.
- ^ Бехер, Дж. (1980). «Синтез и реакции глутакональдегида и 5-амино-2,4-пентадиеналей». Синтез. 1980 (8): 589–612. Дои:10.1055 / с-1980-29134.
- ^ Becher, J .; Finsen, L .; Винкельманн, И. (1981). «Производные и реакции глутакональдегида - XIII Региоспецифическое раскрытие кольца 3-замещенных пиридинов». Тетраэдр. 37 (13): 2375–2378. Дои:10.1016 / S0040-4020 (01) 88892-X.
- ^ Cheng, W.-C .; Курт, М. Дж. (2002). «Реакция Цинке: обзор». Орг. Prep. Процедуры. Int. 34 (6): 587–608. Дои:10.1080/00304940209355784.
- ^ Кирни, Аарон М .; Вандервол, Кристофер Д. (2006). «Синтез азотных гетероциклов раскрытием цикла пиридиниевых солей». Энгью. Chem. Int. Эд. 45 (46): 7803–7806. Дои:10.1002 / anie.200602996.
- ^ Steinhardt, S.E .; Silverston, J. S .; Вандервол, К. Д. (2008). "Стереоуправляемый синтез Z-Диены через неожиданную перициклическую каскадную перегруппировку 5-амино-2,4-пентадиеналей ». Варенье. Chem. Soc. 130 (24): 7560–7561. Дои:10.1021 / ja8028125. PMID 18505251.
- ^ Steinhardt, S.E .; Вандервал, К. Д. (2009). «Сложные полициклические лактамы из перициклических каскадных реакций альдегидов Цинкке». Варенье. Chem. Soc. 131 (22): 7546–7547. Дои:10.1021 / ja902439f. PMID 19449870.
- ^ Paton, R. S .; Steinhardt, S.E .; Vanderwal, C.D .; Хоук, К. Н. (2011). "Стереоуправляемый синтез Z-Диены через неожиданную перициклическую каскадную перегруппировку 5-амино-2,4-пентадиеналей ». Варенье. Chem. Soc. 133 (11): 3895–3905. Дои:10.1021 / ja107988b. PMID 21351736.
- ^ Michels, T .; Rhee, J. U .; Вандервол, К. Д. (2008). «Синтез δ-трибутилстаннилненасыщенных альдегидов из пиридинов». Орг. Lett. 10 (21): 4787–4790. Дои:10.1021 / ol8020435. PMID 18817407.
- ^ Мартин, Д. Б. С .; Вандервал, К. Д. (2009). «Эффективный доступ к ядру алкалоидов Strychnos, Aspidosperma и Iboga. Краткий синтез норфторокурарина». Варенье. Chem. Soc. 131 (10): 3472–3473. Дои:10.1021 / ja900640v. PMID 19236094.
- ^ Мартин, Д. Б. С .; Вандервол, К. Д. (2011). «Синтез стрихнина с помощью самой длинной линейной последовательности из шести шагов». Chem. Sci. 2 (4): 649. Дои:10.1039 / C1SC00009H.
- ^ Nuhant, P .; Raikar, S. B .; Wypych, J.-C .; Delpech, B .; Маразано, К. (2009). «Повышение электрофильности 5-аминопента-2,4-диеналей путем активации О,N-Бистрифторацетилирование. Приложение к N-Ацил-Пикте-Реакция Шпенглера ". J. Org. Chem. 74 (24): 9413–21. Дои:10.1021 / jo9019545. PMID 19924881.
- ^ Nguyen, T .; Peixoto, S .; Ouairy, C .; Nguyen, T .; Bénéchie, M .; Marazano, C .; Мишель, П. (2010). «Простой и удобный метод синтеза солей 2-замещенного глутакональдегида и производных 2-замещенного глутакональдегида». Синтез. 2010 (1): 103–109. Дои:10.1055 / с-0029-1217105.