WikiDer > Аурон
 | |
| Имена | |
|---|---|
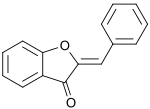
| Предпочтительное название IUPAC 2-Бензилиден-1-бензофуран-3 (2ЧАС)-один | |
| Другие имена 2-Бензилиденбензофуран-3 (2ЧАС)-один 2-бензилиден-1-бензофуран-3-он | |
| Идентификаторы | |
| |
3D модель (JSmol) | |
| ChemSpider | |
PubChem CID | |
| |
| |
| Характеристики | |
| C15ЧАС10О2 | |
| Молярная масса | 222.243 г · моль−1 |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
An аурон это гетероциклический химическое соединение который является типом флавоноид.[1] Есть два изомера молекулы, с (E)- и (Z) -конфигурации. Молекула содержит бензофуран элемент, связанный с бензилиден связаны в позиции 2. В ауроне халкон-подобная группа замкнута в 5-членное кольцо вместо 6-членного кольца, более типичного для флавоноиды.
Производные аурона
Аурон составляет ядро семейства производных, которые вместе известны как ауроны. Ауроны - это растительные флавоноиды, которые обеспечивают желтый цвет к цветам некоторых популярных декоративных растений, таких как львиный зев и космос.[2] Ауроны, включая 4'-хлор-2-гидроксиаурон (C15ЧАС11О3Cl) и 4'-хлороаурон (C15ЧАС9О2Cl) также можно найти в коричневая водоросль Spatoglossum variabile.[3]
Большинство ауронов находятся в (Z) -конфигурация, которая является более стабильной конфигурацией согласно Остин Модель 1 вычисление[3] но есть и в (E) -конфигурации, такие как (E) -3'-O-β-d-глюкопиранозил-4,5,6,4'-тетрагидрокси-7,2'-диметоксиаурон, нашел в Гомфрена агрестис.[4]
Биосинтез
Ауроны биосинтезированный начиная с кумарил-КоА.[5] Ауреузидинсинтаза катализирует образование ауронов из халконов путем гидроксилирования и окислительной циклизации.[2]
Приложения
Некоторые производные аурона обладают противогрибковыми свойствами.[6] и аналогия с флавоноидами предполагает, что ауроны могут иметь другие биологические свойства.[7]
Примеры родственных соединений
- Ауреусидин
- Hispidol (6,4'-дигидроксиаурон)[8]
- Лептозидин
- Сульфуретин (6,3 ', 4'-тригидроксиаурон)
- 4,5,6-тригидроксиаурон
Рекомендации
- ^ Накаяма, Т. (2002). «Энзимология биосинтеза ауронов». Журнал биологии и биоинженерии. 94 (6): 487–91. Дои:10.1016 / S1389-1723 (02) 80184-0. PMID 16233339.
- ^ а б Накаяма, Т; Сато, Т; Фукуи, Й; Ёнекура-Сакакибара, К; Хаяси, H; Танака, Y; Кусуми, Т; Нишино, Т (2001). «Анализ специфичности и механизм синтеза аурона, катализируемого ауреузидинсинтазой, гомологом полифенолоксидазы, ответственным за окраску цветов». Письма FEBS. 499 (1–2): 107–11. Дои:10.1016 / S0014-5793 (01) 02529-7. PMID 11418122.
- ^ а б Атта-Ур-Рахман; Чоудхари, Мичиган; Hayat, S; Хан, AM; Ахмед, А (2001). «Два новых аурона из морской бурой водоросли Spatoglossum variabile». Химико-фармацевтический бюллетень. 49 (1): 105–7. Дои:10.1248 / cpb.49.105. PMID 11201212.
- ^ Ferreira, EO; Сальвадор, MJ; Pral, EM; Альфиери, Южная Каролина; Ито, IY; Диас, Д.А. (2004). «Новый гептазамещенный (Е) -аурон глюкозид и другие ароматические соединения Gomphrena agrestis с биологической активностью» (PDF). Zeitschrift für Naturforschung C. 59 (7–8): 499–505. Дои:10.1515 / znc-2004-7-808. PMID 15813368.
- ^ Фогт, Т. (2010). «Биосинтез фенилпропаноидов». Молекулярный завод. 3: 2–20. Дои:10,1093 / мп / ссп106. PMID 20035037.
- ^ Sutton, Caleb L .; Тейлор, Захари Э .; Фарон, Мэри Б.; Хэнди, Скотт Т. (15.02.2017). «Противогрибковая активность замещенных ауронов». Письма по биоорганической и медицинской химии. 27 (4): 901–903. Дои:10.1016 / j.bmcl.2017.01.012. PMID 28094180.
- ^ Виллемен, Дидье; Мартин, Бенуа; Бар, Натали (1998). «Применение микроволн в органическом синтезе. Сухой синтез 2-арилметилен-3 (2) -нафтофуранонов». Молекулы. 3 (8): 88. Дои:10.3390/30300088.
- ^ Hispidol на метаболомике.jp
