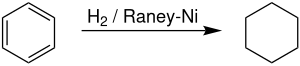WikiDer > Циклогексан
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Циклогексан[2] | |||
| Другие имена Гексанафтен (архаичный)[1] | |||
| Идентификаторы | |||
3D модель (JSmol) | |||
| 3DMet | |||
| 1900225 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.003.461 | ||
| 1662 | |||
| КЕГГ | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1145 | ||
| |||
| |||
| Свойства | |||
| C6ЧАС12 | |||
| Молярная масса | 84.162 г · моль−1 | ||
| Внешность | Бесцветная жидкость | ||
| Запах | Сладкий, бензин-любить | ||
| Плотность | 0,7739 г / мл, жидкость; Плотность = 0,996 г / мл, твердое вещество | ||
| Температура плавления | 6,47 ° С (43,65 ° F, 279,62 К) | ||
| Точка кипения | 80,74 ° С (177,33 ° F, 353,89 К) | ||
| Несмешиваемый | |||
| Растворимость | Растворим в эфир, алкоголь, ацетон | ||
| Давление газа | 78 мм рт. Ст. (20 ° C)[3] | ||
| −68.13·10−6 см3/ моль | |||
| 1.42662 | |||
| Вязкость | 1.02 cP при 17 ° C | ||
| Термохимия | |||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | −156 кДж / моль | ||
Станд. Энтальпия горение (ΔcЧАС⦵298) | −3920 кДж / моль | ||
| Опасности | |||
| Паспорт безопасности | Увидеть: страница данных | ||
| Пиктограммы GHS |     | ||
| Сигнальное слово GHS | Опасность | ||
| H225, H304, H315, H336 | |||
| P210, P233, P240, P241, P242, P243, P261, P264, P271, P273, P280, P301 + 310, P302 + 352, P303 + 361 + 353, P304 + 340, P312, P321, P331, P332 + 313, P362, P370 + 378, P391, P403 + 233, P403 + 235, P405 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | -20 ° С (-4 ° F, 253 К) | ||
| 245 ° С (473 ° F, 518 К) | |||
| Пределы взрываемости | 1.3–8%[3] | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD50 (средняя доза) | 12705 мг / кг (крыса, перорально) 813 мг / кг (мышь, перорально)[4] | ||
LCLo (самый низкий опубликованный) | 17142 частей на миллион (мышь, 2час) 26600 частей на миллион (кролик, 1 час)[4] | ||
| NIOSH (Пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 300 частей на миллион (1050 мг / м3)[3] | ||
REL (Рекомендуемые) | TWA 300 частей на миллион (1050 мг / м3)[3] | ||
IDLH (Непосредственная опасность) | 1300 частей на миллион[3] | ||
| Родственные соединения | |||
Связанный циклоалканы | Циклопентан Циклогептан | ||
Родственные соединения | Циклогексен Бензол | ||
| Страница дополнительных данных | |||
| Показатель преломления (п), Диэлектрическая постоянная (εр), так далее. | |||
Термодинамический данные | Фазовое поведение твердое тело – жидкость – газ | ||
| УФ, ИК, ЯМР, РС | |||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Циклогексан это циклоалкан с молекулярная формула C6ЧАС12. Циклогексан неполярен. Циклогексан - бесцветная легковоспламеняющаяся жидкость с характерным запахом моющего средства, напоминающим чистящие средства (в которых он иногда используется). Циклогексан в основном используется для промышленного производства адипиновая кислота и капролактам, которые являются предшественниками нейлон.[5]
Циклогексил это алкил заместитель циклогексана и сокращенно Сай.[6]
Производство
Современное производство
В промышленных масштабах циклогексан производится гидрирование из бензол в присутствии Никель Ренея катализатор.[7] Производители циклогексана обеспечивают примерно 11,4% мирового спроса на бензол.[8] Реакция сильно экзотермична, с ΔH (500 K) = -216,37 кДж / моль). Дегидрирование начинается заметно выше 300 ° C, что отражает благоприятную энтропию для дегидрирования.[9]
Исторические методы
в отличие бензол, циклогексан не содержится в природных ресурсах, таких как уголь. По этой причине первые исследователи синтезировали свои образцы циклогексана.[10]
Ранние неудачи
- В 1867 г. Марселлен Бертло уменьшенный бензол с участием йодистоводородная кислота при повышенных температурах.[11][12]
- В 1870 г. Адольф фон Байер повторил реакцию[13] и произносится тот же продукт реакции «гексагидробензол»
- в 1890 г. Владимир Марковников считал, что он смог получить то же соединение с Кавказа нефть, назвав его смесь «гексанафтен».
Удивительно, но их циклогексаны кипятят на 10 ° C выше, чем гексагидробензол или гексанафтен, но эта загадка была решена в 1895 году Марковниковым. Н. М. Кишнер, и Николай Зелинский когда они переназначили «гексагидробензол» и «гексанафтен» как метилциклопентан, результат неожиданного реакция перегруппировки.
Успех
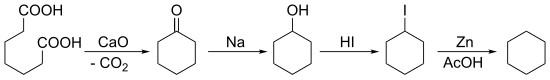
В 1894 году Байер синтезировал циклогексан, начиная с кетонизации пимелиновая кислота с последующим многократным сокращением:
В том же году Э. Хаворт и У. Перкин-младший (1860–1929) подготовил его через Реакция Вюрца 1,6-дибромгексана.
Реакции и использование
Хотя циклогексан довольно инертен, он подвергается каталитическому окислению с образованием циклогексанон и циклогексанол. Смесь циклогексанон-циклогексанол, называемая "КА масло", это сырье для адипиновая кислота и капролактам, предшественники нейлон. Ежегодно производится несколько миллионов килограммов циклогексанона и циклогексанола.[9]
Лабораторный растворитель и другие нишевые применения
Он используется в качестве растворителя в некоторых марках корректирующих жидкостей. Циклогексан иногда используется как неполярный органический растворитель, хотя н-гексан более широко используется для этой цели. Часто используется как перекристаллизация растворитель, так как многие органические соединения обладают хорошей растворимостью в горячем циклогексане и плохой растворимостью при низких температурах.
Циклогексан также используется для калибровки дифференциальная сканирующая калориметрия (DSC) из-за удобного перехода кристалл-кристалл при -87,1 ° C.[14]
Пары циклогексана используются в вакуумных печах науглероживания, при производстве оборудования для термообработки.
Конформация
Кольцо с 6-ю вершинами не соответствует форме идеального шестиугольник. Конформация плоского двумерного плоского шестиугольника имеет значительную угловую деформацию, поскольку его связи не равны 109,5 градусам; то крутильный напряжение также будет значительным, потому что все связи будут затменные узы. Следовательно, чтобы уменьшить скручивающая деформация, циклогексан имеет трехмерную структуру, известную как конформация стула, которые быстро преобразуются при комнатной температуре с помощью процесса, известного как стул флип. Во время переворота кресла встречаются еще три промежуточные конформации: полукресло, которое является наиболее нестабильной конформацией, более стабильная конформация лодочки, и твист-лодочка, которая более устойчива, чем лодка, но все же намного меньше. стабильнее, чем стул. Кресло и твист-лодка - это минимум энергии и, следовательно, конформеры, в то время как полукресло и лодка являются переходными состояниями и представляют собой максимумы энергии. Идея о том, что конформация кресла является наиболее стабильной структурой для циклогексана, была впервые предложена еще в 1890 году Германом Саксом, но получила широкое признание только намного позже. В новом конформации атомы углерода расположены под углом 109,5 °. Половина атомов водорода находится в плоскости кольца (экваториальный), а другая половина перпендикулярна плоскости (осевой). Эта конформация обеспечивает наиболее стабильную структуру циклогексана. Существует еще одна конформация циклогексана, известная как форма лодки, но он преобразуется в более устойчивую форму стула. Если циклогексан является монозамещенным с большим заместитель, то заместитель, скорее всего, будет присоединен в экваториальном положении, так как это немного более стабильный конформация.
Циклогексан имеет самый низкий угол и деформацию при кручении из всех циклоалканов; в результате циклогексан был признан нулевым по общей кольцевой деформации.
Твердые фазы
Циклогексан имеет две кристаллические фазы. Высокотемпературная фаза I, стабильная от 186 К до температуры плавления 280 К, представляет собой пластиковый кристалл, что означает, что молекулы сохраняют некоторую степень свободы вращения. Заказывается низкотемпературная (ниже 186 К) фаза II. Две другие низкотемпературные (метастабильные) фазы III и IV были получены при приложении умеренных давлений выше 30 МПа, при этом фаза IV появляется исключительно в дейтерированный циклогексан (приложение давления увеличивает значения всех температур перехода).[15]
| Нет | Симметрия | Космическая группа | а (Å) | б (Å) | с (Å) | Z | Т (К) | P (МПа) |
|---|---|---|---|---|---|---|---|---|
| я | Кубический | Fm3m | 8.61 | 4 | 195 | 0.1 | ||
| II | Моноклиника | C2 / c | 11.23 | 6.44 | 8.20 | 4 | 115 | 0.1 |
| III | Орторомбический | Пмнн | 6.54 | 7.95 | 5.29 | 2 | 235 | 30 |
| IV | Моноклиника | P12 (1) / n1 | 6.50 | 7.64 | 5.51 | 4 | 160 | 37 |
Здесь Z - количество единиц структуры на ячейка; постоянные элементарной ячейки a, b и c были измерены при заданных температуре T и давлении P.
Смотрите также
- Катастрофа Фликсборо, крупная промышленная авария, вызванная взрывом циклогексана.
- Гексан
- Кольцо флип
- Циклогексан (страница данных)
использованная литература
- ^ Гексанафтен В архиве 2018-02-12 в Wayback Machine, dictionary.com
- ^ «Переднее дело». Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга). Кембридж: Королевское химическое общество. 2014. С. P001 – P004. Дои:10.1039 / 9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ а б c d е Карманный справочник NIOSH по химической опасности. "#0163". Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б «Циклогексан». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ Кэмпбелл, М. Ларри (2011). «Циклогексан». Энциклопедия промышленной химии Ульмана. Дои:10.1002 / 14356007.a08_209.pub2. ISBN 978-3527306732.
- ^ «Стандартные сокращения и акронимы» (PDF). Журнал органической химии.
- ^ Фред Фан Чжан, Томас ван Рейнман, Джи Су Ким, Аллен Ченг «О современных методах гидрирования ароматических соединений с 1945 г. по настоящее время» Лундс Текниска Хёгскола, 2008 г.
- ^ Черезана. «Бензол - Исследование: рынок, анализ, тенденции 2021 года - Ceresana». www.ceresana.com. В архиве из оригинала 21 декабря 2017 г.. Получено 4 мая 2018.
- ^ а б Майкл Таттл Массер (2005). «Циклогексанол и циклогексанон». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a08_217. ISBN 978-3527306732.
- ^ Варнхофф, Э. У. (1996). «Любопытно переплетенные истории бензола и циклогексана». J. Chem. Educ. 73 (6): 494. Bibcode:1996JChEd..73..494W. Дои:10.1021 / ed073p494.
- ^ Бертоле (1867) "Новые приложения методов восстановления в органической химии" (Новые применения методов восстановления в органической химии), Bulletin de la Société chimique de Paris, серия 2, 7 : 53-65.
- ^ Бертоле (1868 г.) "Универсальный метод восстановления и очистки органических соединений" (Универсальный метод восстановления и насыщения органических соединений водородом), Bulletin de la Société chimique de Paris, серия 2, 9 : 8-31. Со страницы 17: "En effet, la benzine, chauffée à 280 ° pendant 24 heures avec 80 fois son poids d'une solution aqueuse saturée à froid d'acide iodhydrique, se change à peu près entièrement en Hydrure d'hexylène, C12ЧАС14, en fixant 4 fois son volume d'hydrogène: C12ЧАС6 + 4H2 = C12ЧАС14 … Карбюратор нового поколения, образованный бензином, является уникальным и определенным: его температура составляет 69 °, и он предлагает все собственные свойства и состав жидкости, экстрагированной для петролей ". (Фактически, бензол, нагретый до 280 ° С в течение 24 часов с массой в 80 раз превышающей его вес водного раствора холодной насыщенной иодистоводородной кислоты, почти полностью превращается в гидрид гексилена, С.12ЧАС14, [Примечание: эта формула для гексана (C6ЧАС14) неверно, потому что химики в то время использовали неправильную атомную массу для углерода.], фиксируя [то есть объединяя с] 4-кратным его объемом водорода: C12ЧАС6 + 4H2 = C12ЧАС14 … Новое углеродное соединение, образованное бензолом, является уникальным и четко определенным веществом: оно кипит при 69 ° и представляет все свойства и состав гидрида гексилена, извлеченного из нефти.)
- ^ Адольф Байер (1870) "Ueber die Reduction aromatischer Kohlenwasserstoffe durch Jodphosphonium" (О восстановлении ароматического соединения йодидом фосфония [H4IP]), Annalen der Chemie und Pharmacie, 155 : 266-281. Со страницы 279: "Bei der Reduction mit Natriumamalgam oder Jodphosphonium addiren sich im höchsten Falle sechs Atome Wasserstoff, und es entstehen Abkömmlinge, die sich von einem Kohlenwasserstoff C6ЧАС12 способный. Dieser Kohlenwasserstoff istaller Wahrscheinlichkeit nach ein geschlossener Ring, da seine Derivate, das Hexahydromesitylen und Hexahydromellithsäure, mit Leichtigkeit wieder в Benzolabkömmlinge übergeführten werden kören körden. (Во время восстановления [бензола] амальгамой натрия или иодидом фосфония в крайнем случае добавляются шесть атомов водорода, и возникают производные, которые происходят из углеводорода C6ЧАС12. Этот углеводород, по всей вероятности, является замкнутым кольцом, поскольку его производные - гексагидромезитилен [1,3,5-триметилциклогексан] и гексагидромеллитовая кислота [циклогексан-1,2,3,4,5,6-гексакарбоновая кислота] - могут быть преобразованы снова в производные бензола.)
- ^ Прайс, Д. М. (1995). «Температурная калибровка дифференциальных сканирующих калориметров». Журнал термического анализа. 45 (6): 1285–1296. Дои:10.1007 / BF02547423.
- ^ а б Mayer, J .; Городской, С .; Хабрило, С .; Holderna, K .; Natkaniec, I .; Würflinger, A .; Zajac, W. (1991). «Изучение рассеяния нейтронов циклогексана C6H12 и C6D12 под высоким давлением». Физика Статус Solidi B. 166 (2): 381. Bibcode:1991ПССБР.166..381М. Дои:10.1002 / pssb.2221660207.
внешние ссылки
| Викискладе есть медиафайлы по теме Циклогексан. |
- Международная карта химической безопасности 0242
- Национальный реестр загрязнителей - информационный бюллетень по циклогексану
- Карманный справочник NIOSH по химической опасности
- Циклогексан @ 3Dchem
- Герман Заксе и первое предположение о конформации стула.
- Банк данных по опасным веществам NLM - Циклогексан
- Метанол обнаружен в космосе
- Расчет давление газа, плотность жидкости, динамическая вязкость жидкости, поверхностное натяжение циклогексана
- Технологическая схема производства циклогексана, метод гидрирования бензола