WikiDer > Атмосферная химия
Атмосферная химия это филиал наука об атмосфере в которой химия из Атмосфера Земли и других планет изучается. Это мультидисциплинарный подход исследований и опирается на химия окружающей среды, физика, метеорология, компьютерное моделирование, океанография, геология и вулканология и другие дисциплины. Исследования все больше связаны с другими областями обучения, такими как климатология.
Состав и химический состав атмосферы Земли важны по нескольким причинам, но в первую очередь из-за взаимодействия между атмосферой и живые организмы. Состав атмосферы Земли изменяется в результате природных процессов, таких как вулкан выбросы, молния и бомбардировка солнечными частицами от корона. Он также был изменен деятельностью человека, и некоторые из этих изменений вредны для здоровья человека, сельскохозяйственных культур и экосистем. Примеры проблем, решаемых с помощью химии атмосферы, включают: кислотный дождь, истощение озонового слоя, фотохимический смог, парниковые газы и глобальное потепление. Атмосферные химики стремятся понять причины этих проблем и, получая их теоретическое понимание, позволяют проверить возможные решения и оценить последствия изменений в государственной политике.
Состав атмосферы

| Средний состав сухой атмосферы (мольные доли) | ||
|---|---|---|
| Газ | на НАСА | |
| Азот, N2 | 78.084% | |
| Кислород, O2[1] | 20.946% | |
| Второстепенные компоненты (мольные доли в промилле) | ||
| Аргон, Ar | 9340 | |
| Углекислый газ, CO2 | 400 | |
| Неон, Ne | 18.18 | |
| Гелий, Он | 5.24 | |
| Метан, CH4 | 1.7 | |
| Криптон, Kr | 1.14 | |
| Водород, H2 | 0.55 | |
| Оксид азота, N2О | 0.5 | |
| Ксенон, Xe | 0.09 | |
| Диоксид азота, НЕТ2 | 0.02 | |
| Вода | ||
| Водяной пар | Высокая вариабельность; обычно составляет около 1% | |
Примечания: концентрация CO2 и CH4 варьироваться в зависимости от сезона и местоположения. Средняя молекулярная масса воздуха 28,97 г / моль. Озон (O3) не включен из-за его высокой изменчивости.
| состав сухого чистого воздуха вблизи уровня моря в соответствии со стандартом ISO 2533 - 1975 | |
|---|---|
| Газ | Содержание тома % |
| Азот, N2 | 78.084 |
| Кислород, O2 | 20.9476 |
| Аргон, Ar | 0.934 |
| Углекислый газ, CO2 | 0.0314 * |
| Неон, Ne | 1.818×10−3 |
| Гелий, Он | 524×10−6 |
| Криптон, Kr | 114×10−6 |
| Ксенон, Xe | 8.7×10−6 |
| Водород, H2 | 50×10−6 |
| Оксид азота, N2О | 50×10−6 |
| Метан, CH4 | 0.2×10−3 |
| Озон, O3, летом | вплоть до 7.0×10−6 * |
| Озон, O3, зимой | вплоть до 2.0×10−6 * |
| Диоксид серы, ТАК2 | вплоть до 0.1×10−3 * |
| Диоксид азота, НЕТ2 | вплоть до 2.0×10−6 * |
| Йод, Я2 | 1.0×10−6* |
| * Содержание газа может значительно меняться время от времени или от места к месту. | |
История
Древний Греки считал воздух одним из четыре элемента. Первые научные исследования состава атмосферы начались в 18 веке, когда химики, такие как Джозеф Пристли, Антуан Лавуазье и Генри Кавендиш произвел первые измерения состава атмосферы.
В конце 19-го и начале 20-го веков интерес сместился в сторону следовых компонентов с очень небольшими концентрациями. Одним из особенно важных открытий для химии атмосферы было открытие озон к Кристиан Фридрих Шёнбейн в 1840 г.
В 20-м веке наука об атмосфере перешла от изучения состава воздуха к рассмотрению того, как со временем меняются концентрации газовых примесей в атмосфере, а также к химическим процессам, которые создают и разрушают соединения в воздухе. Двумя особенно важными примерами этого были объяснения Сидней Чепмен и Гордон Добсон о том, как озоновый слой создается и поддерживается, а объяснение фотохимический смог к Ари Ян Хааген-Смит. Дальнейшие исследования проблем озона привели к присуждению Нобелевской премии по химии 1995 г., разделенной между Пол Крутцен, Марио Молина и Фрэнк Шервуд Роуленд.[2]
В 21 веке акцент снова смещается. Атмосферная химия все чаще изучается как часть Система Земля. Вместо того, чтобы изолированно концентрироваться на химии атмосферы, теперь основное внимание уделяется рассмотрению ее как одной части единой системы с остальными элементами. атмосфера, биосфера и геосфера. Особенно важным фактором этого является связь между химией и климат такие как влияние изменения климата на восстановление озоновой дыры и наоборот, а также взаимодействие состава атмосферы с океанами и земными экосистемы.
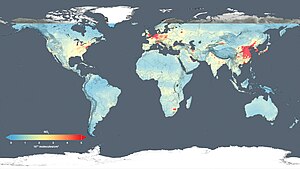
(НАСА симуляция; 9 ноября 2015 г.)
Методология
Наблюдения, лабораторные измерения и моделирование - три центральных элемента в химии атмосферы. Прогресс в химии атмосферы часто обусловлен взаимодействием между этими компонентами, и они образуют единое целое. Например, наблюдения могут сказать нам, что существует больше химического соединения, чем считалось возможным ранее. Это будет стимулировать новые моделирование и лабораторные исследования, которые улучшат наше научное понимание до такой степени, что наблюдения можно будет объяснить.
Наблюдение
Наблюдения за химическим составом атмосферы необходимы для нашего понимания. Регулярные наблюдения за химическим составом говорят нам об изменениях в составе атмосферы с течением времени. Одним из важных примеров этого является Кривая Килинга - серия измерений с 1958 года по сегодняшний день, которые показывают устойчивый рост концентрации углекислый газ (смотрите также текущие измерения атмосферного CO2). Наблюдения за химией атмосферы производятся в обсерваториях, таких как Мауна-Лоа и на мобильных платформах, таких как самолеты (например, британский Установка для измерения атмосферы в воздухе), корабли и воздушные шары. Наблюдения за составом атмосферы все чаще проводят спутники с важными инструментами, такими как GOME и МОПИТТ дает глобальную картину загрязнения воздуха и химического состава. У приземных наблюдений есть то преимущество, что они обеспечивают долгосрочные записи с высоким разрешением по времени, но ограничены в вертикальном и горизонтальном пространстве, из которого они обеспечивают наблюдения. Некоторые инструменты на поверхности, например ЛИДАР могут обеспечивать профили концентрации химических соединений и аэрозолей, но по-прежнему ограничены в горизонтальной области, которую они могут охватить. Многие наблюдения доступны онлайн в Базы данных наблюдений за химией атмосферы.
Лабораторные исследования
Измерения, проводимые в лаборатории, необходимы для нашего понимания источников и стоков загрязнителей и соединений природного происхождения. Эти эксперименты проводятся в контролируемой среде, что позволяет проводить индивидуальную оценку конкретных химических реакций или оценку свойств конкретного компонента атмосферы.[6] Представляющие интерес виды анализа включают анализ газофазных реакций, а также анализ. неоднородный реакции, которые имеют отношение к образованию и росту аэрозоли. Также большое значение имеет изучение атмосферных фотохимия который количественно определяет скорость, с которой молекулы расщепляются солнечным светом, и каковы получаемые продукты. Кроме того, термодинамический данные, такие как Закон Генри коэффициенты также могут быть получены.
Моделирование
Эта секция не цитировать любой источники. (Июнь 2019) (Узнайте, как и когда удалить этот шаблон сообщения) |
Чтобы синтезировать и проверить теоретические представления о химии атмосферы, компьютерные модели (такие как модели химического транспорта) используются. Численные модели решают дифференциальные уравнения, определяющие концентрации химических веществ в атмосфере. Они могут быть очень простыми или очень сложными. Одним из распространенных компромиссов в численных моделях является соотношение количества смоделированных химических соединений и химических реакций и представления о переносе и перемешивании в атмосфере. Например, блочная модель может включать сотни или даже тысячи химических реакций, но будет иметь лишь очень грубое представление о перемешивании в атмосфере. Напротив, трехмерные модели представляют многие физические процессы в атмосфере, но из-за ограничений компьютерных ресурсов в них будет гораздо меньше химических реакций и соединений. Модели можно использовать для интерпретации наблюдений, проверки понимания химических реакций и прогнозирования будущих концентраций химических соединений в атмосфере. Одна из важных текущих тенденций состоит в том, чтобы модули химии атмосферы стали частью моделей земных систем, в которых можно изучать связи между климатом, составом атмосферы и биосферой.
Некоторые модели строятся автоматическими генераторами кода (например, Автохим или же Кинетический препроцессор). В этом подходе выбирается набор составляющих, а затем автоматический генератор кода выбирает реакции с участием этих составляющих из набора баз данных реакций. Как только реакции выбраны, обыкновенные дифференциальные уравнения которые описывают их эволюцию во времени, могут быть построены автоматически.
Смотрите также
| Часть серия на |
| Погода |
|---|
 |
- Кислородный цикл
- Озоново-кислородный цикл
- Палеоклиматология
- Научная оценка разрушения озона
- События разрушения тропосферного озона
Рекомендации
- ^ Циммер, Карл (3 октября 2013 г.). "Кислород Земли: загадка, которую легко принять на веру". Нью-Йорк Таймс. Получено 3 октября 2013.
- ^ "Пресс-релиз - Нобелевская премия по химии 1995 г.". Нобелевская премия. Нобелевская премия Org. 11 октября 1995 г.
- ^ Санкт-Флер, Николас (10 ноября 2015 г.). «Уровень парниковых газов в атмосфере стал рекордным, говорится в отчете». Нью-Йорк Таймс. Получено 11 ноября 2015.
- ^ Риттер, Карл (9 ноября 2015 г.). "Великобритания: на первом месте средняя мировая температура может быть на 1 градус Цельсия выше". AP Новости. Получено 11 ноября 2015.
- ^ Коул, Стив; Грей, Эллен (14 декабря 2015 г.). «Новые спутниковые карты НАСА показывают глобальное качество воздуха по отпечатку пальца человека». НАСА. Получено 14 декабря 2015.
- ^ Национальные академии наук, инженерии и медицины (2016). Будущее атмосферных исследований: вспомнить вчера, понять сегодня, предвидеть завтрашний день. Вашингтон, округ Колумбия: The National Academies Press. п. 15. ISBN 978-0-309-44565-8.
дальнейшее чтение
- Brasseur, Guy P .; Орландо, Джон Дж .; Тиндалл, Джеффри С. (1999). Атмосферная химия и глобальные изменения. Издательство Оксфордского университета. ISBN 0-19-510521-4.
- Финлейсон-Питтс, Барбара Дж .; Питтс, Джеймс Н., младший (2000). Химия верхней и нижней атмосферы. Академическая пресса. ISBN 0-12-257060-X.
- Сайнфелд, Джон Х .; Пандис, Спирос Н. (2006). Химия и физика атмосферы: от загрязнения воздуха до изменения климата (2-е изд.). John Wiley and Sons, Inc. ISBN 0-471-82857-2.
- Варнек, Питер (2000). Химия естественной атмосферы (2-е изд.). Академическая пресса. ISBN 0-12-735632-0.
- Уэйн, Ричард П. (2000). Химия атмосферы (3-е изд.). Издательство Оксфордского университета. ISBN 0-19-850375-X.
- Дж. В. Ирибарн, Х. Р. Чо, Атмосферная физика, D. Reidel Publishing Company, 1980 г.
внешняя ссылка
- Научная оценка ВМО истощения озонового слоя: 2006 г.
- IGAC Международный проект по глобальной химии атмосферы
- Пол Крутцен Интервью Freeview видео Пол Крутцен Нобелевский лауреат за свою работу по разложению озона в беседе с Нобелевским лауреатом Гарри Крото, то Vega Science Trust.
- Кембриджская база данных по химии атмосферы - это большая составная база данных наблюдений в общем формате.
- Наука об окружающей среде опубликована для всех вокруг Земли
- Химическая кинетика и фотохимические данные NASA-JPL для использования в исследованиях атмосферы
- Кинетические и фотохимические данные оцениваются Подкомитетом ИЮПАК по оценке газокинетических данных
- Глоссарий по химии атмосферы в Государственный университет Сэма Хьюстона
- Химия тропосферы
- Калькуляторы для использования в химии атмосферы
- Иллюстрированная элементарная оценка состава воздуха.