WikiDer > Щелкните по химии
В химический синтез, "щелкнуть" по химии это класс биосовместимый малая молекула реакции, обычно используемые в биоконъюгация, позволяя соединять выбранные субстраты с конкретными биомолекулами. Химия щелчка - это не отдельная конкретная реакция, а описание способа получения продуктов, которые следуют примерам в природа, который также генерирует вещества путем объединения небольших модульных единиц. Во многих приложениях реакции щелчка присоединяются к биомолекула и репортерная молекула. Химия щелчка не ограничивается биологическими условиями: концепция реакции щелчка использовалась в фармакологии и различных биомиметических приложениях. Однако они стали особенно полезными для обнаружения, локализации и квалификации биомолекул.
Щелчки происходят в один горшок, не беспокоит воды, генерируют минимальные и безобидные побочные продукты и являются «подпружиненными» - характеризуются высокой термодинамической движущей силой, которая быстро и необратимо приводит к высокому выходу единственного продукта реакции с высокой специфичностью реакции (в некоторых случаях с обоими регионами) и стерео-специфичность). Эти качества делают щелчковые реакции особенно подходящими для задачи выделения и нацеливания молекул в сложных биологических средах. В такой среде продукты соответственно должны быть физиологически стабильными, а любые побочные продукты - нетоксичными (для in vivo системы).
Разрабатывая конкретные и контролируемые биоортогональный реакции, ученые открыли возможность поражать определенные цели в сложных лизатах клеток. Недавно ученые адаптировали химию щелчков для использования в живых клетках, например, используя зонды с небольшими молекулами, которые находят свои цели и прикрепляются к ним с помощью реакций щелчка. Несмотря на проблемы проницаемости клеток, биоортогональности, фоновой маркировки и эффективности реакции, щелчковые реакции уже доказали свою полезность в новом поколении тянуть вниз эксперименты (в которых конкретные мишени могут быть выделены с использованием, например, репортерных молекул, которые связываются с определенным столбцом), и флуоресцентная спектрометрия (в которой флуорофор прикреплен к интересующей цели, и цель количественно определена или расположена). Совсем недавно были использованы новые методы для включения партнеров реакции щелчка в биомолекулы и в них, включая включение неприродные аминокислоты содержащие реактивные группы в белки и модификация нуклеотиды. Эти методы представляют собой часть области химическая биология, в котором химия щелчков играет фундаментальную роль за счет намеренного и целенаправленного подключения модульных блоков к различным концам.
Термин «химия кликов» был придуман К. Барри Шарплесс в 1998 году и впервые полностью описан Шарплессом, Хартмутом Кольбом и М. Финн из Научно-исследовательский институт Скриппса в 2001.[1][2]
Фон
Click Chemistry - это метод крепления зонд или же субстрат представляющий интерес для конкретной биомолекулы, процесс, называемый биоконъюгация. Возможность крепления флуорофоры и другие репортерные молекулы сделал клик-химию очень мощным инструментом для идентификации, определения местоположения и характеристики как старых, так и новых биомолекул.
Одним из первых и наиболее важных методов биоконъюгации было экспрессирование репортера на одном и том же открытая рамка чтения как представляющая интерес биомолекула. В частности, GFP был впервые (и до сих пор) экспрессируется таким образом на N- или C-конце многих белков. Однако этот подход сопряжен с рядом трудностей. Например, GFP - это очень большая единица, которая часто может влиять на сворачивание интересующего белка. Более того, будучи экспрессируемым на любом конце, аддукт GFP также может влиять на нацеливание и экспрессию желаемого белка. Наконец, используя этот метод, GFP может быть прикреплен только к белкам, а не посттрансляционно, оставляя другие важные биомолекулярные классы (нуклеиновые кислоты, липиды, углеводыи т. д.) вне досягаемости.
Чтобы преодолеть эти проблемы, химики решили продолжить определение пар биоортогональный партнеров по реакции, что позволяет использовать небольшие экзогенный молекулы как биомолекулярные зонды. К одному из этих зондов может быть присоединен флуорофор, чтобы давать сигнал флуоресценции при связывании репортерной молекулы с мишенью - точно так же, как GFP флуоресцирует, когда он экспрессируется с мишенью.
Теперь ограничения возникают из-за химического состава зонда по отношению к его цели. Для того, чтобы этот метод был применим в биологических системах, химия щелчков должна работать в биологических условиях или около них, производить мало и (в идеале) нетоксичных побочных продуктов, иметь (предпочтительно) отдельные и стабильные продукты в тех же условиях и быстро переходить к высокая доходность в один горшок. Существующие реакции, такие как Лигирование по Штаудингеру и Huisgen 1,3-диполярное циклоприсоединение, были модифицированы и оптимизированы для таких условий реакции. Сегодня исследования в этой области касаются не только понимания и разработки новых реакций, перепрофилирования и переосмысления известных реакций, но и расширения методов, используемых для включения партнеров реакции в живые системы, разработки новых партнеров реакции и разработки приложений для биоконъюгации.
Реакции
Чтобы реакция считалась реакцией на щелчок, она должна соответствовать определенным характеристикам:[3]
- модульность
- нечувствительность к параметрам растворителя
- высоко химические выходы
- нечувствительность к кислороду и воде
- региоспецифичность и стереоспецифичность
- большая термодинамическая движущая сила (> 20 ккал/моль) в пользу реакции с одним продуктом реакции. Отчетливая экзотермическая реакция делает реагент «подпружиненным».
Желательно, чтобы процесс:
- иметь простые условия реакции
- использовать легкодоступные исходные материалы и реагенты
- не используйте растворитель или используйте безвредный или легко удаляемый растворитель (предпочтительно воду)
- обеспечивают простое выделение продукта нехроматографическими методами (кристаллизация или же дистилляция)
- иметь высокий атомная экономика.
Многие критерии химии щелчков являются субъективными, и даже если измеримые и объективные критерии могут быть согласованы, маловероятно, что какая-либо реакция будет идеальной для каждой ситуации и приложения. Однако было выявлено несколько реакций, которые лучше других соответствуют этой концепции:[требуется разъяснение]
- [3+2] циклоприсоединения, такой как 1,3-диполярное циклоприсоединение Huisgen, в частности, ступенчатый вариант, катализируемый Cu (I),[4] часто называют реакцией на клик
- Тиол-еновая реакция[5][6]
- Реакция Дильса-Альдера и обратная реакция Дильса-Альдера на электронное потребление[7][8]
- [4+1] циклоприсоединения между изонитрилами (изоцианидами) и тетразинами[9]
- нуклеофильное замещение особенно маленьким напряженный кольца как эпоксидная смола [10] и азиридины
- карбонильно-химическое образование мочевина но не реакции альдол типа из-за низкой термодинамической движущей силы.
- реакции присоединения на углерод-углерод двойные связи подобно дигидроксилирование или алкины в тиолиновая реакция. [3]
Азид-алкиновое циклоприсоединение, катализируемое медью (I) (CuAAC)
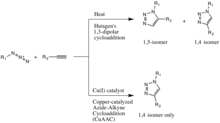
Классический[11][12] реакция щелчка - это катализируемая медью реакция азид с алкин образовывать 5-членный гетероатом кольцо: азид-алкин, катализируемый Cu (I) циклоприсоединение (CuAAC). Первый триазол синтез из диэтилацетилендикарбоксилата и фенилазида был описан Артур Майкл в 1893 г.[13] Позже, в середине ХХ века, это семейство 1,3-диполярных циклоприсоединений приобрело Huisgen's имя в честь его исследований их реакции кинетика и условия.
Катализ меди (I) 1,3-диполярного циклоприсоединения Хьюсгена был открыт одновременно и независимо группами Валерия В. Фокина и К. Барри Шарплесс на Научно-исследовательский институт Скриппса в Калифорния[14] и Мортен Мелдал в Лаборатория Carlsberg, Дания.[15] Вариант этой реакции, катализируемый медью, дает только 1,4-изомер, в то время как некатализируемое 1,3-диполярное циклоприсоединение Хьюсгена дает как 1,4-, так и 1,5-изомеры, является медленным и требует температуры 100 градусов по Цельсию.[13]
Более того, этот катализируемый медью «щелчок» не требует наличия лигандов на металле, хотя сообщалось об ускоряющих лигандах, таких как трис (триазолил) метиламинные лиганды с различными заместителями, и они с успехом использовались в водном растворе.[13] Также можно использовать другие лиганды, такие как PPh3 и TBIA, даже если PPh3 подвержен лигированию по Штаудингеру с азидным заместителем. Cu2Было обнаружено, что O в воде при комнатной температуре также катализирует ту же реакцию за 15 минут с выходом 91%.[16]
Первый предложенный механизм реакции включал один каталитический атом меди; но изотопные, кинетические и другие исследования показали, что более актуальным может быть механизм дикоппера.[17][18][19][20][21] Несмотря на то, что эта реакция эффективно протекает в биологических условиях, медь в этом диапазоне доз является цитотоксической. Были представлены решения этой проблемы, такие как использование водорастворимых лигандов на меди для улучшения проникновения катализатора в клетки и, таким образом, уменьшения необходимой дозировки,[22][23][24] или использовать хелатирующие лиганды для дальнейшего увеличения эффективной концентрации Cu (I) и, таким образом, уменьшения фактической дозировки.[25][26][27]
Хотя вариант, катализируемый Cu (I), впервые был описан Мелдалом и его сотрудниками для синтеза пептидотриазолы при твердой поддержке им потребовалось больше времени, чтобы в полной мере оценить реакцию, и их обогнал более признанный в обществе Шарплесс. Мелдал и его сотрудники также предпочли не называть этот тип реакции «щелочной химией», что якобы привело к тому, что их открытие в значительной степени не было замечено основным химическим обществом. Шарплесс и Фокин независимо друг от друга описали его как надежный каталитический процесс, предлагающий «беспрецедентный уровень селективности, надежности и возможностей для тех усилий по органическому синтезу, которые зависят от создания ковалентных связей между различными строительными блоками».
Об аналогичной реакции RuAAC, катализируемой рутением вместо меди, сообщили группы Цзя и Фолкина в 2005 году, и она позволяет селективно получать 1,5-изомеры.[28]
Азид-алкиновое циклоприсоединение, стимулируемое напряжением (SPAAC)
Группа Бертоцци дополнительно разработала одну из щелочных реакций Хейсгена без содержания меди, чтобы преодолеть цитотоксичность реакции CuAAC.[29] Вместо использования Cu (I) для активации алкина, алкин вводится в напряженный дифтороктин (DIFO), в котором электроноакцепторные пропаргиловые гем-фторины действуют вместе с кольцевым штаммом, сильно дестабилизируя алкин.[30] Эта дестабилизация увеличивает движущую силу реакции и желание циклоалкина ослабить его кольцевую деформацию.
Эта реакция протекает как согласованное [3 + 2] циклоприсоединение по тому же механизму, что и 1,3-диполярное циклоприсоединение Huisgen. Заместители, отличные от фтора, такие как бензольные кольца, также допускаются в циклооктине.
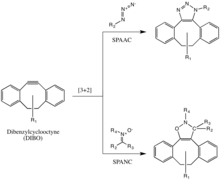
Эта реакция успешно использовалась для исследования азидов в живых системах, хотя скорость реакции несколько ниже, чем у CuAAC. Более того, поскольку синтез циклооктинов часто дает низкий выход, разработка зондов для этой реакции не была такой быстрой, как для других реакций. Но производные циклооктина, такие как DIFO, дибензилциклооктин (DIBO) и биарилазациклооктинон (BARAC), были успешно использованы в реакции SPAAC для исследования азидов в живых системах.[31][32][33]
Штамм-промотируемое циклоприсоединение алкин-нитрон (SPANC)
Диарил-напряженные циклооктины, включая дибензилциклооктин (DIBO), также использовались для взаимодействия с 1,3-нитронами в штамм-промотированных циклоприсоединениях алкин-нитрон (SPANC) с образованием N-алкилированных изоксазолинов.[34]
Поскольку эта реакция не содержит металлов и протекает с быстрой кинетикой (k2 составляет 60 л / мс, быстрее, чем CuAAC или SPAAC), SPANC можно использовать для мечения живых клеток. Более того, допускается замещение атомов углерода и азота нитронного диполя, а также ациклических и эндоциклических нитронов. Этот большой допуск обеспечивает большую гибкость при установке нитронной ручки или зонда.[35]
Однако изоксазолиновый продукт не так стабилен, как триазольный продукт CuAAC и SpAAC, и может подвергаться перегруппировке в биологических условиях. Несмотря на это, эта реакция по-прежнему очень полезна, так как имеет очень быструю кинетику реакции.[34]
Применение этой реакции включает маркировку белков, содержащих серин в качестве первого остатка: серин окисляется до альдегида с помощью NaIO.4 и затем превращают в нитрон с помощью п-метоксибензолтиола, N-метилгидроксиламина и п-ансидина и, наконец, инкубируют с циклооктином с получением продукта щелчка. SPANC также позволяет осуществлять мультиплексную маркировку.[36][37]
Реакции напряженных алкенов
Напряженные алкены также используют снятие напряжения в качестве движущей силы, которая позволяет им участвовать в щелчковых реакциях. Трансциклоалкены (обычно циклооктены) и другие напряженные алкены, такие как оксанорборнадиен, вступают в реакцию щелчка с рядом партнеров, включая азиды, тетразины и тетразолы. Эти партнеры по реакции могут специфически взаимодействовать с напряженным алкеном, оставаясь биоортогональными по отношению к эндогенным алкенам, содержащимся в липидах, жирных кислотах, кофакторах и других природных продуктах.[36]
Алкен и азид [3 + 2] циклоприсоединение
Оксанорборнадиен (или другой активированный алкен) реагирует с азидами, давая в качестве продукта триазолы. Однако эти триазолы не являются ароматическими, как в реакциях CuAAC или SPAAC, и в результате не так стабильны. Активированная двойная связь в оксаноборнадиене образует промежуточный триазолин, который впоследствии самопроизвольно подвергается ретро-реакции Дильса-Альдера с высвобождением фурана и образованием 1,2,3- или 1,4,5-триазолов. Несмотря на то, что эта реакция протекает медленно, она полезна, потому что оксаборнодиен относительно просто синтезировать. Однако реакция не является полностью хемоселективной.[38]
Алкены и тетразин с обратным спросом по Дильсу-Альдеру
Напряженные циклооктены и другие активированные алкены реагируют с тетразинами по обратному электронному требованию Дильса-Альдера с последующим ретро [4 + 2] циклоприсоединением (см. Рисунок).[39] Подобно другим реакциям трансциклооктена, снятие напряжения кольца является движущей силой этой реакции. Таким образом, трехчленные и четырехчленные циклоалкены из-за их высокой кольцевой деформации составляют идеальные алкеновые субстраты.[39]
Подобно другим [4 + 2] циклоприсоединениям, электронодонорные заместители в диенофиле и электроноакцепторные заместители в диене ускоряют диильс-альдровую реакцию с обратной потребностью. Диен, тетразин, благодаря наличию дополнительных атомов азота, является хорошим диеном для этой реакции. Диенофил, активированный алкен, часто может быть присоединен к электронодонорным алкильным группам целевых молекул, что делает диенофил более подходящим для реакции.[40]
Алкен и тетразол фотоклик реакция
Реакция тетразол-алкенового «фотоклика» - это еще одно диполярное соединение, которое Huisgen впервые ввел около 50 лет назад (ChemBioChem 2007, 8, 1504. (68) Clovis, JS; Eckell, A .; Huisgen, R .; Sustmann, R. Chem. . Ber. 1967, 100, 60). Тетразолы с амино- или стирильными группами, которые могут быть активированы УФ-светом на длине волны 365 нм (365 не повреждает клетки), реагируют быстро (так что УФ-свет не должен быть включен в течение длительного времени. время, обычно около 1–4 минут) для производства флуорогенных пиразолиновых продуктов. Эта схема реакции хорошо подходит для целей мечения живых клеток, потому что УФ-свет на длине волны 365 нм минимально повреждает клетки. Более того, реакция протекает быстро, так что УФ-свет можно использовать в течение короткого времени. Квантовый выход для коротковолнового УФ-света может быть выше 0,5. Это позволяет использовать тетразолы по длине волны избирательно в сочетании с другой реакцией фотолигирования, где на короткой длине волны реакция лигирования тетразола протекает почти исключительно, а при более длинной длине волны протекает исключительно другая реакция (лигирование через о-хинодиметаны).[41] Наконец, нефлуорогенные реагенты приводят к образованию флюорогенного продукта, что обеспечивает реакцию встроенной спектрометрической ручкой.
И тетразолы, и алкеновые группы были включены в состав белков как неприродные аминокислоты, но это преимущество не является уникальным. Вместо этого фотоиндуцируемость реакции делает ее главным кандидатом на пространственно-временную специфичность в живых системах. Проблемы включают присутствие эндогенных алкенов, хотя обычно цис (как в жирных кислотах) они все еще могут реагировать с активированным тетразолом.[42]
Возможные приложения
Коммерческий потенциал клик-химии велик. Флуорофор родамин был присоединен к норбонену и реагировал с тетразином в живых системах.[43] В других случаях SPAAC между флуорофором, модифицированным циклооктином, и белками, меченными азидом, позволял отобрать эти белки в клеточных лизатах.[44]
Способы включения партнеров реакции щелчка в системы in и ex vivo вносят свой вклад в диапазон возможных реакций. Развитие включения неприродных аминокислот рибосомами позволило включить партнеров реакции щелчка в качестве неприродных боковых групп в этих неприродных аминокислотах. Например, UAA с боковой азидной группой обеспечивает удобный доступ циклоалкинов к белкам, меченным этой неприродной аминокислотой «AHA».[45] В другом примере «CpK» имеет боковую группу, включающую альфа-циклопропан с амидной связью, которая служит партнером по реакции тетразина в обратной реакции Дильса-Альдера.[46]
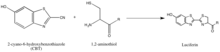
Синтез люциферин иллюстрирует другую стратегию выделения партнеров реакции, которая заключается в использовании редко встречающихся природных групп, таких как 1,2-аминотиол, который появляется только тогда, когда цистеин является последней аминокислотой N ’в белке. Их естественная селективность и относительная биоортогональность, таким образом, важны для разработки зондов, специфичных для этих меток. Вышеуказанная реакция происходит между 1,2-аминотиолом и 2-цианобензотиазолом с образованием люциферина, который является флуоресцентным. Эту флуоресценцию люциферина можно затем количественно оценить спектрометрией после промывки и использовать для определения относительного присутствия молекулы, несущей 1,2-аминотиол. Если требуется количественная оценка белка, не несущего 1,2-аминотиол, представляющий интерес белок может быть расщеплен с образованием фрагмента с N ’Cys, который уязвим для 2-CBT.[47]
Дополнительные приложения включают:
- Двумерный гель-электрофорез разделение[48]
- препаративный органический синтез 1,4-замещенных триазолы
- модификация функции пептида с помощью триазолов
- модификация натуральных продуктов и фармацевтических препаратов
- натуральный продукт открытие [49]
- открытие лекарств
- макроциклизации с использованием триазольных сочетаний, катализируемых Cu (I)
- модификация ДНК и нуклеотиды путем лигирования триазолом
- супрамолекулярная химия: каликсарены, ротаксаны, и катенаны
- дендример дизайн
- углевод кластеры и конъюгация углеводов с помощью реакций лигирования триазола, катализируемых Cu (1)
- Полимеры и Биополимеры [50]
- поверхности[51]
- материаловедение
- нанотехнологии[52] и
- Биоконъюгирование, например, азидокумарин.
- Биоматериалы[53]
В комбинации с комбинаторная химия, высокопроизводительный скрининг, и строительство химические библиотекихимия ускорила открытие новых лекарств, заставляя каждую реакцию многоступенчатый синтез быстро, эффективно и предсказуемо.
Лицензия на технологию
Исследовательский институт Скриппса имеет портфель патентов на химические технологии.[54] Лицензиаты включают Invitrogen,[55] Аллозин,[56] Элерон,[57] Комплексная диагностика,[58] и биотехнологическая компания baseclick, дочерняя компания BASF, созданная для продажи продуктов, изготовленных с использованием химии щелчков.[59] Кроме того, baseclick имеет эксклюзивную лицензию на мировой рынок исследований и диагностики в области нуклеиновых кислот. Флуоресцентные азиды и алкины также производятся такими компаниями, как Active Motif Chromeon.[60] и Cyandye
Смотрите также
Рекомендации
- ^ Х. К. Кольб; М. Г. Финн; К. Б. Шарплесс (2001). «Щелкните Химия: Разнообразная химическая функция из нескольких хороших реакций». Angewandte Chemie International Edition. 40 (11): 2004–2021. Дои:10.1002 / 1521-3773 (20010601) 40:11 <2004 :: AID-ANIE2004> 3.0.CO; 2-5. PMID 11433435.
- ^ Р. А. Эванс (2007). «Повышение уровня азид-алкинового 1,3-диполярного« щелочного »циклоприсоединения и его применение в науке о полимерах и модификации поверхности». Австралийский химический журнал. 60 (6): 384–395. Дои:10.1071 / CH06457.
- ^ а б Стереолитография полимерной керамики с помощью Thiol-Ene Click Chemistry
- ^ Спитери, Кристиан; Моисей, Джон Э. (2010). «Азид-алкиновое циклоприсоединение, катализируемое медью: региоселективный синтез 1,4,5-тризамещенных 1,2,3-триазолов». Angewandte Chemie International Edition. 49 (1): 31–33. Дои:10.1002 / anie.200905322. PMID 19921729.
- ^ Хойл, Чарльз Э .; Боуман, Кристофер Н. (2010). «Химия тиол – эне клик». Angewandte Chemie International Edition. 49 (9): 1540–1573. Дои:10.1002 / anie.200903924. PMID 20166107.
- ^ Лоу, А. Б. Полимерная химия 2010, 1 (1), 17–36. DOI: 10.1039 / B9PY00216B
- ^ Блэкман, Мелисса Л .; Ройзен Максим; Фокс, Джозеф М. (2008). «Лигирование тетразина: быстрое биоконъюгирование на основе реакции Дильса-Альдера с обратным электронным запросом». Журнал Американского химического общества. 130 (41): 13518–13519. Дои:10.1021 / ja8053805. ЧВК 2653060. PMID 18798613.
- ^ Деварадж, Нил К .; Вайследер Ральф и Хильдербранд, Скотт А. (2008). «Циклоприсоединения на основе тетразина: применение для предварительно заданного мечения живых клеток». Биоконъюгат химия. 19 (12): 2297–2299. Дои:10.1021 / bc8004446. ЧВК 2677645. PMID 19053305.
- ^ Штёкманн, Хеннинг; Невес, Андре; Лестница, Шон; Бриндл, Кевин; Липер, Финиан (2011). «Изучение щелочной химии на основе изонитрила для лигирования с биомолекулами». Органическая и биомолекулярная химия. 9 (21): 7303–5. Дои:10.1039 / C1OB06424J. PMID 21915395.
- ^ Кашемиров, Борис А .; Бала, Джой Л. Ф .; Чен, Сяолань; Ebetino, F.H .; Ся, Чжидао; Russell, R. Graham G .; Coxon, Fraser P .; Рулофс, Анке Дж .; Роджерс Майкл Дж .; Маккенна, Чарльз Э. (2008). «Флуоресцентно меченый ризедронат и родственные ему аналоги: синтез« магического линкера »». Биоконъюгат химия. 19 (12): 2308–2310. Дои:10.1021 / bc800369c. PMID 19032080.
- ^ Разработка и применение Click Chemistry Грегори С. Паттон 8 ноября г., 2004 http://www.scs.uiuc.edu Интернет[постоянная мертвая ссылка]
- ^ Kolb, H.C .; Шарплесс, Б. (2003). «Растущее влияние химии щелчков на открытие лекарств». Drug Discov сегодня. 8 (24): 1128–1137. Дои:10.1016 / S1359-6446 (03) 02933-7. PMID 14678739.
- ^ а б c Л. Лян и Д. Аструк: «Катализируемая медью (I) алкино-азидная циклоприсоединение (CuAAC)« щелчка »реакция и ее применения. Обзор», 2011; 255, 23-24, 2933-2045, стр. 2934
- ^ Ростовцев, Всеволод В .; Грин, Люк Джи; Фокин, Валерий В .; Шарплесс, К. Барри (2002). «Поэтапный процесс циклоприсоединения по Хьюисгену: региоселективное« лигирование »азидов и концевых алкинов, катализируемое медью (I)». Angewandte Chemie International Edition. 41 (14): 2596–2599. Дои:10.1002 / 1521-3773 (20020715) 41:14 <2596 :: aid-anie2596> 3.0.co; 2-4. PMID 12203546.
- ^ Tornoe, C.W .; Christensen, C .; Мелдал, М. (2002). "Пептидотриазолы на твердой фазе: [1,2,3] -Триазолы региоспецифическими медь (I) -катализированными 1,3-диполярными циклоприсоединениями концевых алкинов к азидам". Журнал органической химии. 67 (9): 3057–3064. Дои:10.1021 / jo011148j. PMID 11975567.
- ^ К. Ван, Х. Би, С. Син, П. Ляо, З. Фанг, Х. Мэн, К. Чжан, К. Лю, Ю. Цзи Green Chem., 13 (2011), с. 562
- ^ Б. Т. Уоррелл, Дж. А. Малик, В. В. Фокин 2013, 340, 457-459; J.E. Hein, В.В. Фокин, Хим. Soc. Ред. 39 (2010) 1302.
- ^ Родионов, Валентин О .; Фокин, Валерий В .; Финн, М. Г. (2005-04-08). "Механизм реакции азид-алкинового циклоприсоединения, катализируемой CuI без лиганда". Angewandte Chemie International Edition. 44 (15): 2210–2215. Дои:10.1002 / anie.200461496. ISSN 1521-3773. PMID 15693051.
- ^ Якобуччи, Клаудио; Реале, Саманта; Галь, Жан-Франсуа; Де Анжелис, Франческо (02.03.2015). «Двухъядерные промежуточные соединения меди в катализируемом медью (I) азид-алкиновом циклоприсоединении, непосредственно наблюдаемом с помощью масс-спектрометрии с ионизацией электрораспылением». Angewandte Chemie International Edition. 54 (10): 3065–3068. Дои:10.1002 / anie.201410301. ISSN 1521-3773. PMID 25614295.
- ^ Озкилыч, Йылмаз; Тюзюн, Нуркан Ş. (2016-08-22). "Исследование двухъядерной реакции CuAAC: механизм в свете новых экспериментов". Металлоорганические соединения. 35 (16): 2589–2599. Дои:10.1021 / acs.organomet.6b00279. ISSN 0276-7333.
- ^ Ziegler, Micah S .; Лакшми, К. В .; Тилли, Т. Дон (2017-04-19). «Комплексы Dicopper Cu (I) Cu (I) и Cu (I) Cu (II) в азидно-алкиновом циклоприсоединении, катализируемом медью» (PDF). Журнал Американского химического общества. 139 (15): 5378–5386. Дои:10.1021 / jacs.6b13261. ISSN 0002-7863. PMID 28394586.
- ^ Brotherton, W. S .; Michaels, H.A .; Simmons, J. T .; Clark, R.J .; Dalal, N. S .; Zhu, L. Org. Lett. 2009, 11, 4954.
- ^ Kuang, G.-C .; Michaels, H.A .; Simmons, J. T .; Clark, R.J .; Чжу, L " J. Org. Chem. 2010; 75, 6540.
- ^ Uttamapinant, C .; Tangpeerachaikul, A .; Греческий, S .; Clarke, S .; Singh, U .; Slade, P .; Джи, К. Р .; Тинг, А. И " Энгью. Chem. Int. Эд. 2012; 51, 5852
- ^ Ольха, К .; Stein, G .; Финценхаген, Х. Юстус Либигс Ann. Chem 1931, 485, 211.
- ^ Ольха, К .; Stein, G. Justus Liebigs Ann. Chem. 1933, 501, 1.
- ^ Wittig, G .; Krebs, A. Chem. Бер. 1961, 94, 3260.
- ^ Чжан, Ли; Чен, Ксинго; Сюэ, Пэн; Sun, Herman H. Y .; Уильямс, Ян Д.; Шарплесс, К. Барри; Фокин, Валерий В .; Цзя, Гочен (ноябрь 2005 г.). «Катализируемое рутением циклоприсоединение алкинов и органических азидов». Журнал Американского химического общества. 127 (46): 15998–15999. Дои:10.1021 / ja054114s. PMID 16287266.
- ^ Хейсген, Р. Энгью. Chem. Int. Эд. Англ. 1963, 2, 565
Agard, N.J .; Baskin, J.M .; Прешер, Дж. А .; Lo, A .; Бертоцци, К. Р. (2006). «Сравнительное исследование биоортогональных реакций с азидами». ACS Chem. Биол. 1 (10): 644–648. Дои:10.1021 / cb6003228. PMID 17175580.
- ^ Agard, N.J .; Baskin, J.M .; Прешер, Дж. А .; Lo, A .; Бертоцци, К. Р. (2006). «Сравнительное исследование биоортогональных реакций с азидами». ACS Chem. Биол. 1 (10): 644–648. Дои:10.1021 / cb6003228. PMID 17175580.
- ^ Codelli, J. A .; Baskin, J.M .; Agard, N.J .; Бертоцци, К. Р. (2008). «Дифторированные циклооктины второго поколения для щелочной химии без меди». Варенье. Chem. Soc. 130 (34): 11486–11493. Дои:10.1021 / ja803086r. ЧВК 2646667. PMID 18680289.
- ^ Нин, X .; Guo, J .; Wolfert, M. A .; Бунс, Г.-Дж. (2008). «Визуализация метаболически меченных гликоконъюгатов живых клеток с помощью свободных от меди и быстрых циклоприсоединений Huisgen». Энгью. Chem. Int. Эд. 47 (12): 2253–2255. Дои:10.1002 / anie.200705456. ЧВК 2835304. PMID 18275058.
- ^ Gordon, C.G .; Mackey, J. L .; Jewett, J.C .; Sletten, E.M .; Houk, K. N .; Бертоцци, К. Р. (2012). «Реакционная способность биарилазациклооктинонов в щелочной химии без меди». Варенье. Chem. Soc. 134 (22): 9199–9208. Дои:10.1021 / ja3000936. ЧВК 3368396. PMID 22553995.
- ^ а б MacKenzie, DA; Sherratt, AR; Чигринова, М; Cheung, LL; Pezacki, JP (август 2014 г.). «Штамм-промотируемые циклоприсоединения с участием нитронов и алкинов - быстро настраиваемые реакции для биоортогонального мечения». Curr Opin Chem Biol. 21: 81–8. Дои:10.1016 / j.cbpa.2014.05.023. PMID 25022431.
- ^ (64) (a) Ning, X .; Temming, R.P .; Dommerholt, J .; Guo, J .; Ania, D.B .; Дебец, М. Ф .; Wolfert, M. A .; Бунс, Г.-Дж .; ван Делфт, Ф. Л " Энгью. Chem. Int. Эд. 2010; 49, 3065. (b) McKay, C.S .; Moran, J .; Pezacki, J. P. Chem. Commun. (Кембридж, У. К.) 2010, 46, 931. (c) Debets, M. F .; ван Беркель, С. С .; Dommerholt, J .; Dirks, A. T. J .; Rutjes, F. P. J. T .; van Delft, F. L. Acc. Chem. Res. 2011, 44, 805. (d) McKay, C.S .; Чигринова, М .; Blake, J. A .; Pezacki, J. P. Org. Biomol. Chem. 2012, 10, 3066.
- ^ а б Lang, K .; Чин, Дж. (2014).«Биоортогональные реакции для маркировки белков». ACS Chem. Биол. 9 (1): 16–20. Дои:10.1021 / cb4009292. PMID 24432752.
- ^ MacKenzie, DA; Pezacki, JP (2014). «Кинетические исследования быстрых деформационно-стимулированных [3 + 2] циклоприсоединений нитронов с бицикло [6.1.0] нонином». Может J Chem. 92 (4): 337–340. Дои:10.1139 / cjc-2013-0577.
- ^ (67) (a) van Berkel, S. S .; Dirks, A. T. J .; Meeuwissen, S.A .; Pingen, D. L. L .; Boerman, O.C .; Laverman, P .; van Delft, F. L .; Корнелиссен, Дж. Дж. Л. М .; Rutjes, F. P. J. T. ChemBioChem 2008, 9, 1805. (b) van Berkel, S. S .; Dirks, A. T. J .; Дебец, М. Ф .; van Delft, F. L .; Корнелиссен, Дж. Дж. Л. М .; Nolte, R.J.M .; Rutjes, F. P. J. T. ChemBioChem 2007, 8, 150
- ^ а б Лю, Фанг; Патон, Роберт С .; Ким, Сеона; Лян, Юн; Хоук, К. Н. (2013). "Реакционная способность Дильса-Альдера деформированных и недеформированных циклоалкенов с диенами с нормальным и обратным электронным запросом: активационные барьеры и анализ искажения / взаимодействия". Варенье. Chem. Soc. 135 (41): 15642–15649. Дои:10.1021 / ja408437u. PMID 24044412.
- ^ Ридер, Ульрике; Людтке, Натан В. (25 августа 2014 г.). «Лигирование алкен-тетразин для визуализации клеточной ДНК». Angew Chem Int Ed Engl. 53 (35): 9168–9172. Дои:10.1002 / anie.201403580. PMID 24981416.
- ^ Menzel, Jan P .; Файст, Флориан; Тутен, Брайан; Вейль, Таня; Блинко, Джеймс П .; Барнер ‐ Коволлик, Кристофер (2019). «Формирование ортогональных ковалентных связей под контролем света на двух разных длинах волн». Angewandte Chemie International Edition. 58 (22): 7470–7474. Дои:10.1002 / anie.201901275. PMID 30916368.
- ^ Рамиль, Карло П.; Линь, Цин (август 2014 г.). "Фотокликовая химия: флуорогенный световой in vivo реакция лигирования ". Современное мнение в области химической биологии. 21: 89–95. Дои:10.1016 / j.cbpa.2014.05.024. ЧВК 4149939. PMID 25022432.
- ^ Деварадж, Нил К .; Вайследер, Ральф; Хильдербранд, Скотт А. (декабрь 2008 г.). «Циклоприсоединения на основе тетразина: применение для предварительной визуализации живых клеток». Биоконъюгат Chem. 19 (12): 2297–2299. Дои:10.1021 / bc8004446. ЧВК 2677645. PMID 19053305.
- ^ Ding, H .; Демпл, Б. (2000). «Прямая передача сигнала оксида азота через нитрозилирование центров железо-сера в активаторе транскрипции SoxR». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 97 (10): 5146–5150. Bibcode:2000PNAS ... 97.5146D. Дои:10.1073 / пнас.97.10.5146. ЧВК 25796. PMID 10805777.
- ^ Дитрих; и другие. (2007). «Маркировка, обнаружение и идентификация вновь синтезированных протеомов с биоортогональной неканонической аминокислотной маркировкой». Протоколы природы. 2 (3): 532–540. Дои:10.1038 / nprot.2007.52. PMID 17406607.
- ^ Ю; и другие. (2012). «Генетически закодированный циклопропен направляет быстрое мечение белков, опосредованное фотохимическим анализом, в клетках млекопитающих». Angew Chem Int Ed Engl. 51 (42): 10600–10604. Дои:10.1002 / anie.201205352. ЧВК 3517012. PMID 22997015.
- ^ (а) Liang, G .; Ren, H .; Рао, J. Nat. Chem. 2010, 2, 54. (b) Ren, H .; Xiao, F .; Жан, К .; Kim, Y.-P .; Xie, H .; Xia, Z .; Rao, J. Angew.Chem., Int. Эд. 2009, 48, 9658.
- ^ Илья А. Остерман; Алексей В. Устинов; Денис В. Евдокимов; Коршун Владимир Александрович; Петр В. Сергиев; Марина Владимировна Серебрякова; Ирина А. Демина; Мария Анатольевна Галямина; Вадим М. Говорун; Ольга Анатольевна Донцова (январь 2013 г.). «Новое исследование протеома, сочетающее химию щелчков и 2DE» (PDF). Протеомика. 13 (1): 17–21. Дои:10.1002 / pmic.201200393. PMID 23161590. Архивировано из оригинал (PDF) на 2015-06-30. Получено 2015-02-11.
- ^ Кокс, Кортни Л .; Тиц, Джонатан I .; Соколовский, Кароль; Мелби, Джоэл О .; Дорогази, Джеймс Р .; Митчелл, Дуглас А. (17 июня 2014 г.). «Нуклеофильные 1,4-добавки для открытия природных продуктов». ACS Химическая биология. 9 (9): 2014–2022. Дои:10.1021 / cb500324n. ЧВК 4168802. PMID 24937678.
- ^ Майкл Флорос; Алсидес Леао; Суреш Наринэ (2014). "Растворитель на основе растительного масла и без катализатора" Click Chemistry "Термопластичные политриазолы". BioMed Research International. 2014: 1–14. Дои:10.1155/2014/792901. ЧВК 4085725. PMID 25032224.
- ^ Лондон, Габор; Чен, Куанг-Янь; Кэрролл, Грегори Т .; Феринга, Бен Л. (2013). «На пути к динамическому контролю смачиваемости с помощью функциональных высотных молекулярных двигателей на твердых поверхностях». Химия: европейский журнал. 19 (32): 10690–10697. Дои:10.1002 / chem.201300500. PMID 23784916.
- ^ Джон Э. Моисей; Адам Д. Мурхаус (2007). «Растущее применение щелочной химии». Chem. Soc. Ред. 36 (8): 1249–1262. Дои:10.1039 / b613014n. PMID 17619685.
- ^ Жан-Франсуа Лутц; Зоя Зарафшани (2008). «Эффективное конструирование терапевтических средств, биоконъюгатов, биоматериалов и биоактивных поверхностей с использованием азид-алкиновой химии». Расширенные обзоры доставки лекарств. 60 (9): 958–970. Дои:10.1016 / j.addr.2008.02.004. PMID 18406491.
- ^ «Архивная копия». Архивировано из оригинал на 2012-05-15. Получено 2012-06-05.CS1 maint: заархивированная копия как заголовок (связь)
- ^ «Архивная копия». Архивировано из оригинал на 2012-12-17. Получено 2012-06-05.CS1 maint: заархивированная копия как заголовок (связь)
- ^ "Xconomy: Allozyne Licenses Scripps Chemistry". 2010-07-15.
- ^ «Экономика: сделка с чернилами Элерона и Скриппса». 2010-11-30.
- ^ «Архивная копия». Архивировано из оригинал на 2012-04-30. Получено 2012-06-05.CS1 maint: заархивированная копия как заголовок (связь)
- ^ «Химия | Определение в науке». Получено 2020-08-29.
- ^ http://www.chromeon.com/
внешняя ссылка
- Щелкните "Химия: краткий обзор и недавняя литература"
- Национальный научный фонд: статья «В жизнь с Click Chemistry».
- Новости химии и техники: статья «Химия в режиме реального времени».
- Новости химии и машиностроения: статья "Щелочная химия без меди"
- Обзор безметалловой химии
- Щелкните Химия - а Chem Soc Rev тематический выпуск о последних приложениях клик-химии под редакцией М. Г. Финна и Валерия Фокина. Опубликовано Королевское химическое общество