WikiDer > Сетчатка
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК (2E,4E,6E,8E) -3,7-Диметил-9- (2,6,6-триметилциклогексен-1-ил) нона-2,4,6,8-тетраеналь | |
Другие имена
| |
| Идентификаторы | |
3D модель (JSmol) | |
| ChemSpider | |
| ECHA InfoCard | 100.003.760 |
PubChem CID | |
| UNII | |
| |
| |
| Свойства | |
| C20ЧАС28О | |
| Молярная масса | 284.443 г · моль−1 |
| Внешность | Оранжевые кристаллы из петролейный эфир[1] |
| Температура плавления | От 61 до 64 ° C (от 142 до 147 ° F, от 334 до 337 K)[1] |
| Почти не растворим | |
| Растворимость в жире | Растворимый |
| Родственные соединения | |
Родственные соединения | ретинол; ретиноевая кислота; бета-каротин; дегидроретинальный; 3-гидроксиретинал; 4-гидроксиретинал |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Сетчатка (также известен как ретинальдегид) это полиен хромофор, связанный с белками, называемыми опсины, и является химической основой зрения животных.
Сетчатка позволяет определенным микроорганизмам преобразовывать свет в метаболическую энергию.
Есть много форм витамин А - все они превращаются в сетчатку, что невозможно без них. Сам по себе сетчатка считается формой витамина А при употреблении в пищу животными. Количество различных молекул, которые могут быть преобразованы в сетчатку, варьируется от вида к виду. Ретинал изначально назывался ретинен,[2] и переименовал[3] после того, как было обнаружено, что это витамин А альдегид.[4][5]
Позвоночные животные глотают сетчатку непосредственно из мяса или продуцируют сетчатку из каротиноиды - либо из α-каротин или β-каротин - оба из которых каротины. Они также производят его из β-криптоксантин, тип ксантофилл. Эти каротиноиды должны быть получены из растений или других фотосинтетический организмы. Никакие другие каротиноиды не могут быть преобразованы животными в сетчатку. Некоторые плотоядные животные вообще не могут преобразовывать каротиноиды. Другие основные формы витамина А - ретинол и частично активная форма, ретиноевая кислота - оба могут быть произведены из сетчатки.
Беспозвоночные, такие как насекомые и кальмары, используют гидроксилированные формы сетчатки в своих зрительных системах, которые возникают в результате преобразования из других ксантофиллы.
Метаболизм витамина А
Живые организмы продуцируют сетчатку (RAL) путем необратимого окислительного расщепления каротиноидов.[6]Например:
- бета-каротин + O2 → 2 сетчатки
катализируется бета-каротин 15,15'-монооксигеназа[7]или бета-каротин 15,15'-диоксигеназа.[8]Подобно тому, как каротиноиды являются предшественниками сетчатки, сетчатка является предшественником других форм витамина А. Ретиналь является взаимопревращаемым веществом. ретинол (ROL), транспортная форма и форма хранения витамина А:
катализируется ретинолдегидрогеназы (RDH)[9] и алкогольдегидрогеназы (ADH).[10]Ретинол называют витамином А алкоголь или, чаще, просто витамин А. Сетчатка также может окисляться до ретиноевая кислота (РА):
- сетчатка + НАД+ + H2О → ретиноевая кислота + НАДН + Н+ (катализируется RALDH)
- сетчатка + O2 + H2O → ретиноевая кислота + H2О2 (катализируется ретинальной оксидазой)
катализируется дегидрогеназы сетчатки[11] также известные как дегидрогеназа ретинальдегида (RALDH)[10]а также оксидазы сетчатки.[12]Ретиноевая кислота, иногда называемая витамином А кислота, является важной сигнальной молекулой и гормоном у позвоночных животных.
Видение
Сетчатка - это конъюгированный хромофор. в человеческий глаз, сетчатка начинается в 11-СНГ-ретинальная конфигурация, которая - при захвате фотон правильной длины волны - выпрямляется во все-транс-ретинальная конфигурация. Это изменение конфигурации отталкивает белок опсин в сетчатка, который запускает каскад химических сигналов, который может привести к восприятие света или изображений человеческого мозга. Спектр поглощения хромофора зависит от его взаимодействия с белком опсина, с которым он связан, так что разные комплексы ретиналь-опсин будут поглощать фотоны с разной длиной волны (то есть с разными цветами света).
Опсины

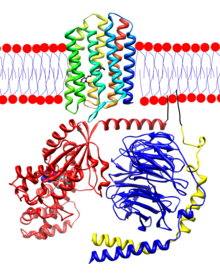
Опсины белки и связывающие сетчатку зрительные пигменты, обнаруженные в фоторецепторные клетки в сетчатка глаз. Опсин состоит из семи трансмембранных альфа-спирали связаны шестью петлями. В стержневые клеткимолекулы опсина встроены в мембраны дисков, которые полностью находятся внутри клетки. В N-конец Голова молекулы простирается внутрь диска, а C-конец хвост заходит в цитоплазму клетки. В конических ячейках диски определяются размером ячейки. плазматическая мембрана, так что N-концевая головка выходит за пределы ячейки. Сетчатка ковалентно связывается с лизин на трансмембранной спирали, ближайшей к С-концу белка через База Шиффа связь. Образование связи основания Шиффа включает удаление атома кислорода из сетчатки и двух атомов водорода из свободной аминогруппы лизина, что дает H2О. Ретинилиден - это двухвалентная группа, образованная удалением атома кислорода из сетчатки, поэтому опсины были названы ретинилиденовые белки.
Опсины являются прототипами G-белковые рецепторы (GPCR).[13] Родопсин крупного рогатого скота, опсин палочек крупного рогатого скота, был первым GPCR, имеющим свой Рентгеновская структура определяется.[14]Бычий родопсин содержит 348 аминокислотных остатков. Хромофор сетчатки связывается с Lys296.
Хотя млекопитающие используют сетчатку исключительно в качестве хромофора опсина, другие группы животных дополнительно используют четыре хромофора, тесно связанные с сетчаткой: 3,4-дидегидроретиналь (витамин А2), (3р) -3-гидроксиретинал, (3S) -3-гидроксиретиналь (оба витамина А3) и (4р) -4-гидроксиретиналь (витамин А4). Многие рыбы и амфибии используют 3,4-дидегидроретинал, также называемый дегидроретинальный. За исключением двукрылое животное подотряд Циклоррафа (так называемые высшие мухи), все насекомые исследовано использовать (р)-энантиомер 3-гидроксиретиналя. (р) -энантиомер следует ожидать, если 3-гидроксиретиналь получают непосредственно из ксантофилл каротиноиды. Циклоррафаны, в том числе Дрозофила, используйте (3S) -3-гидроксиретинал.[15][16]Светлячок-кальмар были найдены для использования (4р) -4-гидроксиретинал.
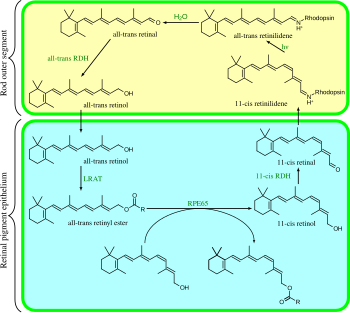
Визуальный цикл
Визуальный цикл представляет собой круговой ферментативный путь, который является передним концом фототрансдукции. Восстанавливает 11-СНГ-ретинальный. Например, зрительный цикл стержневых клеток млекопитающих выглядит следующим образом:
- все-транс-ретиниловый эфир + H2О → 11-СНГ-ретинол + жирная кислота; RPE65 изомерогидролазы,[17]
- 11-СНГ-ретинол + НАД+ → 11-СНГ-ретинал + НАДН + Н+; 11-СНГ-ретинолдегидрогеназы,
- 11-СНГ-ретинальный + апородопсин → родопсин + H2О; формы База Шиффа связь с лизин, -CH = N+ЧАС-,
- родопсин + hν → метародопсин II, т.е. 11-СНГ фотоизомеризуется все-транс,
- родопсин + hν → фотородопсин → батородопсин → люмиродопсин → метародопсин I → метародопсин II,
- метародопсин II + H2О → апородопсин + все-транс-ретинальный,
- все-транс-ретинальный + НАДФН + Н+ → все-транс-ретинол + НАДФ+; все-транс-ретинол дегидрогеназы,
- все-транс-ретинол + жирная кислота → все-транс-ретиниловый эфир + H2О; лецитин ретинол ацилтрансферазы (LRAT).[18]
Шаги 3, 4, 5 и 6 выполняются в внешние сегменты стержневой ячейки; Шаги 1, 2 и 7 выполняются в пигментный эпителий сетчатки (RPE) клетки.
Изомерогидролазы RPE65 являются гомологичный с бета-каротинмонооксигеназами;[6] гомологичный фермент ninaB в Дрозофила обладает как каротиноид-оксигеназной активностью, формирующей сетчатку, так и полностьютранс к 11-СНГ изомеразная активность.[19]
Микробные родопсины
Все-транс-ретинал также является важным компонентом микробных опсинов, таких как бактериородопсин, канал родопсин, и галородопсин. В этих молекулах свет вызывает всетранс-ретинал станет 13-СНГ сетчатка, которая затем возвращается ко всем -транс-ретинал в темном состоянии. Эти белки не связаны эволюционно с опсинами животных и не являются GPCR; тот факт, что они оба используют сетчатку, является результатом конвергентная эволюция.[20]
История
Американский биохимик Джордж Уолд и другие наметили визуальный цикл к 1958 году. За свою работу Уолд получил долю конкурса 1967 года. Нобелевская премия по физиологии и медицине с участием Халдан Кеффер Хартлайн и Рагнар Гранит.[21]
Смотрите также
использованная литература
- ^ а б Индекс Merck, 13-е издание, 8249
- ^ УОЛД, ДЖОРДЖ (14 июля 1934 г.). «Каротиноиды и цикл витамина А в зрении». Природа. 134 (3376): 65. Bibcode:1934 Натур.134 ... 65 Вт. Дои:10.1038 / 134065a0. S2CID 4022911.
- ^ Вальд, G (11 октября 1968 г.). «Молекулярные основы зрительного возбуждения». Наука. 162 (3850): 230–9. Bibcode:1968Sci ... 162..230Вт. Дои:10.1126 / science.162.3850.230. PMID 4877437.
- ^ MORTON, R.A .; ГУДВИН, Т. У. (1 апреля 1944 г.). «Приготовление ретинена in vitro». Природа. 153 (3883): 405–406. Bibcode:1944Натура.153..405М. Дои:10.1038 / 153405a0. S2CID 4111460.
- ^ МЯЧИ; GOODWIN, TW; МОРТОН, Р.А. (1946). «Ретинен-1-витаминный альдегид». Биохимический журнал. 40 (5–6): lix. PMID 20341217.
- ^ а б фон Линтиг, Йоханнес; Фогт, Клаус (2000). «Заполнение пробела в исследованиях витамина А: молекулярная идентификация фермента, отщепляющего бета-каротин до сетчатки». Журнал биологической химии. 275 (16): 11915–11920. Дои:10.1074 / jbc.275.16.11915. PMID 10766819.
- ^ Воггон, Вольф-Д. (2002). «Окислительное расщепление каротиноидов, катализируемое моделями ферментов и бета-каротин 15,15´-монооксигеназой». Чистая и прикладная химия. 74 (8): 1397–1408. Дои:10.1351 / pac200274081397.
- ^ Ким, Ён Су; Ким, Нам-Хи; Йом, Су-Джин; Ким, Сон-Вон; О, Док-Кун (2009). «In vitro характеристика рекомбинантного белка Blh из некультивируемых морских бактерий как β-каротин 15,15'-диоксигеназа». Журнал биологической химии. 284 (23): 15781–93. Дои:10.1074 / jbc.M109.002618. ЧВК 2708875. PMID 19366683.
- ^ Лиден, Мартин; Эрикссон, Ульф (2006). «Понимание метаболизма ретинола: структура и функция ретинолдегидрогеназ». Журнал биологической химии. 281 (19): 13001–13004. Дои:10.1074 / jbc.R500027200. PMID 16428379.
- ^ а б Дестер, Дж. (Сентябрь 2008 г.). «Синтез ретиноевой кислоты и передача сигналов во время раннего органогенеза». Ячейка. 134 (6): 921–31. Дои:10.1016 / j.cell.2008.09.002. ЧВК 2632951. PMID 18805086.
- ^ Линь, Мин; Чжан, Мин; Авраам, Михаил; Смит, Сьюзен М .; Неаполь, Джозеф Л. (2003). «Дегидрогеназа сетчатки 4 мыши (RALDH4), молекулярное клонирование, клеточная экспрессия и активность в биосинтезе 9-цис-ретиноевой кислоты в интактных клетках». Журнал биологической химии. 278 (11): 9856–9861. Дои:10.1074 / jbc.M211417200. PMID 12519776.
- ^ «KEGG ENZYME: 1.2.3.11 оксидаза сетчатки». Получено 2009-03-10.
- ^ Лэмб, Т. Д. (1996). «Усиление и кинетика активации в каскаде фототрансдукции G-белков». Труды Национальной академии наук. 93 (2): 566–570. Bibcode:1996ПНАС ... 93..566Л. Дои:10.1073 / пнас.93.2.566. ЧВК 40092. PMID 8570596.
- ^ Пальчевский, Кшиштоф; Кумасака, Такаши; Хори, Т; Бенке, Калифорния; Motoshima, H; Фокс, BA; Ле Тронг, я; Teller, DC; и другие. (2000). «Кристаллическая структура родопсина: рецептор, связанный с G-белком». Наука. 289 (5480): 739–745. Bibcode:2000Sci ... 289..739P. CiteSeerX 10.1.1.1012.2275. Дои:10.1126 / science.289.5480.739. PMID 10926528.
- ^ Секи, Такахару; Исоно, Кунио; Ито, Масаёши; Кацута, Юко (1994). «Мухи в группе Cyclorrhapha используют (3S) -3-Hydroxyretinal в качестве уникального хромофора визуального пигмента». Европейский журнал биохимии. 226 (2): 691–696. Дои:10.1111 / j.1432-1033.1994.tb20097.x. PMID 8001586.
- ^ Секи, Такахару; Исоно, Кунио; Одзаки, Каору; Цукахара, Ясуо; Шибата-Кацута, Юко; Ито, Масаёши; Ирие, Тошиаки; Катагири, Масанао (1998). «Метаболический путь образования хромофора зрительного пигмента у Drosophila melanogaster: All-trans (3S) -3-hydroxyretinal формируется из полностью транс-ретиналя через (3R) -3-hydroxyretinal в темноте». Европейский журнал биохимии. 257 (2): 522–527. Дои:10.1046 / j.1432-1327.1998.2570522.x. PMID 9826202.
- ^ Моисеев, Геннадий; Чен, Инь; Такахаши, Юске; Ву, Билл Х .; Ма, Цзянь-син (2005). «RPE65 - изомерогидролаза в зрительном цикле ретиноидов». Труды Национальной академии наук. 102 (35): 12413–12418. Bibcode:2005ПНАС..10212413М. Дои:10.1073 / pnas.0503460102. ЧВК 1194921. PMID 16116091.
- ^ Цзинь, Минхао; Юань, Цюань; Ли, Сунхуа; Трэвис, Габриэль Х. (2007). «Роль LRAT на активность ретиноид-изомеразы и мембранную ассоциацию Rpe65». Журнал биологической химии. 282 (29): 20915–20924. Дои:10.1074 / jbc.M701432200. ЧВК 2747659. PMID 17504753.
- ^ Оберхаузер, Витус; Вулстра, Олаф; Бангерт, Аннетт; фон Линтиг, Йоханнес; Фогт, Клаус (2008). «NinaB сочетает в себе активность каротиноидной оксигеназы и ретиноид-изомеразы в одном полипептиде». Труды Национальной академии наук. 105 (48): 19000–5. Bibcode:2008PNAS..10519000O. Дои:10.1073 / pnas.0807805105. ЧВК 2596218. PMID 19020100.
- ^ Чен, Де-Лян; Ван, Гуан-ю; Сюй, Бинг; Ху, Кунь-Шэн (2002). «Изомеризация сетчатки полностью из транс в 13 цис в адаптированном к свету бактериородопсине при кислом pH». Журнал фотохимии и фотобиологии B: Биология. 66 (3): 188–194. Дои:10.1016 / S1011-1344 (02) 00245-2. PMID 11960728.
- ^ Нобелевская премия 1967 года по медицине
дальнейшее чтение
- Прадо-Кабреро, Альфонсо; Шерзингер, Дэниел; Авалос, Хавьер; Аль-Бабили, Салим (2007). «Биосинтез сетчатки в грибах: характеристика каротиноидной оксигеназы CarX из Fusarium fujikuroi». Эукариотическая клетка. 6 (4): 650–657. Дои:10.1128 / EC.00392-06. ЧВК 1865656. PMID 17293483.
- Kloer, Daniel P .; Рух, Сандра; Аль-Бабили, Салим; Бейер, Питер; Шульц, Георг Э. (2005). «Структура каротиноидной оксигеназы, формирующей сетчатку». Наука. 308 (5719): 267–269. Bibcode:2005Наука ... 308..267K. Дои:10.1126 / science.1108965. PMID 15821095. S2CID 6318853.
- Шмидт, Хольгер; Курцер, Роберт; Айзенрайх, Вольфганг; Шваб, Вильфрид (2006). «Каротеназа AtCCD1 из Arabidopsis thaliana является диоксигеназой». Журнал биологической химии. 281 (15): 9845–9851. Дои:10.1074 / jbc.M511668200. PMID 16459333.
- Ван, Дао; Цзяо, Ючэнь; Монтелл, Крейг (2007). «Рассечение пути, необходимого для производства витамина А и фототрансдукции дрозофилы». Журнал клеточной биологии. 177 (2): 305–316. Дои:10.1083 / jcb.200610081. ЧВК 2064138. PMID 17452532.
- Уолд, Джордж (1967). «Нобелевская лекция: Молекулярные основы визуального возбуждения» (PDF). Получено 2009-02-23.
- Фернальд, Рассел Д. (2006). «Проливая генетический свет на эволюцию глаз». Наука. 313 (5795): 1914–1918. Bibcode:2006Научный ... 313.1914F. Дои:10.1126 / science.1127889. PMID 17008522. S2CID 84439732.
- Briggs, Winslow R .; Спудич, Джон Л., ред. (2005). Справочник по фотосенсорным рецепторам. Вайли. ISBN 978-3-527-31019-7.
- Бейлор, Д. А.; Lamb, T D; Яу, К. В. (1979). «Реакция палочек сетчатки на одиночные фотоны». Журнал физиологии. 288: 613–634. Дои:10.1113 / jphysiol.1979.sp012716 (неактивно 01.09.2020). ЧВК 1281447. PMID 112243.CS1 maint: DOI неактивен по состоянию на сентябрь 2020 г. (ссылка на сайт)
- Гехт, Селиг; Шлаер, Саймон; Пиренн, Морис Анри (1942). "Энергия, кванта и видение". Журнал общей физиологии. 25 (6): 819–840. Дои:10.1085 / jgp.25.6.819. ЧВК 2142545. PMID 19873316.
- Barlow, H.B .; Levick, W.R .; Юн, М. (1971). «Ответы на одиночные кванты света в ганглиозных клетках сетчатки кошки». Исследование зрения. 11 (Приложение 3): 87–101. Дои:10.1016/0042-6989(71)90033-2. PMID 5293890.
- Вентер, Дж. Крейг; Ремингтон, К; Гейдельберг, JF; Halpern, AL; Rusch, D; Eisen, JA; Ву, Д; Паульсен, я; и другие. (2004). «Экологическое секвенирование генома из дробовика Саргассова моря». Наука. 304 (5667): 66–74. Bibcode:2004Наука ... 304 ... 66V. CiteSeerX 10.1.1.124.1840. Дои:10.1126 / science.1093857. PMID 15001713. S2CID 1454587. Океаны полны родопсина 1 типа.
- Ващук, Стивен А .; Безерра, Аранди Дж .; Ши, Личи; Браун, Леонид С. (2005). «Leptosphaeria rhodopsin: Бактериородопсиноподобный протонный насос эукариот». Труды Национальной академии наук. 102 (19): 6879–6883. Bibcode:2005PNAS..102.6879W. Дои:10.1073 / pnas.0409659102. ЧВК 1100770. PMID 15860584.
- Су, Чжи-Инь; Ло, Дун-Ген; Теракита, Акихиса; Шичида, Йошинори; Ляо, Си-Вэнь; Kazmi, Manija A .; Sakmar, Thomas P .; Яу, Кинг-Вай (2006). «Компоненты фототрансдукции теменного глаза и их потенциальные эволюционные последствия». Наука. 311 (5767): 1617–1621. Bibcode:2006Научный ... 311.1617S. Дои:10.1126 / science.1123802. PMID 16543463. S2CID 28604455.
- Ло, Дун-Ген; Сюэ, Тянь; Яу, Кинг-Вай (2008). «Как начинается видение: Одиссея». Труды Национальной академии наук. 105 (29): 9855–9862. Bibcode:2008ПНАС..105.9855Л. Дои:10.1073 / pnas.0708405105. ЧВК 2481352. PMID 18632568. Хороший исторический обзор.
- Шефер, Гюнтер; Энгельхард, Мартин; Мюллер, Фолькер (1999). «Биоэнергетика архей». Обзоры микробиологии и молекулярной биологии. 63 (3): 570–620. Дои:10.1128 / MMBR.63.3.570-620.1999. ЧВК 103747. PMID 10477309.
- Fan, Jie; Вудрафф, Майкл Л; Cilluffo, Marianne C; Крауч, Розали К.; Файн, Гордон L (2005). «Активация трансдукции опсином в палочках темнокожих мышей с нокаутом Rpe65». Журнал физиологии. 568 (1): 83–95. Дои:10.1113 / jphysiol.2005.091942. ЧВК 1474752. PMID 15994181.
- Садекар, Сумедха; Раймонд, Джейсон; Бланкеншип, Роберт Э. (2006). «Сохранение отдаленно связанных мембранных белков: центры фотосинтетической реакции имеют общее структурное ядро». Молекулярная биология и эволюция. 23 (11): 2001–2007. Дои:10.1093 / molbev / msl079. PMID 16887904.
- Ёкояма, сёдзо; Радлвиммер, Ф. Бернхард (2001). «Молекулярная генетика и эволюция красного и зеленого цветового зрения у позвоночных». Генетика. 158 (4): 1697–1710. ЧВК 1461741. PMID 11545071.
- Рэкер, Эфраим; Стоекениус, Вальтер (1974). «Восстановление пурпурных мембранных пузырьков, катализирующих поглощение протонов под действием света и образование аденозинтрифосфата». Журнал биологической химии. 249 (2): 662–663. PMID 4272126.
- Кавагути, Рики; Ю, Цзямей; Хонда, Джейн; Ху, Джейн; Уайтлегдж, Джулиан; Пинг, Пейпей; Виита, Патрик; Бок, декан; Солнце, Хуэй (2007). «Мембранный рецептор ретинол-связывающего белка опосредует клеточное поглощение витамина А». Наука. 315 (5813): 820–825. Bibcode:2007Наука ... 315..820K. Дои:10.1126 / science.1136244. PMID 17255476. S2CID 25258551.
- Amora, Tabitha L .; Ramos, Lavoisier S .; Галан, Дженни Ф .; Бирдж, Роберт Р. (2008). «Спектральная настройка пигментов темно-красного конуса». Биохимия. 47 (16): 4614–20. Дои:10.1021 / bi702069d. ЧВК 2492582. PMID 18370404.
- Пошли, Роберт; Сандхольм, Дейдж (2007). «Лестница к коническому пересечению: компьютерное исследование изомеризации сетчатки». Журнал физической химии А. 111 (36): 8766–8773. Bibcode:2007JPCA..111.8766S. Дои:10.1021 / jp073908l. PMID 17713894.
- Салом, Давид; Лодовски, Дэвид Т .; Стенкамп, Рональд Э .; Ле Тронг, Изольда; Гольчак, Марцин; Ястшебская, Беата; Харрис, Тим; Ballesteros, Juan A .; Пальчевский, Кшиштоф (2006). «Кристаллическая структура фотоактивированного депротонированного промежуточного соединения родопсина». Труды Национальной академии наук. 103 (44): 16123–16128. Bibcode:2006ПНАС..10316123С. Дои:10.1073 / pnas.0608022103. ЧВК 1637547. PMID 17060607.
внешние ссылки
- Первые шаги видения - Национальный музей здоровья
- Зрение и молекулярные изменения, вызванные светом
- Анатомия сетчатки и зрительные способности
- Сетчатка