WikiDer > Кардиомиопатия после родов
| Кардиомиопатия после родов | |
|---|---|
| Другие имена | Послеродовая кардиомиопатия[1] |
| Специальность | Акушерство, кардиология |
Перипартальная кардиомиопатия (ППКМ) это форма дилатационная кардиомиопатия что определяется как ухудшение сердечной функции, обычно проявляющееся между последним месяцем беременность и до полугода послеродовой. Как и в случае других форм дилатационной кардиомиопатии, PPCM включает систолическую дисфункцию сердца с уменьшением фракция выброса левого желудочка (EF) с ассоциированным хроническая сердечная недостаточность и повышенный риск предсердный и желудочковый аритмии, тромбоэмболия (закупорка кровеносного сосуда сгустком крови) и даже внезапная сердечная смерть. По сути, сердечная мышца не может сокращаться с достаточной силой, чтобы перекачивать достаточное количество крови для нужд жизненно важных органов тела.[2][3][4][5][6]
PPCM - это диагноз исключения, при котором пациенты не имеют в анамнезе сердечных заболеваний и нет других известных возможных причин сердечной недостаточности. Эхокардиограмма используется как для диагностики, так и для мониторинга эффективности лечения PPCM.[2][3][4][5][6]
Причина PPCM неизвестна. В настоящее время исследователи исследуют кардиотропные вирусы, аутоиммунитет или же иммунная система дисфункция, другие токсины, которые служат триггерами дисфункции иммунной системы, микронутриент или дефицит микроэлементов, а также генетика как возможные компоненты, которые способствуют или вызывают развитие PPCM.[2][4][7]
Процесс PPCM начинается с неизвестного триггера (возможно, кардиотропного вируса или другого еще неустановленного катализатора), который запускает воспалительный процесс в сердце. Следовательно, клетки сердечной мышцы повреждаются; некоторые умирают или превращаются в рубцовую ткань. Рубцовая ткань не способна сокращаться; следовательно, эффективность насосного действия сердца снижается. Кроме того, повреждение цитоскелетного каркаса сердца приводит к увеличению, растяжению или изменению формы сердца, что также снижает систолическую функцию или объем сердечной деятельности. Первоначальный воспалительный процесс, по-видимому, вызывает аутоиммунный или иммунный дисфункциональный процесс, который, в свою очередь, подпитывает начальный воспалительный процесс. Прогрессирующая потеря клеток сердечной мышцы приводит в конечном итоге к сердечной недостаточности.[8]
Признаки и симптомы
Симптомы обычно включают одно или несколько из следующих: ортопноэ (затрудненное дыхание в горизонтальном положении), одышка (одышка) при физической нагрузке, точечная коррозия отек (отек), кашель, частое мочеиспускание в ночное время, чрезмерное увеличение веса в течение последнего месяца беременности (1-2 + кг в неделю; от двух до четырех или более фунтов в неделю), сердцебиение (ощущение учащенного сердцебиения, пропуск ударов, длительных пауз между ударами или трепетание) и боль в груди.[2][4]
Одышка часто описывается пациентами PPCM как неспособность сделать глубокий или полный вдох или получить достаточное количество воздуха в легкие. Кроме того, пациенты часто описывают необходимость подкрепиться на ночь с помощью двух или более подушек, чтобы лучше дышать. Эти симптомы, отек и / или кашель могут указывать на отек легких (жидкость в легких) в результате острой сердечной недостаточности и ППКМ.
Диагноз может быть отложен или отклонен, поскольку ранние симптомы могут быть интерпретированы как типичные для нормальной беременности. Задержки в диагностике и лечении PPCM связаны с увеличением заболеваемости и смертности.[2][4][5][6][9][10]
Также довольно часто женщины предъявляют доказательства наличия эмбол (сгусток), переходящий от сердца к жизненно важному органу, вызывая такие осложнения, как Инсультпотеря кровообращения в конечности, даже Коронарная артерия окклюзия (закупорка) с типичной инфаркт миокарда (острое сердечно-сосудистое заболевание).[11]
По этим причинам крайне важно, чтобы клиницисты сильно подозревали ППКМ у любого пациента в пери- или послеродовом периоде, у которого возникают необычные или необъяснимые симптомы или проявления.[2][4][8][12][11]
Диагностика
Следующий инструмент скрининга может быть полезен пациентам и медицинским работникам при определении необходимости принятия дальнейших мер для диагностики симптомов:[13]
| Специализированный анамнез для скрининга PPCM для выявления ранних симптомов сердечной недостаточности в течение последнего месяца беременности: |
|---|
| 1. Ортопноэ (затрудненное дыхание в горизонтальном положении): |
| а.) Нет = 0 баллов; б.) Необходимость поднять голову = 1 балл; c.) Необходимо поднять верхнюю часть тела на 45 ° или более = 2 балла. |
| 2. Одышка (одышка) при физической нагрузке: |
| а.) Нет = 0 баллов; б.) Восхождение на 8 и более ступеней = 1 балл; в.) Ходьба по уровню = 2 балла |
| 3. Необъяснимый кашель: |
| а.) Нет = 0 баллов; б.) Ночное время = 1 балл; в.) День и ночь = 2 балла |
| 4. Отеки (точечные отеки) нижних конечностей: |
| а.) Нет = 0 баллов; б.) Ниже колена = 1 балл; c.) Выше и ниже колена и / или рук / лица = 2 балла. |
| 5. Чрезмерное увеличение веса на последнем месяце беременности: |
| а.) Менее 2 фунтов в неделю = 0 баллов; б.) от 2 до 4 фунтов в неделю = 1 балл; c.) более 4 фунтов в неделю = 2 балла. |
| 6. Сердцебиение (ощущение нерегулярных сердечных сокращений): |
| а.) Нет = 0 баллов; б) в положении лежа ночью = 1 балл; в.) День и ночь, любая позиция = 2 балла |
| Подсчет очков и действие: |
| 0 - 2 = низкий риск - продолжить наблюдение |
| 3–4 = умеренный риск - рассмотрите возможность проведения BNP и CRP в крови; эхокардиограмма, если BNP и CRP повышены |
| 5 или более = высокий риск - сделайте BNP, CRP в крови и эхокардиограмму |
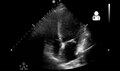
УЗИ
УЗИ послеродовой кардиомиопатии[14]
УЗИ послеродовой кардиомиопатии[14]
УЗИ послеродовой кардиомиопатии[14]
Уход
Раннее выявление и лечение связаны с более высокими показателями выздоровления и снижением заболеваемости и смертности.[2][4][5][6][9][10]
Лечение PPCM аналогично лечению застойной сердечной недостаточности. Обычное лечение сердечной недостаточности включает использование диуретиков, бета-блокаторов (B-B) и ингибиторов ангиотензинпревращающего фермента (ACE-I) после родов. Диуретики, желательно фуросемид, помогают организму избавиться от лишнего веса воды, а также снизить кровяное давление. ACE-I и B-B улучшают кровообращение и способствуют устранению дисфункции иммунной системы, связанной с PPCM. Если АПФ плохо переносится пациентом, его можно заменить блокаторами рецепторов ангиотензина (БРА). Гидралазин с нитратами может заменить ACE-I в кормление грудью матери или до родов; однако данные свидетельствуют о том, что этот курс лечения может быть не таким эффективным, как ACE-I, но полезен при необходимости.[2][4][5][6][8][10][15]
Если EF меньше 35%, антикоагулянт показан, так как существует больший риск развития тромбов левого желудочка (сгустков крови). Иногда имплантация вспомогательное устройство левого желудочка (LVAD) или даже пересадка сердца тоже становится необходимым.[2][5][6][8][16]
Важно, чтобы пациент получал регулярное последующее наблюдение, включая частые эхокардиограммы, чтобы контролировать улучшение или его отсутствие, особенно после изменения режима лечения.
Пациенты, которые не отвечают на начальное лечение, определяемое как ФВ левого желудочка, остающаяся ниже 20% через два месяца или ниже 40% через три месяца при традиционном лечении, могут потребовать дальнейшего исследования, в том числе кардиологического. магнитно-резонансная томография (МРТ), катетеризация сердца, а также эндомиокардиальная биопсия для специального окрашивания и вирусной полимеразной цепной реакции (ПЦР) анализ. Противовирусная терапия, иммуноабсорбция, внутривенное введение гамма-глобулин, или другая иммуномодулирующая терапия может быть рассмотрена соответственно, но в соответствии с протоколом контролируемого типа исследования.[8]
Поскольку никто точно не знает, когда следует прекратить лечение, даже если выздоровление наступает быстро, рекомендуется продолжать прием АПФ-I и B-B в течение как минимум одного года после постановки диагноза.[4]
Пациенты с ППКМ имеют повышенный риск внезапной смерти, и видно, что они получают пользу от имплантируемого кардиовертера-дефибриллятора (ИКД) и сердечной ресинхронизирующей терапии для предотвращения внезапной сердечной смерти. Однако ввиду обратимой кардиомиопатии иногда Имплантируемый кардиовертер-дефибриллятор (ICD) или Сердечная ресинхронизирующая терапия (CRT) обычно не используются и предназначены для лечения тяжелой дисфункции ЛЖ или случаев высокого риска.[17]
Прогноз
Самые последние исследования показывают, что при использовании более новых традиционных методов лечения сердечной недостаточности, мочегонные средства, Ингибиторы АПФ и бета-блокаторы, выживаемость очень высока - 98% или выше, и почти у всех пациентов с ППКМ улучшается состояние при лечении.[15][18][19] В США более 50% пациентов с ППКМ испытывают полное восстановление функции сердца (ФВ 55% или выше).[5][8] Почти все выздоровевшие пациенты в конечном итоге могут прекратить прием лекарств без рецидива и имеют нормальную продолжительность жизни.[18]
Ошибочно считать, что надежда на выздоровление зависит от улучшения или выздоровления в течение первых шести-12 месяцев после постановки диагноза. Многие женщины продолжают поправляться или выздоравливать даже спустя годы после постановки диагноза при продолжении лечения.[4][20] После полного выздоровления и отсутствия последующей беременности вероятность рецидива сердечной недостаточности минимальна.[15][19]
Следует избегать последующей беременности, если функция левого желудочка не восстановилась, а ФВ ниже 55%.[2][21] Тем не менее, многие женщины, полностью выздоровевшие после ППКМ, в дальнейшем успешно забеременели.[8] В значительном исследовании сообщается, что риск рецидива сердечной недостаточности у выздоровевших пациенток с ППКМ в результате последующей беременности составляет примерно 21% или выше.[21] Вероятность рецидива может быть еще меньше у пациентов с нормальным сократительным резервом, что продемонстрировано стресс-эхокардиографией.[22][23] При любой последующей беременности необходимо тщательное наблюдение. В случае рецидива следует возобновить обычное лечение, в том числе: гидралазин с нитраты плюс бета-адреноблокаторы во время беременности или ингибиторы АПФ плюс бета-адреноблокаторы после беременности.
Эпидемиология
По оценкам, заболеваемость PPCM в США составляет от 1 на 1300 до 4000 живорождений.[2][20][24] Хотя он может поражать женщин всех рас, в некоторых странах он более распространен; например, по оценкам, частота ППКМ составляет 1 случай на 1000 живорождений в южноафриканских банту и до 1 случая на 300 в Гаити.[9][20]
Некоторые исследования утверждают, что ППКМ может быть немного более распространена среди пожилых женщин, у которых было больше живорожденных детей, и среди женщин старшего и младшего крайнего детородного возраста.[9][24] Однако от четверти до трети пациентов с ППКМ - молодые женщины, родившие впервые.[3][4][9][20][25][26]
Хотя использование токолитический агенты или развитие преэклампсия (токсикоз беременности) и гипертония, вызванная беременностью (PIH) могут способствовать обострению сердечной недостаточности, они не вызывают PPCM; у большинства женщин развился ППКМ, которые не получали токолитики, не имели преэклампсии или ПВГ.[20][25]
Короче говоря, ППКМ может возникнуть у любой женщины любого расового происхождения, в любом возрасте репродуктивного возраста и при любой беременности.[21]
Рекомендации
- ^ ЗАЩИЩЕНО, INSERM US14 - ВСЕ ПРАВА. «Орфанет: послеродовая кардиомиопатия». www.orpha.net. Получено 28 мая 2019.
- ^ а б c d е ж грамм час я j k Пирсон Г.Д., Вейль Дж. С., Рахимтула С. и др. (Март 2000 г.). «Послеродовая кардиомиопатия: рекомендации и обзор семинара Национального института сердца, легких и крови и Управления редких заболеваний (Национальные институты здравоохранения)». JAMA. 283 (9): 1183–8. Дои:10.1001 / jama.283.9.1183. PMID 10703781.
- ^ а б c Элкаям У, Актер М.В., Сингх Х. и др. (Апрель 2005 г.). «Кардиомиопатия, связанная с беременностью: клинические характеристики и сравнение ранних и поздних проявлений». Тираж. 111 (16): 2050–5. Дои:10.1161 / 01.CIR.0000162478.36652.7E. PMID 15851613.
- ^ а б c d е ж грамм час я j k Слива К., Фетт Дж., Элькаям У. (август 2006 г.). «Послеродовая кардиомиопатия». Ланцет. 368 (9536): 687–93. Дои:10.1016 / S0140-6736 (06) 69253-2. ЧВК 4989733. PMID 16920474.
- ^ а б c d е ж грамм Murali S, Baldisseri MR (октябрь 2005 г.). «Послеродовая кардиомиопатия». Крит. Care Med. 33 (10 Suppl): S340–6. Дои:10.1097 / 01.CCM.0000183500.47273.8E. PMID 16215357.
- ^ а б c d е ж Филипс С.Д., Уорнс, Калифорния (2004). «Послеродовая кардиомиопатия: современные терапевтические перспективы». Варианты лечения Curr Cardiovasc Med. 6 (6): 481–488. Дои:10.1007 / s11936-004-0005-8. PMID 15496265.
- ^ Ансари А.А., Фетт Д.Д., Каррауэй Р.Э., Мейн А.Е., Онламун Н., Сандстрем Дж. Б. (декабрь 2002 г.). «Аутоиммунные механизмы как основа послеродовой кардиомиопатии человека». Clin Rev Allergy Immunol. 23 (3): 301–24. Дои:10.1385 / CRIAI: 23: 3: 301. PMID 12402414.
- ^ а б c d е ж грамм Фетт Дж. Д. (октябрь 2008 г.). «Понимание послеродовой кардиомиопатии, 2008». Int. Дж. Кардиол. 130 (1): 1–2. Дои:10.1016 / j.ijcard.2008.03.076. PMID 18590935.
- ^ а б c d е Десаи Д., Мудли Дж., Найду Д. (июль 1995 г.). «Послеродовая кардиомиопатия: опыт в больнице короля Эдуарда VIII, Дурбан, Южная Африка, и обзор литературы». Троп Докт. 25 (3): 118–23. Дои:10.1177/004947559502500310. PMID 7660481.
- ^ а б c Фетт Дж. Д., Кристи Л. Г., Каррауэй Р. Д., Ансари А. А., Сандстрем Дж. Б., Мерфи Дж. Г. (август 2005 г.). «Непризнанная перинатальная кардиомиопатия у гаитянских женщин». Int J Gynaecol Obstet. 90 (2): 161–6. Дои:10.1016 / j.ijgo.2005.05.004. PMID 15961090.
- ^ а б Ласинская-Ковара М, Дудзяк М, Сухожевская Дж. (Сентябрь 2001 г.). «Два случая послеродовой кардиомиопатии, изначально ошибочно диагностированной как тромбоэмболия легочной артерии». Кан Дж Анаэст. 48 (8): 773–7. Дои:10.1007 / BF03016693. PMID 11546718.
- ^ Фасселл К.М., Авад Дж. А., Вэр Л. Б. (апрель 2005 г.). «Случай молниеносной печеночной недостаточности из-за нераспознанной перинатальной кардиомиопатии». Крит. Care Med. 33 (4): 891–3. Дои:10.1097 / 01.CCM.0000158517.25962.8E. PMID 15818120.
- ^ Фетт Дж. Д. (март 2011 г.). «Валидация самодиагностики для ранней диагностики сердечной недостаточности при послеродовой кардиомиопатии». Критические пути в кардиологии (10): 44–45.
- ^ а б c «UOTW # 14 - УЗИ недели». УЗИ недели. 20 августа 2014 г.. Получено 27 мая 2017.
- ^ а б c Амос А.М., Джабер В.А., Рассел С.Д. (сентябрь 2006 г.). «Улучшение результатов в послеродовой кардиомиопатии с помощью современных методов лечения». Являюсь. Сердце J. 152 (3): 509–13. Дои:10.1016 / j.ahj.2006.02.008. PMID 16923422.
- ^ Азиз Т.М., Берджесс М.И., Акладиус Н.Н. и др. (Август 1999 г.). «Трансплантация сердца при перинатальной кардиомиопатии: отчет о трех случаях и обзор литературы». Cardiovasc Surg. 7 (5): 565–7. Дои:10.1016 / S0967-2109 (99) 00014-9. PMID 10499901.
- ^ Hilfiker-Kleiner, D .; Haghikia, A .; Nonhoff, J .; Bauersachs, J. (2015-05-02). «Послеродовая кардиомиопатия: текущее лечение и перспективы на будущее». Европейский журнал сердца. 36 (18): 1090–1097. Дои:10.1093 / eurheartj / ehv009. ISSN 0195-668X. ЧВК 4422973. PMID 25636745.
- ^ а б Felker GM, Jaeger CJ, Klodas E, et al. (Ноябрь 2000 г.). «Миокардит и отдаленная выживаемость при послеродовой кардиомиопатии». Являюсь. Сердце J. 140 (5): 785–91. Дои:10.1067 / mhj.2000.110091. PMID 11054626.
- ^ а б Палмер Б.А., Яноско К.М., Мактирнан К., Шерман Ф., Макнамара Д.М. (2007). «Восстановление левого желудочка при перипартальной кардиомиопатии: влияние бета-блокады (Реферат № 2500)». Тираж. 116 (Приложение II): 551.
- ^ а б c d е Фетт JD, Кристи LG, Carraway RD, Мерфи JG (декабрь 2005 г.). «Пятилетнее проспективное исследование заболеваемости и прогноза перинатальной кардиомиопатии в одном учреждении» (PDF). Mayo Clin. Proc. 80 (12): 1602–6. Дои:10.4065/80.12.1602. PMID 16342653.[постоянная мертвая ссылка]
- ^ а б c Элькаям У., Туммала П.П., Рао К. и др. (Май 2001 г.). «Материнские и внутриутробные исходы последующих беременностей у женщин с перинатальной кардиомиопатией». N. Engl. J. Med. 344 (21): 1567–71. Дои:10.1056 / NEJM200105243442101. PMID 11372007.
- ^ Lampert MB, Weinert L, Hibbard J, Korcarz C, Lindheimer M, Lang RM (январь 1997 г.). «Сократительный резерв у пациентов с перинатальной кардиомиопатией и восстановленной функцией левого желудочка». Являюсь. J. Obstet. Гинеколь. 176 (1 Пет 1): 189–95. Дои:10.1016 / S0002-9378 (97) 80034-8. PMID 9024112.
- ^ Дорбала С., Брозена С., Зеб С. и др. (Январь 2005 г.). «Стратификация риска у женщин с послеродовой кардиомиопатией при первичном обращении: исследование стресс-эхокардиографии с добутамином». J Am Soc Echocardiogr. 18 (1): 45–8. Дои:10.1016 / j.echo.2004.08.027. PMID 15637488.
- ^ а б Мельничук Л.М., Уильямс К., Дэвис Д.Р. и др. (Июнь 2006 г.). «Частота послеродовой кардиомиопатии». Являюсь. Дж. Кардиол. 97 (12): 1765–8. Дои:10.1016 / j.amjcard.2006.01.039. PMID 16765131.
- ^ а б Слива К., Фёрстер О., Либхабер Э. и др. (Февраль 2006 г.). «Послеродовая кардиомиопатия: воспалительные маркеры как предикторы исхода у 100 проспективно изученных пациентов». Евро. Сердце J. 27 (4): 441–6. Дои:10.1093 / eurheartj / ehi481. PMID 16143707.
- ^ Слива К., Скудицки Д., Бергеманн А., Кэнди Дж., Пурен А., Сарели П. (март 2000 г.). «Послеродовая кардиомиопатия: анализ клинических исходов, функция левого желудочка, уровни цитокинов в плазме крови и Fas / APO-1». Варенье. Coll. Кардиол. 35 (3): 701–5. Дои:10.1016 / S0735-1097 (99) 00624-5. PMID 10716473.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |