WikiDer > Миома матки - Википедия
| Миома матки | |
|---|---|
| Другие имена | Лейомиома матки, миома матки, миома, фибромиома, фибролейомиома |
 | |
| Миома матки во время лапароскопическая хирургия | |
| Специальность | Гинекология |
| Симптомы | Болезненный или же тяжелые периоды[1] |
| Осложнения | Бесплодие[1] |
| Обычное начало | Средний и более поздние репродуктивные годы[1] |
| Причины | Неизвестный[1] |
| Факторы риска | История семьи, ожирение, принимать пищу красное мясо[1] |
| Диагностический метод | Тазовое обследование, медицинская визуализация[1] |
| Дифференциальная диагностика | Лейомиосаркома, беременность, киста яичника, рак яичников[2] |
| Уход | Лекарства, хирургия, эмболизация маточной артерии[1] |
| Медикамент | Ибупрофен, парацетамол (ацетаминофен), добавки железа, агонист гонадотропин-рилизинг-гормона[1] |
| Прогноз | Улучшение после менопауза[1] |
| Частота | ~ 50% женщин к 50 годам[1] |
Миома матки, также известный как лейомиомы матки или же миома, находятся доброкачественные опухоли гладких мышц из матка.[1] У большинства женщин симптомы отсутствуют, в то время как у других могут быть болезненный или же тяжелые периоды.[1] Если они достаточно большие, они могут мочевой пузырь вызывая частые позывы к мочеиспусканию.[1] Они также могут вызывать боль во время секса или же боль в пояснице.[1][3] У женщины может быть одна миома матки или несколько.[1] Иногда миома может затруднить превращение беременная, хотя это редкость.[1]
Точная причина миомы матки неясна.[1] Однако миома передается по наследству и, по-видимому, частично определяется гормон уровни.[1] Факторы риска включают: ожирение и ест красное мясо.[1] Диагноз может быть проведен тазовое обследование или же медицинская визуализация.[1]
Если симптомы отсутствуют, лечение обычно не требуется.[1] НПВП, Такие как ибупрофен, может помочь при боли и кровотечении во время парацетамол (ацетаминофен) может помочь при боли.[1][4] Утюг пищевые добавки могут потребоваться людям с тяжелыми менструациями.[1] Лекарства агонист гонадотропин-рилизинг-гормона может уменьшить размер миомы, но они дороги и связаны с побочными эффектами.[1] Если симптомы более выражены, может помочь операция по удалению миомы или матки.[1] Эмболизация маточной артерии также может помочь.[1] Раковые разновидности миомы очень редки и известны как лейомиосаркомы.[1] Они не развиваются из доброкачественных миом.[1]
К 50 годам миома развивается у 20–80% женщин.[1] По оценкам, в 2013 году во всем мире пострадал 171 миллион женщин.[5] Обычно они встречаются в среднем и позднем репродуктивном возрасте.[1] После менопауза, они обычно уменьшаются в размере.[1] в Соединенные Штаты, миома матки - частая причина хирургическое удаление матки.[6]
Признаки и симптомы
У некоторых женщин миома матки протекает бессимптомно. Боль в животе, анемия и усиление кровотечения могут указывать на наличие миомы.[7] Также может быть боль во время полового акта, в зависимости от расположения миомы. В течение беременность, они также могут быть причиной выкидыш,[8] кровотечение преждевременные роды, или вмешательство в положение плода.[нужна цитата] Миома матки может вызвать ректальное давление. Живот может увеличиваться в размерах, имитируя внешний вид беременности.[1] Некоторые крупные миомы могут распространяться через шейку матки и влагалище.[7]
Хотя миомы встречаются часто, они не являются типичной причиной бесплодия, составляя около 3% причин, по которым женщина не может иметь ребенка.[9] У большинства женщин с миомой матки исход беременности будет нормальным.[10][11] В случае интеркуррентной миомы матки при бесплодии, миома обычно располагается в подслизистом месте, и считается, что это место может мешать функции слизистой оболочки и способности эмбриона к размножению. имплант.[9]
Факторы риска
Некоторые факторы риска, связанные с развитием миомы матки, можно изменить.[12]Миома чаще встречается у полных женщин.[13] Рост миомы зависит от эстрогена и прогестерона, поэтому она актуальна только в репродуктивном возрасте.
Рацион питания
Диета с высоким содержанием фруктов и овощей, как правило, снижает риск развития миомы.[12] Клетчатка, витамины А, С и Е, фитоэстрогены, каротиноиды, мясо, рыба и молочные продукты имеют неясное действие.[12] Нормальный уровень витамина D в рационе может снизить риск развития миомы.[12]
Генетика
Пятьдесят процентов миомы матки демонстрируют генетическую аномалию. Часто на некоторых хромосомах обнаруживается транслокация.[7] Миома частично генетическая. Если у матери была миома, риск для дочери примерно в три раза выше среднего.[14]У чернокожих женщин вероятность развития миомы матки в 3-9 раз выше, чем у белых.[15] Только несколько специфических генов или цитогенетических отклонений связаны с миомой.[16] 80-85% миомы имеют мутацию в субъединице 12 медиаторного комплекса (MED12) ген.[17][18]
Семейные лейомиомы
Синдром (Синдром Рида), которая вызывает лейомиому матки наряду с кожными лейомиомами и почечно-клеточный рак было сообщено.[19][20][21] Это связано с мутацией в гене, который производит фермент. фумаратгидратаза, расположенный на длинной руке хромосома 1 (1q42.3-43). Наследование аутосомно-доминантный.
Патофизиология
Миома - это разновидность матки. лейомиома. Фибромы выглядят примерно как круглые, четко очерченные (но не инкапсулированные) твердые узелки белого или коричневого цвета, на гистологическом срезе видны завитки. Размер варьируется от микроскопических до значительных размеров. Обычно поражения размером с грейпфрут или больше пациент ощущает через брюшную стенку.[1]
Микроскопически опухолевые клетки напоминают нормальные клетки (удлиненные, веретеновидные, с сигарообразным ядром) и образуют разнонаправленные пучки (завитки). Эти клетки одинаковы по размеру и форме, с редкими митозами. Выделяют три доброкачественных варианта: причудливый (атипичный); сотовый; и митотически активный.
Появление выступающих ядрышек с перинуклеолярными ореолами должно насторожить патолога, чтобы он исследовал возможность чрезвычайно редкого наследственного лейомиоматоза и синдрома почечно-клеточного рака (Рида).[22]
Расположение и классификация
Рост и местоположение являются основными факторами, определяющими, приводит ли миома к симптомам и проблемам.[6] Небольшое поражение может быть симптоматическим, если оно расположено в полости матки, в то время как большое поражение за пределами матки может остаться незамеченным. Различные местоположения классифицируются следующим образом:
- Интрамуральные миомы расположены внутри мышечной стенки матки. Если они не большие, они могут протекать бессимптомно. Интрамуральные миомы начинаются с небольших узелков в мышечной стенке матки. Со временем интрамуральные миомы могут расширяться внутрь, вызывая деформацию и удлинение полости матки.
- Подсерозные миомы расположены на поверхности матки. Они также могут расти наружу от поверхности и оставаться прикрепленными к небольшому кусочку ткани, и тогда их называют миомами на ножке.[1]
- Подслизистые миомы являются наиболее распространенным типом, располагаются в мышце под эндометрием матки и деформируют полость матки; даже небольшие поражения в этом месте могут привести к кровотечению и бесплодие. Поражение на ножке внутри полости называется внутриполостной миомой и может проходить через шейку матки.
- Миома шейки матки расположены в стенке шейки матки (шейка матки). Редко миомы обнаруживаются в опорных конструкциях (круглая связка, широкой связки, или же маточно-крестцовая связка) матки, которые также содержат гладкую мышечную ткань.
Миома может быть одиночной или множественной. Большинство миомы начинаются в мышечной стенке матки. При дальнейшем росте некоторые поражения могут развиваться по направлению к внешней стороне матки или к внутренней полости. Вторичные изменения, которые могут развиться внутри миомы, включают кровотечение, некроз, кальцификацию и кистозные изменения. Они имеют тенденцию кальцифицироваться после менопаузы.[23]
Если в матке содержится слишком много, чтобы сосчитать, это называется диффузный лейомиоматоз матки.
Внематочные миомы маточного происхождения, метастатические миомы
Миомы маточного происхождения, расположенные в других частях тела, иногда также называемые паразитарными миомами, исторически встречались крайне редко, но в настоящее время их диагностируют все чаще. Они могут быть связаны или идентичны метастазирующим лейомиома.
В большинстве случаев они все еще зависят от гормонов, но могут вызывать опасные для жизни осложнения, когда появляются в отдаленных органах. Некоторые источники предполагают, что значительная часть случаев может быть поздними осложнениями хирургических вмешательств, таких как миомэктомия или гистерэктомия. В частности, лапароскопическая миомэктомия с использованием морцеллятора связана с повышенным риском этого осложнения.[24][25][26]
Существует ряд редких состояний, при которых фибромы метастазируют. Они по-прежнему растут без вреда для здоровья, но могут быть опасны в зависимости от их местоположения.[27]
- При лейомиоме с сосудистой инвазией обычная миома проникает в сосуд, но риска рецидива нет.
- В внутривенный лейомиоматоз, лейомиомы растут в венах, источником которых является миома матки. Поражение сердца может быть фатальным.
- При доброкачественной метастазирующей лейомиоме лейомиомы растут в более отдаленных местах, таких как легкие и лимфатические узлы. Источник не совсем ясен. Поражение легких может быть фатальным.
- При диссеминированном внутрибрюшинном лейомиоматозе лейомиомы разрастаются диффузно на перитонеальной и сальниковой поверхностях, причем их источником является миома матки. Это может имитировать злокачественную опухоль, но ведет себя доброкачественно.
Патогенез
Миомы моноклональный опухоли и примерно от 40 до 50% показывают кариотипически обнаруживаемый хромосомные аномалии.При наличии множественных миом они часто имеют несвязанные генетические дефекты. Специфические мутации MED12 белок был отмечен в 70 процентах миомы.[28]
Точная причина миомы до конца не выяснена, но текущая рабочая гипотеза состоит в том, что генетическая предрасположенность, пренатальное воздействие гормонов и эффекты гормонов, факторов роста и ксеноэстрогены вызвать рост миомы. Известные факторы риска - африканское происхождение, ожирение, синдром поликистоза яичников, сахарный диабет, гипертония, и никогда не рожала.[29]
Считается, что эстроген и прогестерон имеют митогенный воздействуют на клетки лейомиомы, а также действуют, влияя (прямо или косвенно) на большое количество факторы роста, цитокины и факторы апоптоза, а также другие гормоны. Более того, действие эстрогена и прогестерона регулируется перекрестным взаимодействием эстрогена, прогестерона и пролактин передача сигналов, которая контролирует экспрессию соответствующих ядерных рецепторов. Считается, что эстроген способствует росту за счет активации IGF-1, EGFR, TGF-beta1, TGF-beta3 и PDGF, и способствует аберрантному выживанию клеток лейомиомы путем подавления p53, увеличивая экспрессию антиапоптотического фактора PCP4 и противодействовать PPAR-гамма сигнализация. Считается, что прогестерон способствует росту лейомиомы за счет активации EGF, TGF-beta1 и TGF-beta3, и способствует выживанию за счет повышающей регуляции Bcl-2 экспрессия и подавление TNF-альфа. Считается, что прогестерон противодействует росту, подавляя IGF-1.[30] Выражение трансформирующий фактор взаимодействия роста (TGIF) увеличивается при лейомиоме по сравнению с миометрием.[31] TGIF - потенциальный репрессор TGF-β пути в клетках миометрия.[31]
Ароматаза и 17-бета-гидроксистероиддегидрогеназа аномально экспрессируются в миомах, что указывает на то, что миомы могут превращать циркулирующий андростендион в эстрадиол.[32] Подобный механизм действия был выяснен в эндометриоз и другие заболевания эндометрия.[33] В настоящее время для лечения рассматриваются ингибиторы ароматазы, в определенных дозах они полностью подавляли бы выработку эстрогена в миоме, не влияя в значительной степени на выработку эстрогена яичниками (и, следовательно, на его системные уровни). Избыточная экспрессия ароматазы особенно выражена у афроамериканок.[34]
Рассматриваются генетические и наследственные причины, и некоторые эпидемиологические данные указывают на значительное генетическое влияние, особенно в случаях с ранним началом. Родственники первой степени родства имеют 2,5-кратный риск и почти 6-кратный риск при рассмотрении случаев с ранним началом. Монозиготные близнецы имеют двойную степень соответствия для гистерэктомии по сравнению с дизиготные близнецы.[35]
Расширение миомы матки происходит за счет медленной скорости пролиферации клеток в сочетании с производством большого количества внеклеточный матрикс.[34]
Небольшая популяция клеток миомы матки обладает свойствами стволовые клетки или же клетки-предшественники, и вносят значительный вклад в яичниковый стероид-зависимый рост миомы. Эти стволовые клетки-предшественники испытывают дефицит рецептора эстрогена α и рецептора прогестерона и вместо этого полагаются на значительно более высокие уровни этих рецепторов в окружающих дифференцированных клетках, чтобы опосредовать действие эстрогена и прогестерона посредством паракринная передача сигналов.[34]
Диагностика
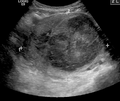
Установлено наличие миомы матки по сравнению с опухолью придатков. Миомы могут быть ошибочно приняты за новообразования яичников. Необычная опухоль, которую можно принять за миому, - это саркома ботриоидес. Чаще встречается у детей и подростков. Как и миома, она также может выступать из влагалища и отличается от миомы.[7] Пока пальпация используется в тазовое обследование обычно можно определить наличие более крупных миомы, гинекологическое ультразвуковое исследование (УЗИ) превратился в стандартный инструмент для оценки матки на наличие миомы. Сонография изобразит миомы как очаговые образования с неоднородной текстурой, которые обычно вызывают затенение ультразвукового луча. Можно определить местоположение и измерить размеры поражения. Также магнитно-резонансная томография (МРТ) можно использовать для определения размера и расположения миомы в матке.[нужна цитата]
Методы визуализации не могут четко отличить доброкачественную лейомиому матки от злокачественной лейомиосаркомы матки, однако последняя встречается довольно редко. Быстрый или неожиданный рост, например увеличение очага после менопаузы, повышает уровень подозрения, что поражение может быть саркомой. Кроме того, при запущенных злокачественных новообразованиях могут быть признаки местной инвазии. Биопсия выполняется редко и редко является диагностической. Если после УЗИ и МРТ есть неясный диагноз, обычно показана операция.[нужна цитата]
Другие методы визуализации, которые могут быть особенно полезны при оценке поражений в полости матки: гистеросальпингография или же соногистерография.[нужна цитата]
Очень большая (9 см) миома матки, вызывающая синдром заложенности таза как видно на КТ
Очень большая (9 см) миома матки, которая вызывает синдром заложенности таза, как показано на УЗИ
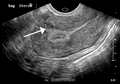
Небольшая миома матки, видимая в стенке миометрий на поперечном ультразвуковом изображении
Гистопатология миомы матки обычно имеют гладкую мускулатуру в виде завитков (пучков).[36]
Этот вариант Пятно Ван Гизона отличает мышцу (желтый) от соединительной ткани (красный)
Сосуществующие расстройства
Миома, которая приводит к обильному вагинальному кровотечению, приводит к анемия и недостаток железа. Из-за воздействия давления желудочно-кишечные проблемы, такие как запор и вздутие живота. Сдавление мочеточника может привести к гидронефроз. Фибромы также могут присутствовать эндометриоз, что само по себе может вызвать бесплодие. Аденомиоз может быть ошибочно принят за миому или сосуществовать с ней.
В очень редких случаях злокачественные новообразования, лейомиосаркома, миометрия может развиваться.[37] В очень редких случаях миома матки может быть частью или ранним симптомом наследственный лейомиоматоз и почечно-клеточный рак синдром.
Уход
Большинство миомы не требуют лечения, если только они не вызывают симптомов. После менопаузы миомы уменьшаются в размерах, и для них это необычно.
Симптоматическую миому матки можно лечить:
- лекарства для контроля симптомов (например, симптоматическое лечение)
- лекарство, направленное на уменьшение опухолей
- ультразвуковая деструкция миомы
- миомэктомия или же радиочастотная абляция
- гистерэктомия
- эмболизация маточной артерии
У тех, у кого есть симптомы, эмболизация маточной артерии и хирургические варианты имеют аналогичные результаты в отношении удовлетворенности.[38]
Медикамент
Для контроля симптомов можно использовать ряд лекарств. НПВП можно использовать для уменьшения болезненных менструаций. Для уменьшения маточного кровотечения и спазмов могут быть назначены оральные противозачаточные таблетки.[9] Анемию можно лечить добавками железа.
Левоноргестрел внутриматочные спирали эффективны для ограничения менструального кровотока и улучшения других симптомов. Побочных эффектов обычно немного, так как левоноргестрел (а прогестин) локально выделяется в низкой концентрации.[39] В то время как большинство исследований левонгестрела-ВМС было сосредоточено на лечении женщин без миомы, некоторые сообщили о хороших результатах, особенно для женщин с миомой, включая существенную регрессию миомы.[40][41]
Каберголин В двух исследованиях было показано, что в умеренных и хорошо переносимых дозах эффективно сокращаются миомы. Механизм действия, ответственного за то, как каберголин сокращает миомы, неясен.[40]
Улипристала ацетат синтетический селективный модулятор рецепторов прогестерона (SPRM), который имеет предварительные доказательства в поддержку его использования для дооперационного лечения миомы с небольшими побочными эффектами.[42] Миома, подвергавшаяся длительному лечению УПА, показала уменьшение объема примерно на 70%.[43] В некоторых случаях используется только УПА для облегчения симптомов без хирургического вмешательства.[7]
Даназол является эффективным средством для уменьшения миомы и контроля симптомов. Его использование ограничено неприятными побочными эффектами. Механизм действия считается антиэстрогенным. Недавний опыт показывает, что профиль безопасности и побочных эффектов можно улучшить за счет более осторожного дозирования.[40]
Аналоги гонадотропин-рилизинг-гормона вызвать временную регрессию миомы за счет снижения уровня эстрогена. Из-за ограничений и побочных эффектов этого лекарства его редко рекомендуют, кроме как для предоперационного использования, для уменьшения размера миомы и матки перед операцией. Обычно его используют максимум 6 месяцев или меньше, потому что после более длительного использования они могут вызвать остеопороз и другие типичные постменопаузальные осложнения. Основные побочные эффекты - преходящие симптомы постменопаузы. Во многих случаях миома возобновляется после прекращения лечения, однако в некоторых случаях значительные преимущества могут сохраняться намного дольше. Возможны несколько вариантов, например, агонисты ГнРГ с дополнительными схемами, предназначенными для уменьшения побочных эффектов дефицита эстрогена. Возможны несколько режимов добавления, тиболон, ралоксифен, прогестагены один, эстроген отдельно и в сочетании с эстрогенами и прогестагенами.[40]
Прогестерон антагонисты, такие как мифепристон были протестированы, есть доказательства того, что он облегчает некоторые симптомы и улучшает качество жизни, но из-за неблагоприятных гистологических изменений, которые наблюдались в нескольких исследованиях, в настоящее время его нельзя рекомендовать вне рамок исследований.[44][45] Рост миомы возобновился после прекращения лечения антипрогестинами.[34]
Ингибиторы ароматазы были использованы экспериментально для уменьшения миомы. Считается, что этот эффект частично обусловлен снижением системных уровней эстрогена и частично ингибированием локально сверхэкспрессируемой ароматазы в миомах.[40] Однако рост миомы возобновился после прекращения лечения.[34] Опыт экспериментального лечения ингибитором ароматазы эндометриоз указывает на то, что ингибиторы ароматазы могут быть особенно полезными в комбинации с прогестагенным ингибитором овуляции.
Маточная артерия
Эмболизация маточной артерии (ОАЭ) - это неинвазивная процедура, которая блокирует кровоток к миомам, вызывая их сокращение.[46] Долгосрочные результаты в отношении того, насколько люди довольны процедурой, аналогичны результатам операции.[47] Есть предварительные доказательства того, что традиционная хирургия может улучшить фертильность.[47] Один обзор показал, что ОАЭ удваивают будущий риск выкидыш.[48] ОАЭ также требует большего количества повторных процедур, чем если бы операция была сделана изначально.[47] Обычно человек восстанавливается после процедуры в течение нескольких дней.
Перевязка маточной артерии, иногда также лапароскопическая окклюзия маточных артерий - это минимально инвазивные методы ограничения кровоснабжения матки с помощью небольшой операции, которая может выполняться трансвагинально или лапароскопически. Основной механизм действия может быть таким же, как и в ОАЭ, но его легче выполнить, и ожидается меньше побочных эффектов.[49][неосновной источник необходим][50][неосновной источник необходим]
В рекомендациях NICE 2016 года (Национальный институт клинического совершенства - негосударственный государственный орган, который публикует руководства по использованию медицинских технологий и надлежащей клинической практике в Соединенном Королевстве) говорится, что ОАЭ / UFE могут предлагаться женщинам с симптоматической миомой (обычно миома Размером> 30 мм). Женщины должны быть проинформированы о том, что ЭМА и миомэктомия (хирургическое удаление миомы) потенциально могут позволить им сохранить фертильность.[51]
Миомэктомия

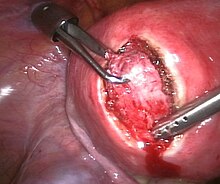
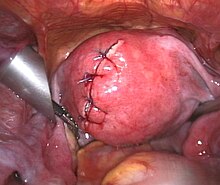
Миомэктомия - это операция по удалению одной или нескольких миомы. Обычно его рекомендуют, когда более консервативные методы лечения не помогают женщинам, которые хотят сохранить фертильность или хотят сохранить матку.[52]
Существует три типа миомэктомии:
- В гистероскопический миомэктомия (также называемая трансшейный резекция) фибромы можно удалить с помощью резектоскопа или эндоскопический инструмент, вводимый через влагалище и шейку матки, который может использовать высокочастотную электрическую энергию для разрезания ткани, или подобное устройство.
- А лапароскопический миомэктомия выполняется через небольшой разрез около пупка. Для удаления миомы врач использует лапароскоп и хирургические инструменты. Исследования показали, что лапароскопическая миомэктомия приводит к снижению болезненность темпы и более быстрое восстановление, чем при лапаротомной миомэктомии.[53]
- А лапаротомический миомэктомия (также известная как открыто или же брюшной миомэктомия) - это наиболее инвазивная хирургическая процедура по удалению миомы. Врач делает разрез в брюшной стенке и удаляет миому из матки.
При лапароскопической миомэктомии меньше боли и меньше времени в больнице, чем при открытой операции.[54]
Гистерэктомия
Гистерэктомия был классическим методом лечения миомы. Хотя сейчас это рекомендуется только как последний вариант, миома по-прежнему является основной причиной гистерэктомии в США.
Абляция эндометрия
Абляция эндометрия может использоваться, если миома находится только внутри матки, а не интрамурально и относительно небольшая. Ожидается высокая частота неудач и рецидивов при наличии больших или интрамуральных миомы.
Прочие процедуры
Радиочастотная абляция это малоинвазивное лечение миомы.[55] В этом методе миома сокращается путем введения иглоподобного устройства в миому через брюшную полость и нагревания ее с помощью радиочастотной (RF) электрической энергии, чтобы вызвать некроз ячеек. Это лечение является потенциальным вариантом для женщин с миомой, завершивших деторождение и желающих избежать гистерэктомии.
Сфокусированный ультразвук под магнитным резонансом, представляет собой неинвазивное вмешательство (не требующее разрезов), при котором используются сфокусированные УЗИ волны для разрушения тканей в сочетании с магнитно-резонансная томография (МРТ), который направляет и контролирует лечение. Во время процедуры направляется и контролируется доставка сфокусированной ультразвуковой энергии с помощью МРТ-тепловизора.[56] Пациенты с симптоматической миомой, желающие выбрать неинвазивное лечение и не имеющие противопоказаний к МРТ, являются кандидатами на MRgFUS. Около 60% пациентов соответствуют требованиям. Это амбулаторная процедура, которая занимает от одного до трех часов в зависимости от размера миомы. Это безопасно и около 75% эффективности.[57] Симптоматическое улучшение сохраняется в течение двух с лишним лет.[58] Потребность в дополнительном лечении варьируется от 16 до 20% и во многом зависит от количества миомы, которую можно безопасно удалить; чем выше объем абляции, тем ниже частота повторной обработки.[59] В настоящее время нет рандомизированного исследования между MRgFUS и ОАЭ. В настоящее время проводится многоцентровое исследование для изучения эффективности MRgFUS по сравнению с ОАЭ.
Прогноз
Около 1 из 1000 поражений являются или становятся злокачественными, обычно в виде лейомиосаркома по гистологии.[9] Признаком того, что поражение может быть злокачественным, является его рост после менопауза.[9] Среди патологов нет единого мнения относительно трансформации лейомиома в саркому.
Метастаз
Существует ряд редких состояний, при которых фибромы метастазируют. Они по-прежнему растут без вреда для здоровья, но могут быть опасны в зависимости от их местоположения.[27]
Видеть внематочные миомы.
Эпидемиология
К 50 годам миома развивается у 20–80% женщин.[12][1] По оценкам, в 2013 году во всем мире пострадал 171 миллион женщин.[5] Обычно они встречаются в среднем и позднем репродуктивном возрасте.[1] После менопауза они обычно уменьшаются в размерах.[1] Операция по удалению миомы матки чаще встречается у женщин из «высших социальных слоев».[12] У подростков миома матки развивается гораздо реже, чем у женщин старшего возраста.[7] До 50% женщин с миомой матки не имеют симптомов. Распространенность миомы матки среди подростков составляет 0,4%.[7]
Европа
Считается, что заболеваемость миомой матки в Европе ниже, чем в США.[12]
Соединенные Штаты
По данным Национального института гигиены окружающей среды, у 80% афроамериканских женщин к 40 годам разовьются доброкачественные опухоли миомы матки.[60] Афроамериканки в два-три раза чаще заболевают миомой, чем женщины европеоидной расы.[12][13][61] У афроамериканских женщин миомы появляются в более молодом возрасте, быстрее растут и чаще вызывают симптомы.[62] Это приводит к более высокому количеству хирургических операций у афроамериканцев, как миомэктомии, так и гистерэктомии.[63] Повышенный риск миомы у афроамериканцев ухудшает их состояние при лечении бесплодия in vitro и повышает риск преждевременных родов и родоразрешения путем кесарева сечения.[63]
Непонятно, почему миома чаще встречается у афроамериканок. Некоторые исследования показывают, что чернокожие женщины, страдающие ожирением и высоким кровяным давлением, чаще страдают миомой.[63] Другие предполагаемые причины включают тенденцию афроамериканских женщин потреблять пищу с меньшей дневной потребностью в витамине D.[12]
Соответствующее законодательство
Соединенные Штаты
Законопроект S.1289 2005 года был прочитан дважды и передан в комитет по здравоохранению, труду и пенсиям, но так и не прошел Сенат или же жилой дом голосование; в предлагаемом Законе об исследованиях и образовании миомы матки от 2005 г. упоминается, что ежегодно на гистерэктомия операции каждый год, которыми страдают 22% афроамериканцев и 7% женщин европеоидной расы. В законопроекте также содержится призыв к увеличению финансирования исследовательских и образовательных целей. В нем также говорится, что из 28 миллиардов долларов, выданных NIH, 5 миллионов долларов были выделены на миому матки в 2004 году.[64]
Другие животные
Миома матки редко встречается у других млекопитающих, хотя они наблюдались у некоторых собак и балтийских серые тюлени.[65]
Исследование
Селективные модуляторы рецепторов прогестерона, Такие как прогента, находятся под следствием. Другой селективный модулятор рецепторов прогестерона асоприснил проходит испытания с многообещающими результатами в качестве возможного использования в качестве средства лечения миомы, призванного обеспечить преимущества антагонистов прогестерона без их побочных эффектов.[40] Низкое диетическое потребление Витамин Д связано с развитием миомы матки.[12]
Рекомендации
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае аф аг ах ай эй ак «Информационный бюллетень по миоме матки». Управление по женскому здоровью. 15 января 2015 года. В архиве из оригинала 7 июля 2015 г.. Получено 26 июн 2015.
- ^ Ферри, Фред Ф. (2010). Дифференциальный диагноз Ферри: практическое руководство по дифференциальной диагностике симптомов, признаков и клинических расстройств (2-е изд.). Филадельфия, Пенсильвания: Эльзевьер / Мосби. п. Глава U. ISBN 978-0323076999.
- ^ «Миома матки | Миома | MedlinePlus». Получено 2018-11-07.
- ^ Кашани Б.Н.; Centini, G; Морелли, СС; Вайс, G; Петралья, Ф (июль 2016 г.). «Роль медицинского лечения лейомиомы матки». Лучшие практики и исследования. Клиническое акушерство и гинекология. 34: 85–103. Дои:10.1016 / j.bpobgyn.2015.11.016. PMID 26796059.
- ^ а б Исследование глобального бремени болезней, 2013 г., соавторы (5 июня 2015 г.). «Глобальная, региональная и национальная заболеваемость, распространенность и годы, прожитые с инвалидностью для 301 острого и хронического заболевания и травмы в 188 странах, 1990–2013 гг .: систематический анализ для исследования глобального бремени болезней 2013». Ланцет. 386 (9995): 743–800. Дои:10.1016 / S0140-6736 (15) 60692-4. ЧВК 4561509. PMID 26063472.
- ^ а б Валлах Э. Э., Влахос Н. Ф. (август 2004 г.). «Миома матки: обзор развития, клинические особенности и лечение». Акушер Гинеколь. 104 (2): 393–406. Дои:10.1097 / 01.AOG.0000136079.62513.39. PMID 15292018.
- ^ а б c d е ж грамм Мороний, Рафаэль Мендес; Виейра, Каролина Сейлз; Ферриани, Руи Альберто; душ Рейс, Розана Мария; Ногейра, Антонио Альберто; Брито, Луис Густаво Оливейра (2015). «Представление и лечение лейомиомы матки в подростковом возрасте: систематический обзор». BMC Women's Health. 15 (1): 4. Дои:10.1186 / s12905-015-0162-9. ISSN 1472-6874. ЧВК 4308853. PMID 25609056.
- ^ Метвалли, Мостафа; Ли, Тин-Чиу (2015). Репродуктивная хирургия при вспомогательном зачатии. п. 107. ISBN 9781447149538.
- ^ а б c d е Буклет для пациентов Американского общества репродуктивной медицины: Миома матки, 2003 В архиве 2008-07-03 на Wayback Machine
- ^ Сегарс Дж. Х., Парротт Э. К., Нагель Дж. Д., Гуо XC, Гао X, Бирнбаум Л. С., Пинн В. В., Диксон Д. (2014). «Труды Третьего Международного конгресса национальных институтов здравоохранения по достижениям в исследованиях лейомиомы матки: всесторонний обзор, резюме конференции и будущие рекомендации». Обновление репродукции человека. 20 (3): 309–333. Дои:10.1093 / humupd / dmt058. ЧВК 3999378. PMID 24401287.
- ^ Сегарс Дж. Х., Парротт Э. К., Нагель Дж. Д., Гуо XC, Гао X, Бирнбаум Л. С., Пинн В. В., Диксон Д. (2014). «Труды Третьего Международного конгресса национальных институтов здравоохранения по достижениям в исследованиях лейомиомы матки: всесторонний обзор, резюме конференции и будущие рекомендации». Гм. Репрод. Обновлять. 20 (3): 309–33. Дои:10.1093 / humupd / dmt058. ЧВК 3999378. PMID 24401287.
- ^ а б c d е ж грамм час я j Параццини, Фабио; Ди Мартино, Мирелла; Кандиани, Массимо; Вигано, Паола (2015). «Диетические компоненты и лейомиомы матки: обзор опубликованных данных». Питание и рак. 67 (4): 569–579. Дои:10.1080/01635581.2015.1015746. ISSN 0163-5581. PMID 25826470.
- ^ а б Миома матки в Руководство по диагностике и терапии Merck Профессиональное издание
- ^ "Информационный бюллетень о миоме матки". womenshealth.gov. 2016-12-15. В архиве из оригинала от 09.02.2016.
- ^ Юнас, Кинза; Хадура, Эссам; Майоко, Франц; Бункейла, Аднан (январь 2016 г.). «Обзор научно-обоснованного лечения миомы матки». Акушер и гинеколог. 18 (1): 33–42. Дои:10.1111 / tog.12223.
- ^ Medikare, V; Кандукури, LR; Анантапур, V; Динадаял, М; Наллари, П. (июль 2011 г.). «Генетические основы миомы матки; обзор». Журнал репродукции и бесплодия. 12 (3): 181–91. ЧВК 3719293. PMID 23926501.
- ^ Kämpjärvi K, Park MJ, Mehine M, Kim NH, Clark AD, Bützow R, Böhling T, Böhm J, Mecklin JP, Järvinen H, Tomlinson IP, van der Spuy ZM, Sjöberg J, Boyer TG, Vahteristo P (сентябрь 2014 г.) . «Мутации в экзоне 1 подчеркивают роль MED12 в лейомиомах матки». Человеческая мутация. 35 (9): 1136–41. Дои:10.1002 / humu.22612. PMID 24980722.
- ^ Heinonen HR, Pasanen A, Heikinheimo O, Tanskanen T, Palin K, Tolvanen J, Vahteristo P, Sjöberg J, Pitkänen E, Bützow R, Mäkinen N, Aaltonen LA (2017). «Множественные клинические характеристики разделяют лейомиомы матки с положительной и отрицательной мутацией MED12». Научный представитель. 7 (1): 1015. Дои:10.1038 / s41598-017-01199-0.CS1 maint: несколько имен: список авторов (связь)
- ^ Толванен Дж., Уймари О, Рюйянен М, Аалтонен Л.А., Вахтеристо П. (2012). «Сильный семейный анамнез лейомиоматоза матки требует скрининга мутации фумаратгидратазы». Репродукция человека. 27 (6): 1865–9. Дои:10.1093 / humrep / des105. PMID 22473397.
- ^ Торо Дж. Р. и др. (2003). «Мутации в гене фумаратгидратазы вызывают наследственный лейомиоматоз и почечно-клеточный рак в семьях в Северной Америке». Am J Hum Genet. 73 (1): 95–106. Дои:10.1086/376435. ЧВК 1180594. PMID 12772087.
- ^ «Архивная копия». Архивировано из оригинал на 2012-02-24. Получено 2012-04-09.CS1 maint: заархивированная копия как заголовок (связь)[требуется полная цитата]
- ^ Гарг К., Тикоо С.К., Сослов Р.А., Рейтер В.Е. (2011). «Морфологические особенности лейомиомы матки, связанные с наследственным лейомиоматозом и синдромом почечно-клеточной карциномы». Американский журнал хирургической патологии. 35 (8): 1235–1237. Дои:10.1097 / PAS.0b013e318223ca01. PMID 21753700.
- ^ Импи, Лоуренс; Ребенок, Тим (2016). Акушерство и Гинекология. 24: Джон Уайли и сыновья. ISBN 9781119010807.CS1 maint: location (связь)
- ^ Cucinella G, Granese R, Calagna G, Somigliana E, Perino A (2011). «Паразитарные миомы после лапароскопической операции: возникающее осложнение при использовании морцеллятора? Описание четырех случаев». Фертильность и бесплодие. 96 (2): e90 – e96. Дои:10.1016 / j.fertnstert.2011.05.095. PMID 21719004.
- ^ Нежат Ц., Хо К. (2010). «Ятрогенные миомы: новый класс миом?». Журнал малоинвазивной гинекологии. 17 (5): 544–550. Дои:10.1016 / j.jmig.2010.04.004. PMID 20580324.
- ^ «Обновленная оценка FDA использования лапароскопических силовых морцеллаторов для лечения миомы матки» (PDF). Получено 23 декабря 2017.
- ^ а б Диагностическая гистопатология опухолей Флетчера (3-е изд.). С. 692–4.
- ^ Мякинен Н, Мехине М, Толванен Дж., Каасинен Э., Ли Й, Лехтонен Х. Дж., Джентиле М, Ян Дж., Энге М, Тайпале М, Аавикко М., Катайнен Р., Виролайнен Э, Бёлинг Т., Коски Т. А., Лаунонен В., Сьёберг Дж. , Тайпале Дж., Вахтеристо П., Аалтонен Л.А. (2011). «MED12, медиаторный комплекс субъединицы 12, мутирует с высокой частотой в лейомиомах матки». Наука. 334 (6053): 252–255. Bibcode:2011Наука ... 334..252M. Дои:10.1126 / science.1208930. PMID 21868628.
- ^ Около S (2008). «Заболеваемость, этиология и эпидемиология миомы матки». Лучшие практики и исследования. Клиническое акушерство и гинекология. 22 (4): 571–588. Дои:10.1016 / j.bpobgyn.2008.04.002. PMID 18534913.
- ^ Маруо Т., Охара Н., Ван Дж, Мацуо Х (2004). «Половые стероидные регуляторы роста лейомиомы матки и апоптоза». Обновление репродукции человека. 10 (3): 207–220. Дои:10.1093 / humupd / dmh019. PMID 15140868.
- ^ а б Йен-Пинг Хо Дж, Ман У.С., Вэнь И, Полан М.Л., Ши-Чу Хо Э, Чен Б. (июнь 2009 г.). «Преобразование экспрессии взаимодействующего фактора роста в лейомиоме по сравнению с миометрием». Fertil. Стерил. 94 (3): 1078–83. Дои:10.1016 / j.fertnstert.2009.05.001. ЧВК 2888713. PMID 19524896.
- ^ Сёзу М., Мураками К., Иноуэ М. (2004). «Ароматаза и лейомиома матки». Семинары по репродуктивной медицине. 22 (1): 51–60. Дои:10.1055 / с-2004-823027. PMID 15083381.
- ^ Булун ЮВ, Ян С., Фанг З., Гуратес Б., Тамура М., Чжоу Дж., Себастьян С. (2001). «Роль ароматазы в заболевании эндометрия». Журнал стероидной биохимии и молекулярной биологии. 79 (1–5): 19–25. Дои:10.1016 / S0960-0760 (01) 00134-0. PMID 11850203.
- ^ а б c d е Моравек, МБ; Инь, П; Оно, М; Coon, JS; Дайсон, MT; Наварро, А; Marsh, EE; Чакраварти, Д; Ким, Джей Джей; Вэй, JJ; Булун, С.Е. (февраль 2015 г.). «Стероиды яичников, стволовые клетки и лейомиома матки: терапевтическое значение». Обновление репродукции человека (Рассмотрение). 21 (1): 1–12. Дои:10.1093 / humupd / dmu048. ЧВК 4255606. PMID 25205766.
- ^ Ходж Дж. К., Мортон СС (2007). «Генетическая гетерогенность лейомиомы матки: понимание злокачественного прогрессирования». Молекулярная генетика человека. 16 Спец. № 1: Р7–13. Дои:10.1093 / hmg / ddm043. PMID 17613550.
- ^ Мохамед Мохтар Десуки. «Матка - Стромальные опухоли - Лейомиома». Патология Очертания. Тема завершена: 1 августа 2011 г. Доработана: 15 декабря 2019 г.
- ^ «Миома». NHS Choices. Национальная служба здравоохранения Великобритании. 2017-10-19. В архиве из оригинала от 05.05.2008.
- ^ Гупта Дж. К., Синха А., Ламсден М. А., Хики М. (26 декабря 2014 г.). «Эмболизация маточной артерии при симптоматической миоме матки». Кокрановская база данных систематических обзоров. 12 (12): CD005073. Дои:10.1002 / 14651858.CD005073.pub4. PMID 25541260.
- ^ Сапата Л.Б., Уайтман М.К., Теппер Н.К., Джеймисон Д.Д., Марчбэнкс ПА, Кертис К.М. (2010). «Использование внутриматочных спиралей среди женщин с миомой матки: систематический обзор ☆». Контрацепция. 82 (1): 41–55. Дои:10.1016 / j.contraception.2010.02.011. PMID 20682142.
- ^ а б c d е ж Шанкаран С., Маньонда ИТ (2008). «Лечебное лечение миомы» (PDF). Лучшая практика Res Clin Obstet Gynaecol. 22 (4): 655–76. Дои:10.1016 / j.bpobgyn.2008.03.001. PMID 18468953. В архиве (PDF) из оригинала от 11.09.2011.
- ^ Кайласам С., Кэхилл Д. (2008). «Обзор безопасности, эффективности и приемлемости для пациентов внутриматочной системы, высвобождающей левоноргестрел». Предпочтения пациентов и приверженность лечению. 2: 293–302. Дои:10.2147 / ppa.s3464. ЧВК 2770406. PMID 19920976.
- ^ Талауликар, VS; Манёнда, ИТ (август 2012 г.). «Улипристала ацетат: новый вариант лечения симптоматической миомы матки». Достижения в терапии. 29 (8): 655–63. Дои:10.1007 / s12325-012-0042-8. PMID 22903240.
- ^ Перес-Лопес, Франция (апрель 2015 г.). "Ulipristal acetate in the management of symptomatic uterine fibroids: facts and pending issues". Климактерический. 18 (2): 177–81. Дои:10.3109/13697137.2014.981133. PMID 25390187.
- ^ Tristan M, Orozco LJ, Steed A, Ramírez-Morera A, Stone P (2012). Orozco LJ (ed.). "Mifepristone for uterine fibroids". Кокрановская база данных систематических обзоров. 8 (8): CD007687. Дои:10.1002/14651858.CD007687.pub2. PMID 22895965.
- ^ Malartic C, Morel O, Akerman G, Tulpin L, Desfeux P, Barranger E (2008). "La mifépristone dans la prise en charge des fibromes utérins". Gynécologie Obstétrique & Fertilité. 36 (6): 668–74. Дои:10.1016/j.gyobfe.2008.01.017. PMID 18539512.
- ^ "The Embolisation Process". FEmISA: Fibroid Embolisation: Information, Support, Advice. В архиве from the original on 2014-05-31.
- ^ а б c Gupta, JK; Sinha, A; Lumsden, MA; Hickey, M (26 December 2014). "Uterine artery embolization for symptomatic uterine fibroids". Кокрановская база данных систематических обзоров. 12: CD005073. Дои:10.1002/14651858.CD005073.pub4. PMID 25541260.
- ^ Homer, Hayden; Saridogan, Ertan (June 2010). "Uterine artery embolization for fibroids is associated with an increased risk of miscarriage". Фертильность и бесплодие (Регулярный обзор). 94 (1): 324–330. Дои:10.1016/j.fertnstert.2009.02.069. PMID 19361799.
- ^ Liu WM, Ng HT, Wu YC, Yen YK, Yuan CC (2001). "Laparoscopic bipolar coagulation of uterine vessels: a new method for treating symptomatic fibroids". Фертильность и бесплодие. 75 (2): 417–22. Дои:10.1016/S0015-0282(00)01724-6. PMID 11172850.
- ^ Akinola OI, Fabamwo AO, Ottun AT, Akinniyi OA (2005). "Uterine artery ligation for management of uterine fibroids". International Journal of Gynaecology and Obstetrics. 91 (2): 137–40. Дои:10.1016/j.ijgo.2005.07.012. PMID 16168993.
- ^ "Uterine Fibroid Embolisation Africa". 2017-02-23.
- ^ Metwally, Mostafa; Raybould, Grace; Cheong, Ying C.; Horne, Andrew W. (29 January 2020). "Surgical treatment of fibroids for subfertility". Кокрановская база данных систематических обзоров. 1: CD003857. Дои:10.1002/14651858.CD003857.pub4. ISSN 1469-493X. ЧВК 6989141. PMID 31995657.
- ^ Agdi M, Tulandi T (August 2008). "Endoscopic management of uterine fibroids". Лучшая практика Res Clin Obstet Gynaecol. 22 (4): 707–16. Дои:10.1016/j.bpobgyn.2008.01.011. PMID 18325839.
- ^ Bhave Chittawar P, Franik S, Pouwer AW, Farquhar C (Oct 21, 2014). "Minimally invasive surgical techniques versus open myomectomy for uterine fibroids". Кокрановская база данных систематических обзоров. 10 (10): CD004638. Дои:10.1002/14651858.CD004638.pub3. PMID 25331441.
- ^ Beck, Melinda (2010-01-20). "A New Treatment to Help Women Avoid Hysterectomy". Журнал "Уолл Стрит.
- ^ "FDA Approves New Device to Treat Uterine Fibroids" (Пресс-релиз). FDA. 2004-10-22. В архиве from the original on 2008-05-09. Получено 2008-05-26.
- ^ Shen SH, Fennessy F, McDannold N, Jolesz F, Tempany C (April 2009). "Image-guided thermal therapy of uterine fibroids". Seminars in Ultrasound, CT, and MR. 30 (2): 91–104. Дои:10.1053/j.sult.2008.12.002. ЧВК 2768544. PMID 19358440.CS1 maint: использует параметр авторов (связь)
- ^ Stewart EA, Rabinovici J, Tempany CM, Inbar Y, Regan L, Gostout B, Gastout B, Hesley G, Kim HS, Hengst S, Gedroyc WM, Gedroye WM (January 2006). "Clinical outcomes of focused ultrasound surgery for the treatment of uterine fibroids". Fertil. Стерил. 85 (1): 22–9. Дои:10.1016/j.fertnstert.2005.04.072. PMID 16412721.
- ^ Kurashvili J, Stepanov A, Kulabuchova E, Batarshina O (2014). "MRgFUS for Uterine Myomas: Safety, Effectiveness and Pathogenesis". Журнал терапевтического ультразвука. 2 (Suppl 1): A1–A25. Дои:10.1186/2050-5736-2-S1-A1. ЧВК 4292016. PMID 25932673.CS1 maint: использует параметр авторов (связь)
- ^ "Helping Black Women Recognize, Treat Fibroids". энергетический ядерный реактор. В архиве из оригинала 22 января 2012 г.. Получено 30 марта 2011.
- ^ "African American Women and Fibroids". Philadelphia Black Women's Health Project. В архиве из оригинала от 1 апреля 2011 г.. Получено 30 марта 2011.
- ^ "Minority Women's Health". Women's Health.gov. Архивировано из оригинал on 2010-08-30.
- ^ а б c "Black Women and High Prevalence of Fibroids". Fibroid Treatment Collective. 29 ноября 2010 г. В архиве из оригинала 25 декабря 2010 г.. Получено 30 марта 2011.
- ^ Office of Budget (PDF)В архиве 2011-09-30 на Wayback Machine[требуется полная цитата]
- ^ Bäcklin BM, Eriksson L, Olovsson M (March 2003). "Histology of uterine leiomyoma and occurrence in relation to reproductive activity in the Baltic gray seal (Halichoerus grypus)". Вет. Патол. 40 (2): 175–80. Дои:10.1354/vp.40-2-175. PMID 12637757.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |
| Викискладе есть медиафайлы по теме Миома матки. |