WikiDer > Серебряный молниеносный
 | |
| Имена | |
|---|---|
| Имена ИЮПАК | |
| Другие имена Серебряный молниеносный Серебро (I) молниеносное Аргентиновый молниеносный | |
| Идентификаторы | |
3D модель (JSmol) | |
| ChemSpider | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| AgCNO | |
| Молярная масса | 149,885 г / моль |
| Плотность | 3,938 г / см3 |
| Взрывоопасные данные | |
| Чувствительность к ударам | Экстремально высокий |
| Чувствительность к трению | Экстремально высокий |
| Опасности | |
| Главный опасности | Чувствительное взрывчатое вещество |
| NFPA 704 (огненный алмаз) | |
| 170 ° С (338 ° F, 443 К) | |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Серебряный молниеносный (AgCNO) очень взрывоопасен серебро поваренная соль из фульминовая кислота.
Серебряный молниеносный первичное взрывчатое вещество, но имеет ограниченное использование как таковое из-за его чрезвычайной чувствительности к ударам, теплу, давлению и электричеству. По мере агрегирования соединение становится все более чувствительным, даже в небольших количествах; прикосновение падения перо, влияние одного воды капелька или маленькая статический разряд все они способны взорвать неограниченную груду гремящего серебра размером не больше копейка и не тяжелее нескольких миллиграммы. Агрегирование больших количеств невозможно из-за тенденции соединения самовзрываться под собственным весом.
Фульминат серебра был впервые получен в 1800 г. Эдвард Чарльз Ховард в своем исследовательском проекте по подготовке большого разнообразия гремит. Вместе с гремучая ртуть, это единственный фульминат, достаточно стабильный для коммерческого использования. Детонаторы с использованием фульмината серебра были использованы для инициирования пикриновая кислота в 1885 году, но с тех пор использовались только итальянским флотом.[3] В настоящее время коммерческое использование направлено на производство новых неповреждающих шумоглушителей в качестве детских игрушек и трюков.
Структура
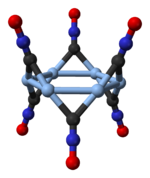
Фульминат серебра встречается в двух полиморфные формы, ромбический один и тригональный с ромбоэдрическая решетка.[4] Тригональный полиморф состоит из циклических гексамеров (AgCNO)6.[5]
Характеристики
Фульминаты очень токсичны, примерно такие же, как цианиды.[3] В чистом виде фульминат серебра химически очень стабилен и не разлагается после многих лет хранения. Как и многие соли серебра, он темнеет на свету. Он слабо растворяется в холодной воде и может быть перекристаллизован в горячей воде.[3][6] Его также можно перекристаллизовать из 20% раствора ацетата аммония.[3] Он не гигроскопичен и может взорваться во влажном состоянии или под водой; Сообщалось, что он оставался взрывоопасным после 37 лет нахождения под водой.[3] Взрывается при контакте с концентрированным серная кислота или хлор или бром, но не при контакте йод.[3] Не растворяется в азотная кислота, но растворяется в аммиак, щелочь хлориды, щелочь цианиды, анилин, пиридин, и йодистый калий образуя комплексы.[3] Концентрированный соляная кислота разлагает его невзрыво с шипящим звуком; тиосульфат также разлагает его без взрыва и может быть использован для утилизации.[3]
Подготовка
Это соединение можно приготовить, заливая раствор нитрат серебра в азотная кислота в этиловый спирт, под тщательным контролем условий реакции, чтобы избежать взрыва.[7] Реакцию обычно проводят при 80-90 ° C; при 30 ° C осадок может не образовываться.[3] За один раз следует приготовить очень небольшое количество фульмината серебра, так как даже вес кристаллов может привести к их самовзрыву. Другой способ получения фульмината серебра - реакция карбонат серебра с аммиак в растворе.[нужна цитата]
Фульминат серебра также образуется, когда газообразный оксид азота пропускают через раствор нитрата серебра в этаноле.[3]
Фульминат серебра может быть получен непреднамеренно, когда кислый раствор нитрат серебра контактирует с алкоголем.[7] Это опасность в некоторых составах химически серебрение зеркала.
Новинка взрывчатка
Гремящее серебро, часто в сочетании с хлорат калия, используется в трюках, создающих шум, известных как "бросок", "крекеры", "снэпперы", "хлыстики", "хлопки" или "хлопки", популярные типы новинок. салют. В них содержится примерно 200 миллиграммов мелкого гравий покрытый незначительным количеством (примерно 80 мкг)[8] серебра молниеносного. При броске о твердую поверхность удара достаточно, чтобы взорвать крошечное количество взрывчатого вещества, создавая небольшой отдать честь от сверхзвуковой детонации. Защелки сконструированы так, чтобы не вызывать повреждений (даже при взрыве по коже) из-за буферного эффекта, обеспечиваемого гораздо большей массой гравийной среды. Это также химическое вещество, содержащееся в Рождественское печенье[9] был впервые использован для этой цели Том Смит в 1860 году. Химикат нарисован на одной из двух узких полосок картона, на второй - абразивом. При вытягивании крекера абразив взрывает фульминат серебра.
Гремучая смесь с 10-20% хлората калия дешевле и дороже. бризантный чем один только молниеносный.[3]
Гремящее серебро и «гремящее серебро»
Фульминат серебра часто путают с нитрид серебра, азид серебра, или же гремящее серебро. «Молниеносное серебро», хотя всегда относится к взрывоопасному серебросодержащему веществу, является неоднозначным термином. Хотя это может быть синоним фульмината серебра, это может также относиться к нитриду или азиду, продукту разложения Реагент Толлена, или алхимический смесь, не содержащая гремучий анион.
Смотрите также
- Первичное взрывчатое вещество
- Юстус фон Либих
- Фридрих Вёлер
- Цианат серебра
- Изомерия
- Молниеносный
- Фульминовая кислота
- Фульминат калия
- Меркурий (II) молниеносный
- Фульминат галлия
Рекомендации
- ^ Международный союз теоретической и прикладной химии (2005). Номенклатура неорганической химии (Рекомендации ИЮПАК 2005 г.). Кембридж (Великобритания): RSC–ИЮПАК. ISBN 0-85404-438-8. п. 291. Электронная версия.
- ^ «Серебряный молниеносный». ChemBase. Получено 8 июн 2012.[постоянная мертвая ссылка]
- ^ а б c d е ж грамм час я j k Матиас, Роберт; Пачман, Иржи (12 марта 2013 г.). Первичные взрывчатые вещества. Springer Science & Business Media, 338 страниц.
- ^ Britton, D .; Дуниц, Дж. Д. (1965). «Кристаллическая структура фульмината серебра». Acta Crystallographica. 19 (4): 662–668. Дои:10.1107 / S0365110X6500405X.
- ^ Бриттон, Д. (1991). «Повторное определение тригональной серебряной фульминатной структуры». Acta Crystallographica C. 47 (12): 2646–2647. Дои:10.1107 / S0108270191008855.
- ^ 0,0075 г при 13 ° C, 0,018 г при 30 ° C и 0,25 г на 100 г H2O при 100 ° C
- ^ а б Collins, P.H .; Холлоуэй, К. Дж. (1978). «Переоценка гремучей серебра как детонатора». Топливо, взрывчатые вещества, пиротехника. 3 (6): 159–162. Дои:10.1002 / преп.19780030603.
- ^ пакетное раскрытие Alexron Co. Ltd, Гонконг, Phantom Brand Bang Snaps, (c) 2013
- ^ "Спектр". "Комментарий №70". Расположение старых заводов фейерверков. Пиротехническое общество Великобритании. Получено 20 декабря 2011.
дальнейшее чтение
- Сингх, К. (1959). «Кристаллическая структура фульмината серебра». Acta Crystallographica. 12 (12): 1053. Дои:10.1107 / S0365110X5900295X.