WikiDer > PEPAP
 | |
| Клинические данные | |
|---|---|
| Другие имена | PEPAP |
| Легальное положение | |
| Легальное положение | |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| Панель управления CompTox (EPA) | |
| Химические и физические данные | |
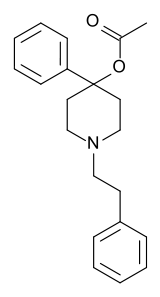
| Формула | C21ЧАС25NО2 |
| Молярная масса | 323.436 г · моль−1 |
| 3D модель (JSmol) | |
| |
| |
| (проверять) | |
PEPAP (фенэтилфенилацетоксипиперидин) является опиоид обезболивающее это аналог из петидин (меперидин).
Это связано с препаратом MPPP, с N-фенэтильная группа вместо N-метил замена и ацетат сложный эфир, а не пропионат. PEPAP примерно в 6-7 раз сильнее морфина у лабораторных крыс.[1] Предположительно, PEPAP имеет аналогичные эффекты с другими опиоидами, вызывая обезболивание, седативный эффект и эйфорию. Побочные эффекты могут включать: зуд, тошнота и потенциально серьезный угнетение дыхания что может быть опасным для жизни.
PEPAP оказался мощным CYP2D6 ингибитор, который может вызывать неблагоприятные взаимодействия с некоторыми другими лекарствами, хотя ингибирующая способность PEPAP меньше, чем у MPPP.[2] И кокаин, и метадон тоже CYP2D6 ингибиторы и теоретически могут усилить эффект.
Маловероятно, что побочные продукты тетрагидропиридина, которые могут образовываться во время синтеза PEPAP, являются нейротоксичными так же, как побочный продукт MPPP. MPTP. Похоже, что N-метильная группа MPTP необходима для нейротоксической активности. В экспериментах на животных только аналоги МФТП, сохранившие N-метил-4-фенил-1,2,3,6-тетрагидропиридин структуры были активны как дофаминергические нейротоксины. Большинство структурных изменений, включая замену N-метильная группа с другими заместителями, устраняет нейротоксичность.[3]
Есть свидетельства того, что подпольные производители, которые производили MPPP в 1970-х годах, включая испорченную партию, продолжали производить PEPAP.[4] в попытке избежать использования наблюдаемых прекурсоров или промежуточных лекарственных препаратов, являющихся незаконными.
Рекомендации
- ^ Янссен П.А., Эдди Н.Б. (февраль 1960 г.). «Соединения, относящиеся к петидину-IV. Новые общехимические методы повышения анальгетической активности петидина». Журнал медицинской и фармацевтической химии. 2: 31–45. Дои:10.1021 / jm50008a003. PMID 14406754.
- ^ Притцкер Д., Канунго А., Киликарслан Т., Тиндейл РФ, Селлерс Е.М. (июнь 2002 г.). «Дизайнерские препараты, которые являются мощными ингибиторами CYP2D6». Журнал клинической психофармакологии. 22 (3): 330–2. Дои:10.1097/00004714-200206000-00015. PMID 12006905. S2CID 492513.
- ^ Юный С.К., Сонсалла П.К., Зибер Б.А., Хейккила Р.Э. (июнь 1989 г.). «Исследование структуры-активности механизма нейротоксичности, вызванной 1-метил-4-фенил-1,2,3,6-тетрагидропиридином (МРТР). I. Оценка биологической активности аналогов МФТП». Журнал фармакологии и экспериментальной терапии. 249 (3): 820–8. PMID 2786564.
- ^ Лэнгстон, Джеймс Уильям; Палфреман, Джон (1995). Дело о замороженных наркоманах. ISBN 0-679-42465-2.