WikiDer > Гексафторид родия - Википедия
 | |
| Имена | |
|---|---|
| Название ИЮПАК фторид родия (VI) | |
| Другие имена гексафторид родия | |
| Идентификаторы | |
3D модель (JSmol) | |
| |
| |
| Характеристики | |
| F6Rh | |
| Молярная масса | 216,91 г / моль |
| Внешность | черное кристаллическое твердое вещество[1] |
| Плотность | 3,71 г / мл[2] |
| Температура плавления | ≈ 70 ° С (158 ° F, 343 К)[1] |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
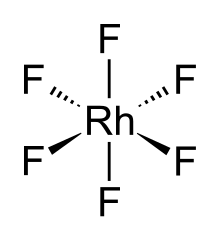
Гексафторид родия, также фторид родия (VI), (RhF6) это неорганическое соединение из родий и фтор. Черное летучее твердое вещество,[1] это высокореактивный материал и редкий пример соединения родия (VI). Это один из семнадцати известных двоичных гексафторид.
Синтез, строение, свойства
Гексафторид родия получают реакцией металлического родия с избытком элементарного фтор:[3]
- Rh + 3 F2 → RhF6
РХФ6 молекула имеет октаэдрическая молекулярная геометрия. В соответствии с его d3 конфигурации шесть Rh – F длина облигаций эквивалентны, составляя 1,824 Å.[2] Он кристаллизуется в ромбический космическая группа ПНМА с параметры решетки из а = 9.323 Å, б = 8,474 Å и c = 4,910 Å.
Как и некоторые другие фториды металлов, RhF6 сильно окисляет. Он атакует даже стекло даже в отсутствие воды.[3] Он может даже реагировать с элементалью кислород.[4]
Рекомендации
- ^ а б c CRC Справочник по химии и физике, 90-е издание, CRC Press, Бока-Ратон, Флорида, 2009 г., ISBN 978-1-4200-9084-0, Раздел 4, Физические константы неорганических соединений, п. 4-85.
- ^ а б Drews, T .; Supeł, J .; Hagenbach, A .; Сеппельт, К. (2006). «Твердотельные молекулярные структуры гексафторидов переходных металлов». Неорганическая химия. 45 (9): 3782–3788. Дои:10.1021 / ic052029f. PMID 16634614.
- ^ а б 《无机 化学 丛书》 第九卷 : 锰 分 族 、 铁 系 、 铂 系 (на китайском языке).北京: 科学 出 Версия社. п. 478. ISBN 7-03-002238-6.
- ^ Ридель, Себастьян; Каупп, Мартин (2009). «Наивысшие степени окисления элементов переходных металлов» (PDF). Обзоры координационной химии. Эльзевир. 253: 606–624. Дои:10.1016 / j.ccr.2008.07.014.[постоянная мертвая ссылка]
дальнейшее чтение
- Gmelins Handbuch der anorganischen Chemie, Система №. 63, Родий, Часть B1, стр. 266–268.