WikiDer > Оксид родия (III)
 | |
| Идентификаторы | |
|---|---|
3D модель (JSmol) | |
| ECHA InfoCard | 100.031.666 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| Rh2О3 | |
| Молярная масса | 253,8092 г / моль |
| Внешность | темно-серый порошок без запаха |
| Плотность | 8,20 г / см3 |
| Температура плавления | 1100 ° С (2,010 ° F, 1370 К) (разлагается) |
| нерастворимый | |
| Растворимость | не растворим в царская водка |
| +104.0·10−6 см3/ моль | |
| Структура | |
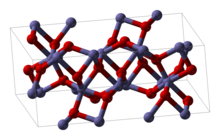
| шестиугольник (корунд) | |
| Опасности | |
Классификация ЕС (DSD) (устарело) | нет в списке |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Оксид родия (III) (или же Полуторный оксид родия) это неорганическое соединение с формулой Rh2О3. Это серое твердое вещество, не растворимое в обычных растворителях.
Структура
Rh2О3 был обнаружен в двух основных формах. Гексагональная форма принимает корунд структура. Он превращается в ромбический структура при нагревании выше 750 ° C.[1]
Производство
Оксид родия можно производить несколькими способами:
- Лечение RhCl3 кислородом при высоких температурах.[2]
- Металлический порошок Rh сплавлен с гидросульфат калия. Добавление едкий натр приводит к гидратированный оксид родия, который при нагревании превращается в Rh2О3.[3]
- Оксид родия тонкие пленки может быть получен путем воздействия на слой Rh кислородной плазмы.[4]
- Наночастицы может быть произведено гидротермальный синтез.[5]
Физические свойства
Пленки оксида родия ведут себя как быстрая двухцветная пленка. электрохромный система: Обратимые изменения цвета желтый, темно-зеленый или желтый, коричнево-фиолетовый цвета получаются в КОН растворов подачей напряжения ~ 1 V.[6]
Пленки оксида родия прозрачные и проводящие, как и оксид индия и олова (ITO) - электрод обычный прозрачный, но Rh2О3 на 0,2 эВ ниже рабочая функция чем ИТО. Следовательно, нанесение оксида родия на ITO улучшает инжекцию носителя из ITO, тем самым улучшая электрические свойства органические светодиоды.[4]
Каталитические свойства
Оксиды родия катализаторы за гидроформилирование алкенов,[7] N2О производство из НЕТ,[8] и гидрирование из CO.[9]
Смотрите также
Рекомендации
- ^ Коуи, Дж. М. Д. (1970-11-01). «Кристаллическая структура Rh2О3". Acta Crystallographica Раздел B Структурная кристаллография и кристаллохимия. Международный союз кристаллографии (IUCr). 26 (11): 1876–1877. Дои:10.1107 / s0567740870005022. ISSN 0567-7408.
- ^ Х. Л. Грубе (1963). «Платиновые металлы». В Г. Брауэре (ред.). Справочник по препаративной неорганической химии, 2-е изд.. Нью-Йорк: Academic Press. п. 1588.
- ^ Уолд, Аарон; Арнотт, Рональд Дж .; Крофт, Уильям Дж. (1963). «Взаимодействие оксидов редкоземельных элементов с высокотемпературной формой оксида родия (III)». Неорганическая химия. Американское химическое общество (ACS). 2 (5): 972–974. Дои:10.1021 / ic50009a023. ISSN 0020-1669.
- ^ а б Ким, Су Ён; Байк, Чон Мин; Ю, Хак Ки; Ким, Кван Ён; Так, Юн-Хын; Ли, Чон-Лам (2005-08-15). «Оксид индия и олова с покрытием из оксида родия для улучшения инжекции дырок в органических светоизлучающих диодах». Письма по прикладной физике. Издательство AIP. 87 (7): 072105. Bibcode:2005АпФЛ..87г2105К. Дои:10.1063/1.2012534. ISSN 0003-6951.
- ^ Mulukutla, Ravichandra S .; Асакура, Киётака; Когуре, Тошихиро; Намба, Сейтаро; Ивасава, Ясухиро (1999). «Синтез и характеристика наночастиц оксида родия в мезопористом MCM-41». Физическая химия Химическая физика. Королевское химическое общество (RSC). 1 (8): 2027–2032. Bibcode:1999PCCP .... 1.2027M. Дои:10.1039 / a900588i. ISSN 1463-9076.
- ^ Готтесфельд, С. (1980). "Анодная пленка оксида родия: двухцветная электрохромная система". Журнал Электрохимического общества. Электрохимическое общество. 127 (2): 272. Дои:10.1149/1.2129654. ISSN 0013-4651.
- ^ Пино, П .; Боттехи, К. (1977). «Альдегиды из олефинов: циклогексанкарбоксальдегид». Органический синтез. 57: 11. Дои:10.15227 / orgsyn.057.0011.
- ^ Мулукутла, Равичандра С. Шидо, Такафуми; Асакура, Киётака; Когуре, Тошихиро; Ивасава, Ясухиро (2002). «Характеристика наночастиц оксида родия в MCM-41 и их каталитических свойств для реакций NO – CO при избытке O2". Прикладной катализ A: Общие. Elsevier BV. 228 (1–2): 305–314. Дои:10.1016 / s0926-860x (01) 00992-9. ISSN 0926-860X.
- ^ Watson, P; Соморжай, Г. А. (1981). «Гидрирование оксида углерода на поверхностях из оксида родия». Журнал катализа. Elsevier BV. 72 (2): 347–363. Дои:10.1016 / 0021-9517 (81) 90018-х. ISSN 0021-9517.