WikiDer > Бета-гидроксибета-метилмасляная кислота
 | |
 Верх: β-гидрокси β-метилмасляная кислота Внизу: β-гидрокси β-метилбутират | |
| Клинические данные | |
|---|---|
| Другие имена | Конъюгированная кислота форма: β-гидроксиизовалериановая кислота 3-гидроксиизовалериановая кислота Основание конъюгата форма: гидроксиметилбутират |
| Маршруты администрация | Устно[1] или назогастральный[2] |
| Код УВД |
|
| Легальное положение | |
| Легальное положение |
|
| Фармакокинетический данные | |
| Метаболиты | HMB-CoA, HMG-CoA, мевалонат, холестерин, ацетил-КоА, ацетоацетат, β-гидроксибутират |
| Начало действия | HMB-FA: 30–60 минут[1] HMB-Ca: 1-2 часа[1] |
| Устранение период полураспада | HMB-FA: 3 часа[1] HMB-Ca: 2,5 часа[1] |
| Экскреция | Почечный (10-40% выводится из организма)[1][3] |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.128.078 |
| Химические и физические данные | |
| Формула | C5ЧАС10О3 |
| Молярная масса | 118.132 г · моль−1 |
| 3D модель (JSmol) | |
| Плотность | ~ 1,1 г / см3 при 20 ° C[4] |
| Температура плавления | −80 ° C (−112 ° F) (стекло)[5] |
| Точка кипения | 128 ° C (262 ° F) при 7мм рт. ст.[4][6] |
| |
| |
| (проверить) | |
β-гидрокси β-метилмасляная кислота[примечание 1] (HMB), иначе известный как его сопряженное основание, β-гидрокси β-метилбутират, это естественно произведенный вещество в организме человека, которое используется в качестве пищевая добавка и как ингредиент в некоторых лечебные продукты которые предназначены для продвижения лечение раны и обеспечить питательную поддержку людям с атрофия мышц из-за рак или ВИЧ / СПИД.[источники 1] Было показано, что у здоровых взрослых добавление HMB увеличивает вызванный физическими упражнениями прирост мышца размер, мышечная сила и мышечная масса тела, уменьшать скелетные мышцы повреждение от упражнений, улучшение результатов аэробных упражнений и ускорение восстановления после упражнений.[источники 2] Медицинские обзоры и метаанализ указывают на то, что добавление HMB также помогает сохранить или увеличить мышечную массу и мышечную силу у людей, возрастная потеря мышечной массы.[заметка 2][11][12][13] HMB производит эти эффекты частично за счет стимуляции производство белков и подавление расщепление белков в мышечной ткани.[11][14][15] Нет побочные эффекты от длительного использования в качестве пищевой добавки у взрослых.[16][17][18]
HMB продается как пищевая добавка по цене около АМЕРИКАНСКИЙ ДОЛЛАР$30–50 в месяц при приеме 3 г в день.[16][19][20] HMB также содержится в нескольких пищевых продуктах, включая определенные составы Гарантировать, Ювен, и Миоплекс.[8][21] HMB также присутствует в незначительных количествах в некоторых продуктах питания, таких как люцерна, спаржа, авокадо, цветная капуста, грейпфрут, и сом.[22][23]
Воздействие HMB на скелетные мышцы человека было впервые обнаружено Стивеном Л. Ниссеном в Государственный университет Айовы в середина 1990-х.[8][24] По состоянию на 2018 год[Обновить] ИСБ не был запрещен Национальная студенческая спортивная ассоциация, Всемирное антидопинговое агентство, или любой другой известной национальной или международной спортивной организацией.[25][26][27] В 2006 г. только около 2% колледжей студенты-спортсмены в США использовали HMB в качестве пищевой добавки.[19][28] По состоянию на 2017 год HMB нашел широкое применение в качестве эргогенная добавка среди юных спортсменов.[29]
Использует
Доступные формы
HMB продается как без рецепта пищевая добавка в свободная кислота форма, β-гидрокси β-метилмасляная кислота (HMB-FA), и как моногидратированный кальций поваренная соль из сопряженное основание, кальций β-гидрокси β-метилбутират моногидрат (HMB-Ca, CaHMB).[19][20] Поскольку только небольшая часть метаболического предшественника HMB, L-лейцин, метаболизируется в HMB, фармакологически активные концентрации соединения в плазма крови а мышечная масса может быть достигнута только путем прямого приема HMB.[1][30][31] Здоровый взрослый человек производит примерно 0,3 грамма в день, тогда как добавки HMB обычно принимаются в дозах 3–6 грамм в сутки.[17] HMB продается по цене около АМЕРИКАНСКИЙ ДОЛЛАР$30–50 в месяц при приеме по 3 грамма в день.[16] HMB также содержится в нескольких пищевых продуктах и пищевых продуктах медицинского назначения, продаваемых Abbott Laboratories (например, некоторые составы Гарантировать, Ювен, и Миоплекс),[8][21] и присутствует в незначительных количествах в некоторых продуктах питания, таких как люцерна, спаржа, авокадо, цветная капуста, грейпфрут, и сом.[22][23]
Медицинское
Дополнительный HMB был использован в клинические испытания как средство для сохранения мышечной массы при истощении мышц, особенно саркопения, и был изучен в клинических испытаниях как дополнительная терапия в сочетании с упражнения на сопротивление.[11][16][30] На основании двух медицинских обзоров и метаанализ из семи рандомизированные контролируемые испытания, Добавка HMB может сохранить или увеличить мышечную массу и мышечную силу в саркопенический пожилые люди.[заметка 2][11][12][13] HMB не оказывает значительного влияния на жировую массу у пожилых людей.[11][12] Предварительные клинические данные свидетельствуют о том, что добавление HMB также может предотвратить мышечная атрофия в течение постельный режим.[11][29] Растущее количество доказательств подтверждает эффективность HMB в качестве нутритивной поддержки для уменьшения или даже обращения вспять потери мышечной массы. функция мышц, и мышечная сила что происходит в гиперкатаболический болезненные состояния, такие как рак кахексия;[16][30][32] следовательно, авторы двух обзоров клинических данных 2016 г. рекомендовали, чтобы профилактика и лечение саркопении и мышечной атрофии в целом включала добавление HMB, регулярные упражнения с отягощениями и потребление высокобелковая диета.[16][30]
Клинические испытания HMB для лечения мышечной атрофии включали введение 3 граммов HMB в день при различных режимах дозирования.[16] Согласно одному обзору, оптимальным режимом дозирования является введение его в виде одной дозы в 1 грамм три раза в день, поскольку это обеспечивает повышенные концентрации HMB в плазме в течение дня;[16] однако по состоянию на июнь 2016 г.[Обновить] лучший режим дозирования при истощении мышц все еще исследуется.[30]
Некоторые фирменные продукты, содержащие HMB (например, определенные составы Ensure и Juven), являются лечебные продукты которые предназначены для использования в качестве нутритивной поддержки под наблюдением врача у лиц с атрофия мышц из-за ВИЧ / СПИД или рак, продвигать лечение раны после операции или травмы, или по иным рекомендациям медицинского работника.[источники 3] Juven, пищевой продукт, содержащий 3 грамма HMB-Ca, 14 грамм L-аргинин, и 14 граммов L-глютамин на две порции,[2] было показано улучшение мышечная масса тела во время клинических испытаний на людях со СПИДом и раком, но не ревматоидная кахексия.[17][33][34] Дальнейшие исследования, включающие лечение кахексии рака с помощью Juven в течение нескольких месяцев, необходимы для адекватного определения эффективности лечения.[17][33]
Повышение производительности

Было показано, что при соответствующей программе упражнений диетические добавки с 3 граммами HMB в день увеличивают вызванный физическими упражнениями прирост мышечной массы, мышечной силы и мощности, а также мышечной массы, уменьшают вызванное физическими упражнениями повреждение скелетных мышц,[заметка 3] и ускорить восстановление после упражнений высокой интенсивности.[источники 2] Основываясь на ограниченных клинических исследованиях, добавка HMB может также улучшить производительность аэробных упражнений и увеличить прирост аэробный фитнес в сочетании с высокоинтенсивная интервальная тренировка.[12][14] Эти эффекты HMB более выражены у нетренированных людей и спортсменов, которые выполняют упражнения с отягощениями высокой интенсивности или аэробные упражнения.[1][12][14] У людей, тренирующихся с отягощениями, влияние HMB на мышечную силу и безжировую массу тела ограничено.[37] HMB влияет на размер, силу, массу, мощность и восстановление мышц, частично за счет стимуляции. миофибрилла мышца синтез белка и подавление мышц распад белка через различные механизмы, включая активацию механистическая мишень комплекса рапамицина 1 (mTORC1) и ингибирование протеасома-опосредованный протеолиз в скелетных мышцах.[14][15]
Эффективность добавок HMB для уменьшения повреждения скелетных мышц в результате длительных или высокоинтенсивных упражнений зависит от времени, в течение которого они используются по сравнению с упражнениями.[1][36] Было показано, что наибольшее снижение повреждения скелетных мышц от одного упражнения происходит, когда HMB-Ca проглочен 1–2 часов до тренировки или HMB-FA проглочен 30–60 минут до тренировки.[1]
В 2006 г. только около 2% колледжей студенты-спортсмены в США использовали HMB в качестве пищевой добавки.[19][28] По состоянию на 2017 год HMB нашел широкое применение в качестве эргогенная добавка среди спортсменов.[29] По состоянию на 2018 год[Обновить] ИСБ не был запрещен Национальная студенческая спортивная ассоциация, Всемирное антидопинговое агентство, или любой другой известной национальной или международной спортивной организацией.[25][26][27]
Побочные эффекты
В профиль безопасности HMB у взрослых людей основано на данных клинические испытания у людей и исследования на животных.[16][18] У людей нет побочные эффекты у молодых людей и пожилых людей сообщалось, когда HMB принимается в дозах 3 грамма в день в течение года.[16][17][18] Исследования молодых людей, принимающих 6 граммов HMB в день в течение до 2 месяцев, также не показали никаких побочных эффектов.[17][18] Исследования с добавлением HMB на молодых растущих крысах и домашнем скоте не выявили побочных эффектов, основанных на клиническая химия или наблюдаемые характеристики;[1][23] для людей моложе 18 лет данные о безопасности добавок HMB ограничены.[1] В эквивалентная доза для человека ИСБ для уровень отсутствия наблюдаемых побочных эффектов (NOAEL), который был идентифицирован на модели крыс, составляет примерно 0,4 г / кг масса тела в день.[примечание 4][18][23]
В двух исследованиях на животных изучали влияние добавок HMB беременным свиньям на потомство и не сообщали об отрицательном воздействии на плод.[23] Никаких клинических испытаний с добавлением HMB на беременных женщинах не проводилось.[38] беременным и кормящим женщинам не рекомендуется принимать HMB Metabolic Technologies, Inc., компания, которая предоставляет лицензии на включение HMB в пищевые добавки из-за отсутствия исследований безопасности.[38]
Фармакология
• PA: фосфатидная кислота
• mTOR: механистическая мишень рапамицина
• AMP: аденозинмонофосфат
• ATP: аденозинтрифосфат
• АМПК: АМФ-активированная протеинкиназа
• PGC ‐ 1α: гамма-коактиватор рецептора, активируемого пролифератором пероксисом,-1α
• S6K1: p70S6 киназа
• 4EBP1: фактор инициации трансляции эукариот 4E-связывающий белок 1
• eIF4E: фактор инициации трансляции эукариот 4E
• RPS6: рибосомальный белок S6
• eEF2: фактор элонгации эукариот 2
• RE: упражнения на сопротивление; EE: упражнения на выносливость
• Мио: миофибрилла; Мито: митохондриальный
• AA: аминокислоты
• HMB: β-гидрокси β-метилмасляная кислота.
• ↑ означает активацию
• Τ означает запрет
Фармакодинамика
Несколько компонентов сигнальный каскад который опосредует индуцированное HMB увеличение синтеза белка скелетных мышц человека. in vivo.[14][15] Похоже на HMB метаболический предшественник, L-лейцин, HMB увеличивает синтез белка в скелетных мышцах человека посредством фосфорилирование из механистическая мишень рапамицина (mTOR) и последующая активация mTORC1, что приводит к биосинтез белка в сотовой рибосомы через фосфорилирование ближайших мишеней mTORC1 (т. е. p70S6 киназа и перевод белок-репрессор 4EBP1).[примечание 5][15][39][41] Было показано, что добавление HMB к нескольким видам животных, кроме человека, увеличивает сыворотка концентрация гормон роста и инсулиноподобный фактор роста 1 (IGF-1) по неизвестному механизму, что, в свою очередь, способствует синтезу белка за счет увеличения фосфорилирования mTOR.[1][16][23] Основываясь на ограниченных клинических данных у людей, дополнительный HMB увеличивает секрецию гормона роста и IGF-1 в ответ на упражнения с отягощениями.[14]
По состоянию на май 2016 г.[Обновить], сигнальный каскад, который опосредует индуцированное HMB снижение распада мышечного белка, не был идентифицирован у живых людей, хотя хорошо известно, что он ослабляет протеолиз в людях in vivo.[11][15] в отличие L-лейцин, HMB снижает распад мышечного белка в инсулин-независимо у человека.[примечание 6][15] Считается, что HMB снижает распад мышечного белка у людей, ингибируя 19S и 20S подразделения убиквитин-протеасомная система в скелетных мышцах и подавляя апоптоз из ядра скелетных мышц через неопознанные механизмы.[15][16][41]
На основании исследований на животных, HMB метаболизируется в скелетных мышцах в холестерин, который затем может быть включен в мембрана мышечной клетки, тем самым улучшая целостность и функцию мембраны.[34][35] Воздействие HMB на мышцы белковый обмен может помочь стабилизировать структуру мышечных клеток.[23] В одном обзоре было высказано предположение, что наблюдаемое индуцированное HMB снижение концентрации мышечного повреждения в плазме крови биомаркеры (т.е. мышечные ферменты, такие как креатинкиназа и лактатдегидрогеназа) у людей после интенсивных упражнений может быть связано с опосредованным холестерином улучшением функции мембран мышечных клеток.[заметка 3][23]
Было показано, что HMB стимулирует распространение, дифференциация, и слияние человека миоспателлитные клетки in vitro, который потенциально увеличивает регенеративную способность скелетных мышц за счет увеличения экспрессии белков определенных миогенные регуляторные факторы (например., myoD и миогенин) и ген факторы транскрипции (например., MEF2).[1][17][42] HMB-индуцированная пролиферация миоспателлитных клеток человека in vitro опосредуется через фосфорилирование митоген-активированные протеинкиназы ERK1 и ERK2.[17][23][42] HMB-индуцированная дифференцировка миосателлитов человека и ускоренное слияние миосателлитных клеток с мышечной тканью in vitro опосредуется через фосфорилирование Акт, а серин / треонин-специфическая протеинкиназа.[17][23][42]
Фармакокинетика

Свободная кислота (HMB-FA) и моногидратированная соль кальция (HMB-Ca) формы HMB имеют разные фармакокинетика.[1][20] HMB-FA легче всасывается в кровоток и дольше период полувыведения (3 часа) относительно HMB-Ca (2,5 часа).[1][20] Поглощение тканями и утилизация HMB-FA 25–40% выше, чем для HMB-Ca.[1][20] Доля проглоченной дозы, которая выводится с мочой, не различается между двумя формами.[1]
После приема внутрь HMB-Ca конвертируется в β-гидрокси β-метилбутират следующий диссоциация кальция часть в кишечнике.[1] Когда HMB-Ca лекарственная форма При проглатывании, величина и время, при котором наблюдается пиковая концентрация HMB в плазме, зависят от дозы и одновременного приема пищи.[1] Более высокие дозы HMB-Ca увеличивают скорость поглощение, что приводит к пиковому уровню HMB в плазме (CМаксимум), что непропорционально больше, чем ожидалось от линейного доза-реакция и что происходит раньше по сравнению с более низкими дозами.[примечание 7][1] Потребление HMB-Ca с сахаросодержащими веществами снижает скорость абсорбции HMB, что приводит к более низкому пиковому уровню HMB в плазме, который возникает позже.[примечание 7][1]
HMB выводится через почки, с примерно 10–40% проглоченной дозы выводится в неизмененном виде с мочой.[1][3] Остальные 60–90% дозы остается в тканях или выводится в виде метаболитов HMB.[1][3] Фракция данной дозы HMB, которая выводится в неизмененном виде с мочой, увеличивается с увеличением дозы.[примечание 8][1]
Метаболизм
Биосинтез и метаболизм β-гидрокси β-метилбутирата у человека |
Метаболизм HMB катализируется неизвестным ферментом, который превращает его в β-гидрокси β-метилбутирил-КоА (HMB-CoA).[43][45] HMB-CoA метаболизируется либо еноил-КоА гидратаза или другой не охарактеризованный фермент, производящий β-метилкротонил-КоА (MC-CoA) или гидроксиметилглутарил-КоА (HMG-CoA) соответственно.[3][45] MC-CoA затем превращается ферментом метилкротонил-КоА карбоксилаза к метилглутаконил-КоА (MG-CoA), который впоследствии преобразуется в HMG-CoA от метилглутаконил-КоА гидратаза.[3][45][46] HMG-CoA затем раскалывается на ацетил-КоА и ацетоацетат от HMG-CoA лиазе или используется в производстве холестерина через мевалонатный путь.[3][45]
Биосинтез
HMB синтезируется в организме человека через метаболизм из L-лейцин, а аминокислота с разветвленной цепью.[45] У здоровых людей примерно 60% диетического L-лейцин метаболизируется через несколько часов, примерно 5% (2–10% ассортимент) диетических L-лейцин конвертируется в HMB.[3][16][45]
Подавляющее большинство L-лейцин метаболизм изначально катализируется аминотрансфераза аминокислот с разветвленной цепью фермент, производящий α-кетоизокапроат (α-KIC).[3][45] α-KIC в основном метаболизируется митохондриальный фермент разветвленная цепь α-кетокислота дегидрогеназа, который преобразует его в изовалерил-КоА.[3][45] Изовалерил-КоА впоследствии метаболизируется изовалерил-КоА дегидрогеназа и преобразован в MC-CoA, который используется в синтезе ацетил-КоА и других соединений.[45] В течение дефицит биотина, HMB можно синтезировать из MC-CoA через еноил-КоА гидратаза и неизвестный тиоэстераза фермент[43][44][47] которые конвертируют MC-CoA в HMB-CoA и HMB-CoA в HMB соответственно.[44] Относительно небольшое количество α-KIC метаболизируется в печень посредством цитозольный фермент 4-гидроксифенилпируват диоксигеназа (KIC-диоксигеназа), которая превращает α-KIC в HMB.[3][45][48] У здоровых людей этот второстепенный путь, который включает превращение L-лейцин в α-KIC, а затем на HMB - это преобладающий путь синтеза HMB.[3][45]
Химия
β-гидрокси β-метилмасляная кислота - это монокарбоновый β-гидроксикислота и натуральный продукт с молекулярная формула C5ЧАС10О3.[49][50] При комнатной температуре чистый β-гидрокси β-метилмасляная кислота представляет собой прозрачную жидкость от бесцветного до светло-желтого цвета, растворимую в воде.[6][51][52] β-гидрокси β-метилмасляная кислота - это слабая кислота с пKа из 4.4.[5] это показатель преломления () составляет 1,42.[5]
Химическая структура
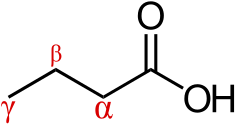
β-гидрокси β-метилмасляная кислота является членом карбоновая кислота семья органические соединения.[49] Это структурный аналог из Масляная кислота с гидроксил функциональная группа и метил заместитель расположен на его бета-углерод.[49][53] В дополнение к другим структурным аналогам относятся: β-гидроксимасляная кислота и β-метилмасляная кислота.[49][53]
Синтез
Разнообразные синтетические пути к β-гидрокси β-метилмасляная кислоты были разработаны. Первый сообщил химический синтез приблизился к HMB путем окисления алкен, вицинальный диол, и алкоголь предшественники:
- в 1877 г. русские химики Михаил и Александр Зайцев сообщили о получении HMB путем окисления 2-метилпент-4-ен-2-ола с хромовая кислота (ЧАС2CrO4);[54]
- в 1880 и 1889 годах Щироков и Реформатский (соответственно) сообщили, что окислительное расщепление вицинального диола 4-метилпентан-1,2,4-триола подкисленным перманганат калия (KMnO4) дает HMB[55][56] - этот результат наиболее близок к первому синтезу, так как холодный разбавленный KMnO4 окисляет алкены до вицинала СНГ-диолы горячей кислоты KMnO4 далее окисляется до карбонилсодержащих соединений, и промежуточное соединение диола не получается, когда горячие кислотные условия используются для окисление алкена.[57] Другими словами, рацемический 4-метилпентан-1,2,4-триол представляет собой производная 2-метилпент-4-ен-2-ола и β-гидрокси β-метилмасляная кислота является производным обоих; и,
- в 1892 г. Кондаков сообщил о получении HMB перманганатным окислением 3-метилбутан-1,3-диола.[58]
В зависимости от условий эксперимента, циклоприсоединение из ацетон и кетен производит либо β-изовалеролактон или 4,4-диметилоксетан-2-он,[59][60] оба из которых гидролизовать в основных условиях для получения конъюгированного основания HMB. В галоформная реакция обеспечивает другой путь к HMB, включающий полное галогенирование метилкетоновой области диацетоновый спирт с участием гипобромит натрия или гипохлорит натрия;[5][61][62] Диацетоновый спирт легко приобрести в альдольная конденсация ацетона.[61] An металлоорганический подход к ИСБ предполагает карбоксилирование из терт-бутиловый спирт с участием монооксид углерода и Реактив Фентона (пероксид водорода и двухвалентное железо).[5][63] В качестве альтернативы HMB можно получить через микробное окисление из β-метилмасляная кислота грибком Galactomyces reessii.[64]
Обнаружение в биологических жидкостях
| Биожидкость | Возрастная группа | Концентрация | Источники | ||
|---|---|---|---|---|---|
| Значить | Ассортимент | Единицы | |||
| Плазма крови | Взрослые (18+) | 4.0 | 0–10.0 | мкМ | [49] |
| CSF | Взрослые (18+) | 4.0 | 2.0–6.0 | мкМ | [49] |
| Саркоплазма | Взрослые (21–23) | 7.0 | 4.0–10.0 | мкМ | [15] |
| Грудное молоко | Взрослые (18+) | – | 42–164 | мкг / л | [65] |
| Моча | Взрослые (18+) | – | 3.2–25.0 | мкмоль / ммоль креатинин | [49] |
| Моча | Дети (1–18) | – | 0–68 | мкмоль / ммоль креатинина | [49] |
Концентрация вырабатываемого естественным путем HMB была измерена у нескольких человек. телесные жидкости с помощью спектроскопия ядерного магнитного резонанса, жидкостная хроматография – масс-спектрометрия, и газовая хроматография – масс-спектрометрия методы.[65][49] В плазме крови и спинномозговая жидкость (CSF) здоровых взрослых, средний молярная концентрация HMB был измерен на уровне 4,0микромолярный (мкМ).[49] Средняя концентрация HMB в внутримышечная жидкость здоровых мужчин в возрасте 21–23 был измерен при 7,0 мкМ.[15] В моче здоровых людей любого возраста концентрация HMB, выделяемая с мочой, измерялась в диапазоне от 0–68 микромоли на миллимоль (мкмоль / ммоль) креатинин.[49] В грудном молоке здоровых кормящих женщин HMB и L-лейцин были измерены в диапазоне 42–164 мкг / л и 2.1–88.5 мг / л.[65] Для сравнения, HMB был обнаружен и измерен в молоке здоровых коров при концентрации <20–29 мкг / л.[66] Эта концентрация слишком низка, чтобы быть адекватным диетическим источником HMB для получения фармакологически активных концентраций соединения в плазме крови.[66]
В исследовании, в котором участники потребляли 2,42 грамма чистого HMB-FA при голодании средняя концентрация HMB в плазме увеличивалась с базального уровня 5,1мкМ до 408 мкМ через 30 минут.[15] Через 150 минут после приема пищи средняя концентрация HMB в плазме среди участников составляла 275 мкМ.[15]
Аномальные концентрации HMB в моче и плазме крови были отмечены при нескольких болезненных состояниях, где они могут служить причиной диагностический биомаркер, особенно в случае метаболические нарушения.[49] В следующей таблице перечислены некоторые из этих заболеваний вместе с соответствующими концентрациями HMB, обнаруженными в моче или плазме крови.[49]
| Состояние здоровья | Биожидкость | Возрастная группа | Концентрация | Источники | ||
|---|---|---|---|---|---|---|
| Значить | Ассортимент | Единицы | ||||
| Дефицит биотинидазы† | Кровь | Взрослые (18+) | 9.5 | 0–19.0 | мкМ | [49] |
| Дефицит биотинидазы† | Кровь | Дети (1–13) | 88.0 | 10.0–166.0 | мкМ | [49] |
| Дефицит биотинидазы† | Моча | Дети (1–13) | 275.0 | 50.0–500.0 | мкмоль / ммоль креатинин | [49] |
| 3-метилглутаконовая ацидурия (тип I)† | Моча | Дети (1–13) | 200.0 | 150.0–250.0 | мкмоль / ммоль креатинина | [49] |
| Эозинофильный эзофагит | Моча | Дети (1–13) | 247.4 | 0–699.4 | мкмоль / ммоль креатинина | [49] |
| Гастроэзофагеальная рефлюксная болезнь | Моча | Дети (1–13) | 119.8 | 5.5–234.0 | мкмоль / ммоль креатинина | [49] |
| Дефицит лиазы HMG-CoA† | Моча | Дети (1–13) | 2030.0 | 60.0–4000.0 | мкмоль / ммоль креатинина | [49] |
| Дефицит MC-CoA карбоксилазы† | Моча | Дети (1–13) | 30350.0 | 1700.0–59000.0 | мкмоль / ммоль креатинина | [49] |
| А † указывает на то, что состояние здоровья нарушение обмена веществ. | ||||||
История
Первый сообщил химический синтез HMB был опубликован в 1877 году русскими химиками Михаилом и Александр Зайцев.[54] HMB был выделен из коры Erythrophleum couminga (мадагаскарское дерево) в 1941 г. Леопольд Ружичка.[67] Самые ранние сообщения о выделении HMB у человека метаболит был получен Танакой и его коллегами в 1968 году от пациента с изовалериановая ацидемия.[68][69]
Воздействие HMB на скелетные мышцы человека было впервые обнаружено Стивеном Л. Ниссеном в Государственный университет Айовы в середина 1990-х.[8][24] Ниссен основал компанию под названием Metabolic Technologies, Inc. (MTI) примерно во время его открытия, которое позже приобрело шесть связанных с HMB патенты которые компания использовала для получения лицензии на производство и включение HMB в пищевые добавки.[24][70][71] Когда он впервые стал коммерчески доступным в конце 1990-х, HMB продавался исключительно как спортивная добавка, помогающая спортсменам и бодибилдерам наращивать мышцы.[70] Впоследствии MTI разработала два продукта, содержащие HMB, Juven и Revigor, для которых Эбботт Нутришн получили рыночные права в 2003 и 2008 годах соответственно.[8][70] С тех пор Abbott продает Juven как лечебное питание, а торговую марку HMB Revigor - как активный ингредиент в пищевых продуктах для спортсменов (например, определенные составы Myoplex) и другие продукты медицинского назначения (например, определенные составы Ensure).[8][21][70]
Заметки
- ^ Синонимы и варианты написания включают: бета-гидрокси бета-метилмасляная кислота, 3-гидрокси-3-метилбутановая кислота кислота (ИЮПАК имя), 3-гидроксиизовалериановая кислота, и бета-гидроксиизовалериановая кислота.[7]
- ^ а б Мета-анализ показал, что средний прирост мышечной массы из-за приема HMB у пожилых людей составил 0,35 кг (0,77 фунта).[11] В 95% доверительный интервал для предполагаемого увеличения мышечной массы за счет добавок HMB составляет 0,11–0,59 кг (0,24–1,30 фунта).[11]
В семи рандомизированных контролируемых испытаниях, включенных в метаанализ, в HMB принимали участие 147 пожилых людей. лечебные группы и 140 пожилых людей в контрольные группы.[11] Семь испытаний имели продолжительность от 2 до 11 месяцев и среднюю продолжительность исследований. взвешенные по размеру их выборки, было примерно 6 месяцев.[11] - ^ а б Влияние HMB на повреждение скелетных мышц было оценено в исследованиях на людях с использованием четырех различных биомаркеры повреждения мышц или распада белка: сыворотка креатинкиназа, сыворотка лактатдегидрогеназа, мочевой азот мочевины, и мочевой 3-метилгистидин.[1][19][35] Когда интенсивность и объем упражнений достаточны для повреждения скелетных мышц, например, во время бег на длинные дистанции или прогрессирующая перегрузка, Добавка HMB снижает рост этих биомаркеров на 20–60%.[1][19][36]
- ^ NOAEL был установлен на основе 3-месячного исследования с участием нескольких групп Крысы Sprague-Dawley которые вводили разные суточные дозы HMB-FA.[18][23] Никаких побочных эффектов не наблюдалось ни в одной группе, получавшей HMB, поэтому самая высокая суточная доза HMB, которая вводилась в этом исследовании, была определена как NOAEL.[18][23]
- ^ Примерно равные дозы чистого HMB-FA (2,42 грамма) и L-лейцин (3,42 грамма) не вызывают статистически различимых анаболических эффектов, измеренных с помощью фракционный синтез из миофибриллярные белки, в скелетных мышцах живых людей.[15][40] Через 150 минут после приема эти дозы HMB-FA и L-лейцин увеличение синтеза мышечного протеина на ~ 70% и ~ 110% соответственно в одном исследовании.[15][40]
- ^ Через 150 минут после приема внутрь доза 2,42 грамма чистого HMB-FA снизил распад белка скелетных мышц у живых людей на 57% в одном исследовании.[15][40] Эффект L-лейцин распад мышечного белка полностью зависит от инсулин секрецию и, следовательно, не измеряли в одном исследовании.[15] Для сравнения, инсулинозависимое снижение расщепления мышечного белка после приема всей еды, содержащей L-лейцин а углеводы составляют в среднем ~ 50%.[15]
- ^ а б В одном исследовании прием 1 грамма HMB-Ca здоровыми добровольцами приводил к пиковому уровню HMB в плазме, равному 120.мкМ через 2 часа после приема внутрь, в то время как прием 3 граммов HMB-Ca дает пиковый уровень HMB в плазме 487 мкМ через 1 час после приема.[1]
Потребление 3 граммов HMB-Ca с 75 граммами глюкоза привел к более низкому пиковому уровню HMB в плазме 352 мкМ, который наблюдался спустя 2 часа после приема внутрь.[1] - ^ В одном исследовании прием внутрь 1 грамма и 3 грамма HMB приводил к выведению 14% и 28% дозы в виде HMB с мочой, соответственно.[1]
- ^ Эта реакция катализируется неизвестным тиоэстераза фермент.[43][44]
Справочные заметки
использованная литература
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае аф аг ах ай Wilson JM, Fitschen PJ, Campbell B, Wilson GJ, Zanchi N, Taylor L, Wilborn C, Kalman DS, Stout JR, Hoffman JR, Ziegenfuss TN, Lopez HL, Kreider RB, Smith-Ryan AE, Antonio J (февраль 2013 г.) . «Позиция Международного общества спортивного питания: бета-гидрокси-бета-метилбутират (HMB)». Журнал Международного общества спортивного питания. 10 (1): 6. Дои:10.1186/1550-2783-10-6. ЧВК 3568064. PMID 23374455.
[Международное общество спортивного питания] пришло к следующему выводу. 1. HMB можно использовать для ускорения восстановления за счет ослабления повреждений скелетных мышц, вызванных физическими упражнениями, у тренированных и нетренированных групп населения. ... 4. Тридцать восемь мг · кг · БМ−1 Было продемонстрировано, что ежедневное употребление HMB увеличивает гипертрофию, силу и мощность скелетных мышц у нетренированных и тренированных групп населения при использовании соответствующих предписаний упражнений. ... 8. Механизмы действия HMB включают ингибирование и усиление протеолиза и синтеза белка соответственно. 9. Хроническое употребление HMB безопасно как для молодого, так и для пожилого населения.
- ^ а б c «Информация о продукте: коктейль Ensure Enlive Advanced с лечебным питанием» (PDF). Abbott Nutrition. 9 августа 2016. В архиве (PDF) из оригинала 12 октября 2016 г.. Получено 22 августа 2016.
• Используйте под наблюдением врача.
• HMB + протеин для здоровья мышц.
"Информация о продукте: Ювен" (PDF). Abbott Nutrition. 7 мая 2016. В архиве (PDF) из оригинала 12 октября 2016 г.. Получено 22 августа 2016.
• Вводить перорально или модульно через зонд для кормления ...
• Используйте под наблюдением врача.
• Nutravigor® (CaHMB, β-гидрокси-β-метилбутират кальция) - ^ а б «Паспорт безопасности: 3-гидрокси-3-метилмасляная кислота». Альфа Эзар. 23 марта 2005 г. В архиве из оригинала 17 сентября 2016 г.. Получено 9 ноября 2016.
- ^ а б c d е Коффман Д.Д., Крамер Р., Мочель В.Е. (июнь 1958 г.). «Синтезы свободнорадикальными реакциями. V. Новый синтез карбоновых кислот». Журнал Американского химического общества. 80 (11): 2882–2887. Дои:10.1021 / ja01544a072.
- ^ а б «3-ОН-изовалериановая кислота». ChemSpider. Королевское химическое общество. 2015 г. В архиве из оригинала 11 августа 2016 г.. Получено 10 августа 2016.
Экспериментальная точка кипения: ... 128 ° C / 7 мм ...
Экспериментальная растворимость:
Растворим в воде - ^ «бета-гидроксиизовалериановая кислота». PubChem Compound. Национальная медицинская библиотека США - Национальный центр биотехнологической информации. 3 февраля 2018. В архиве из оригинала 6 февраля 2018 г.. Получено 6 февраля 2018.
Химические названия: бета-гидроксиизовалериановая кислота; 3-гидрокси-3-метилбутановая кислота; ... 3-гидроксиизовалериановая кислота; 3-гидрокси-3-метилмасляная кислота
- ^ а б c d е ж грамм час Линн Дж. (13 мая 2013 г.). «Белки в здоровье и производительности человека». Государственный университет Айовы. Архивировано из оригинал 27 августа 2016 г.. Получено 31 июля 2016.
Доктор Ниссен и его сотрудник доктор Наджи Н. Абумрад, профессор и заведующий кафедрой хирургии Университета Вандербильта, открыли бета-гидрокси-бета-метилбутират (HMB) и его благотворное влияние на здоровье и работоспособность человека. В настоящее время HMB продается на национальном рынке Abbott Laboratories как Revigor ™, который является компонентом Ensure® Muscle Health, и Juven®, который представляет собой пищевой напиток, который, как клинически доказано, способствует заживлению после травм или хирургических вмешательств.
- ^ а б Хамси Р. (май 2013 г.). «Переосмысление формулы». Природа Медицина. 19 (5): 525–529. Дои:10,1038 / нм0513-525. PMID 23652097. S2CID 205379191.
Вопросы о том, что определяет медицинское питание, вероятно, будут расти вместе с рынком, и этот рынок сейчас выходит далеко за пределы ФКУ и других наследственных нарушений обмена веществ. ... Juven от Abbott Nutrition обеспечивает питательными веществами людей с ВИЧ или СПИДом, страдающих от чрезмерной потери веса из-за болезни
- ^ а б «JUVEN добавлен в линейку пищевых продуктов Abbott Laboratories для людей с раком, ВИЧ / СПИДом и ран / пролежней». PR Newswire. Abbott Laboratories. 12 марта 2004 г. Архивировано с оригинал 20 декабря 2016 г.. Получено 11 декабря 2016.
- ^ а б c d е ж грамм час я j k л У Х, Ся И, Цзян Дж, Ду Х, Го Х, Лю Х, Ли Ц, Хуан Г, Ниу К. (сентябрь 2015 г.). «Влияние добавок бета-гидрокси-бета-метилбутирата на потерю мышечной массы у пожилых людей: систематический обзор и метаанализ». Архив геронтологии и гериатрии. 61 (2): 168–175. Дои:10.1016 / j.archger.2015.06.020. PMID 26169182.
В целом, этот метаанализ показывает, что HMB может предотвратить потерю мышечной массы у пожилых людей. Но влияние HMB на мышечную силу и физическую функцию, по-видимому, различается в разных группах населения. Необходимы дополнительные хорошо спланированные клинические исследования, чтобы подтвердить эффективность HMB в предотвращении потери мышечной силы и физической функции. ... Механизмы, лежащие в основе роли HMB в регенерации мышц, также были изучены: результаты показали, что HMB усиливает синтез белка за счет активации анаболических сигнальных путей и ослабляет протеолиз за счет подавления катаболических сигнальных путей (Wilkinson et al., 2013).
- ^ а б c d е ж Holeček M (август 2017). «Добавки бета-гидрокси-бета-метилбутирата и скелетные мышцы в здоровых условиях и условиях истощения мышц». Журнал кахексии, саркопении и мышц. 8 (4): 529–541. Дои:10.1002 / jcsm.12208. ЧВК 5566641. PMID 28493406.
Обобщенные здесь отчеты показывают, что HMB обеспечивает ряд преимуществ для субъектов, занимающихся силовыми видами спорта и видами спорта на выносливость. Воздействие на мышечную массу и силу, особенно во время тренировок с отягощениями, вероятно, связано с подавлением протеолиза и положительным влиянием на синтез белка. Его преимущества в аэробной производительности, вероятно, больше связаны с улучшением митохондриального биогенеза и окисления жиров. Благоприятное влияние на восстановление после повреждений, вызванных физическими упражнениями, может быть связано с ролью HMB как предшественника холестерина, который модулирует текучесть мембран и влияет на ионные каналы и возбудимость мембран. ... Исследования показали, что HMB может предотвратить развитие саркопении у пожилых людей и что оптимальное действие HMB на рост и силу мышц проявляется в сочетании с упражнениями.
- ^ а б Росси А.П., Д'Интроно А., Рубеле С., Калиари С., Гаттаццо С., Зойко Е., Маццали Г., Фантин Ф, Замбони М. (октябрь 2017 г.). «Возможности β-гидрокси-β-метилбутирата как новой стратегии лечения саркопении и саркопенического ожирения». Наркотики и старение. 34 (11): 833–840. Дои:10.1007 / s40266-017-0496-0. PMID 29086232. S2CID 4284897.
Клинические испытания, проведенные на пожилых людях, подтверждают, что HMB может замедлять прогрессирование саркопении у пожилых людей. Добавка HMB приводит к увеличению массы и силы скелетных мышц у пожилых людей, а его эффект еще больше в сочетании с физическими упражнениями.
- ^ а б c d е ж грамм Сильва В.Р., Белозо, Флорида, Мичелетти, ТО, Конрадо М, Стаут Дж. Р., Пиментел Г.Д., Гонсалес А.М. (сентябрь 2017 г.). «Добавка свободной кислоты β-гидрокси-β-метилбутирата может улучшить восстановление и адаптацию мышц после тренировки с отягощениями: систематический обзор» (PDF). Исследования питания. 45: 1–9. Дои:10.1016 / j.nutres.2017.07.008. HDL:11449/170023. PMID 29037326.
Обычно считается, что механизмы действия HMB связаны с его влиянием как на синтез мышечного белка, так и на распад мышечного белка (Рисунок 1) [2, 3]. HMB, по-видимому, стимулирует синтез мышечного белка за счет активации мишени рапамицина 1 (mTORC1) у млекопитающих / механистической мишени, сигнального каскада, участвующего в координации инициации трансляции синтеза мышечного белка [2, 4]. Кроме того, HMB может оказывать антагонистическое действие на убиквитин-протеасомный путь, систему, которая разрушает внутриклеточные белки [5, 6]. Имеющиеся данные также предполагают, что HMB способствует миогенной пролиферации, дифференцировке и слиянию клеток [7]. ... Экзогенное введение HMB-FA показало, что усиливает внутримышечную анаболическую передачу сигналов, стимулирует синтез мышечного белка и снижает распад мышечного белка у людей [2].
- ^ а б c d е ж грамм час я j k л м п о п Wilkinson DJ, Hossain T, Hill DS, Phillips BE, Crossland H, Williams J, Loughna P, Churchward-Venne TA, Breen L, Phillips SM, Etheridge T, Rathmacher JA, Smith K, Szewczyk NJ, Atherton PJ (июнь 2013 г.) . «Влияние лейцина и его метаболита β-гидрокси-β-метилбутирата на метаболизм белков скелетных мышц человека». Журнал физиологии. 591 (11): 2911–2923. Дои:10.1113 / jphysiol.2013.253203. ЧВК 3690694. PMID 23551944.
Стимуляция MPS посредством передачи сигналов mTORc1 после воздействия HMB согласуется с доклиническими исследованиями (Eley et al. 2008). ... Более того, было явное расхождение в амплитуде фосфорилирования для 4EBP1 (по Thr37 / 46 и Ser65 / Thr70) и p70S6K (Thr389) в ответ как на Leu, так и на HMB, причем последний показал более выраженное и устойчивое фосфорилирование. ... Тем не менее, поскольку общий ответ MPS был аналогичным, это различие в передаче сигналов клетками не привело к статистически различимым анаболическим эффектам в нашем первичном измерении результата MPS. ... Интересно, что хотя пероральный HMB не вызывал увеличения инсулина в плазме, он вызывал снижение MPB (-57%). Обычно постпрандиальное снижение MPB (примерно на 50%) объясняется азотсберегающим действием инсулина, так как инсулин зажимается в постабсорбтивных концентрациях (5 мкЕд / мл.−1) при непрерывной инфузии АК (18 г ч−1) не подавлял MPB (Greenhaff et al. 2008), поэтому мы решили не измерять MPB в группе Leu из-за ожидаемой гиперинсулинемии (рис. 3C). Таким образом, HMB снижает MPB аналогично инсулину, но не зависит от него. Эти данные согласуются с сообщениями об антикатаболических эффектах HMB, подавляющих MPB в доклинических моделях, посредством ослабления протеасомно-опосредованного протеолиза в ответ на LPS (Eley et al. 2008).
- ^ а б c d е ж грамм час я j k л м Brioche T, Pagano AF, Py G, Chopard A (август 2016 г.). «Мышечное истощение и старение: экспериментальные модели, жировые инфильтрации и профилактика» (PDF). Молекулярные аспекты медицины. 50: 56–87. Дои:10.1016 / j.mam.2016.04.006. PMID 27106402.
В заключение следует отметить, что лечение HMB явно представляет собой безопасную действенную стратегию против саркопении и, в целом, против мышечного истощения, поскольку HMB улучшает мышечную массу, мышечную силу и физическую работоспособность. Похоже, что HMB способен воздействовать на три из четырех основных механизмов, участвующих в разрушении мышц (обмен белков, апоптоз и регенеративный процесс), тогда как предполагается, что он сильно влияет на четвертый (динамика и функции митохондрий). Более того, HMB недорогой (~ 30–50 долларов США в месяц по 3 г в день) и может предотвратить остеопению (Bruckbauer and Zemel, 2013; Tatara, 2009; Tatara et al., 2007, 2008, 2012) и снизить сердечно-сосудистые риски. (Nissen et al., 2000). По всем этим причинам HMB следует регулярно использовать при истощении мышц, особенно у пожилых людей. ... 3 г CaHMB, принимаемых три раза в день (по 1 г каждый раз), является оптимальной дозой, которая обеспечивает постоянную биодоступность HMB в организме (Wilson et al., 2013)
- ^ а б c d е ж грамм час я Molfino A, Gioia G, Rossi Fanelli F, Muscaritoli M (декабрь 2013 г.). «Добавка бета-гидрокси-бета-метилбутирата при здоровье и болезнях: систематический обзор рандомизированных испытаний». Аминокислоты. 45 (6): 1273–1292. Дои:10.1007 / s00726-013-1592-z. PMID 24057808. S2CID 8688823.
Обычно человек метаболизирует 60 г L-LEU для получения 3 г HMB, но человек весом 70 кг производит 0,2–0,4 г HMB в день, в зависимости от дозы НОУ в рационе (Van Koevering and Nissen 1992). ... Обычная доза 3 г / день может быть рекомендована для поддержания или улучшения мышечной массы и функции при здоровье и болезни. Профиль безопасности HMB однозначен. ... Эти результаты показывают, что HMB / ARG / GLN можно безопасно использовать для лечения мышечной атрофии, связанной со СПИДом и раком.
- ^ а б c d е ж грамм Борак М.С., Вольпи Э. (декабрь 2016 г.). «Эффективность и безопасность приема лейцина у пожилых людей». Журнал питания. 146 (12): 2625S – 2629S. Дои:10.3945 / jn.116.230771. ЧВК 5118760. PMID 27934654.
В одном исследовании проверялась безопасность HMB при длительном применении на крысах. Fuller et al. (50) провели 91-дневное исследование с использованием крыс Sprague-Dawley, в котором проверялась безопасность β-гидрокси-β-метилмасляной свободной кислоты (HMBFA). Эта новая форма HMB приводит к более высоким концентрациям HMB в сыворотке, чем CaHMB. В этом исследовании крысам вводили HMBFA в размере 0%, 0,8%, 1,6% или 4% рациона по массе тела. Самая высокая доза эквивалентна ~ 400 мг кг.−1 ⋅ г−1 для людей. Ни в одной из групп лечения не наблюдалось неблагоприятных проявлений. Аналогичным образом, анализы крови и мочи были в пределах нормы во всех группах, без групповых различий. Авторы пришли к выводу, что HMBFA безопасен для употребления на модели крыс. ... Никаких серьезных побочных эффектов при добавлении лейцина, EAA или HMB не зарегистрировано; и риски для здоровья, связанные с этими добавками, немногочисленны и предсказуемы.
- ^ а б c d е ж грамм Момая А., Фавал М., Эстес Р. (апрель 2015 г.). «Вещества, улучшающие спортивные результаты: обзор литературы». Спортивная медицина. 45 (4): 517–531. Дои:10.1007 / s40279-015-0308-9. PMID 25663250. S2CID 45124293.
В настоящее время HMB доступен как безрецептурная добавка. Препарат не тестируется и не запрещен какой-либо спортивной организацией. ... Уилсон и др. [91] продемонстрировали, что, когда мужчины, не тренирующиеся с отягощениями, получали HMB перед тренировкой, повышение уровня лактатдегидрогеназы (ЛДГ) снижалось, а HMB имел тенденцию к уменьшению болезненности. Knitter et al. [92] показали снижение уровня ЛДГ и креатинфосфокиназы (КФК), побочного продукта разрушения мышц, под действием HMB после продолжительного бега. ... На полезность HMB действительно влияют время приема до тренировки и дозировка [97]. Кроме того, хроническое потребление HMB кажется безопасным [97]. ... О серьезных побочных эффектах от потребления HMB не сообщалось.
- ^ а б c d е Фуллер Дж. К., Шарп Р. Л., Ангус Х. Ф., Кху П. Ю., Ратмахер Дж. А. (ноябрь 2015 г.). «Сравнение доступности и скорости плазменного клиренса доставки β-гидрокси-β-метилбутирата в форме свободной кислоты и соли кальция». основной источник. Британский журнал питания. 114 (9): 1403–1409. Дои:10.1017 / S0007114515003050. PMID 26373270.
Недавно форма свободной кислоты HMB (HMB-FA) стала коммерчески доступной в форме капсул (гелькап). Настоящее исследование было проведено для сравнения биодоступности HMB с использованием двух коммерчески доступных капсульных форм HMB-FA и Ca-HMB. ... В заключение, HMB-FA в форме капсул улучшает скорость выведения и доступность HMB по сравнению с Ca-HMB в форме капсул.
- ^ а б c «Обзор питания Abbott» (PDF). Эбботт. Abbott Laboratories. Архивировано из оригинал (PDF) 3 сентября 2016 г.. Получено 3 сентября 2016.
- ^ а б Уилсон Дж. Дж., Уилсон Дж. М., Маннинен А. Х. (январь 2008 г.). «Влияние бета-гидрокси-бета-метилбутирата (HMB) на физическую работоспособность и состав тела в зависимости от возраста, пола и опыта тренировок: обзор». Питание и обмен веществ. 5: 1. Дои:10.1186/1743-7075-5-1. ЧВК 2245953. PMID 18173841.
- ^ а б c d е ж грамм час я j k л Щесняк К.А., Осташевский П., Фуллер Ю.С., Цецерска А., Садковский Т. (июнь 2015 г.). «Диетическая добавка β-гидрокси-β-метилбутирата для животных - обзор». Журнал физиологии животных и питания животных. 99 (3): 405–417. Дои:10.1111 / jpn.12234. PMID 25099672.
Холестерин является основным компонентом клеточной мембраны, а сарколемма - это тот компонент, который в основном зависит от синтеза холестерина de novo. Это важно в стрессовых условиях, когда мышечным клеткам может не хватать способности производить достаточное количество холестерина, необходимого для правильного функционирования клеточных мембран. Многие биохимические исследования показали, что HMB может быть предшественником синтеза холестерина (Bachhawat et al., 1955; Bloch et al., 1954; Coon et al., 1955; Adamson and Greenberg, 1955; Gey et al., 1957). Согласно соответствующей литературе, углерод HMB включен в холестерин. Следовательно, повышенные внутримышечные концентрации HMB могут обеспечить легкодоступный субстрат для синтеза холестерина, который необходим для образования и стабилизации сарколеммы. ... Известно, что добавка HMB снижает уровень ферментов после тренировки, что указывает на повреждение мышц, таких как креатининфосфокиназа (CK) и лактатдегидрогеназа (LDH), что свидетельствует об усилении функции мембран мышечных клеток. Это было показано в многочисленных исследованиях на людях, подвергавшихся как силовым тренировкам, так и тренировкам на выносливость (Wilson et al., 2013) ... Теоретически использование HMB в качестве предшественника холестерина может помочь в стабилизации мембран мышечных клеток; однако это не было подтверждено исследованиями. Влияние HMB на метаболизм белка на самом деле может помочь стабилизировать структуру мышц больше, чем любое влияние HMB на метаболизм холестерина в клетке.
- ^ а б c Фицджеральд М (май 2014 г.). Диетические культы: удивительное заблуждение, лежащее в основе модных диет и руководство по здоровому питанию для всех нас. Книги Пегаса. п.148. ISBN 978-1-60598-595-4. Получено 31 июля 2016.
HMB был открыт в середине 1990-х годов Стивом Ниссеном, исследователем из Университета штата Айова.
- ^ а б Риппе Дж. М. (март 2013 г.). «Бета-гидрокси бета-метилбутират». Медицина образа жизни (2-е изд.). CRC Press. п. 724. ISBN 978-1-4398-4544-8. В архиве из оригинала 22 марта 2018 г.. Получено 15 августа 2016.
- ^ а б «Запрещенный список (январь 2018 г.)» (PDF). Всемирное антидопинговое агентство. В архиве (PDF) из оригинала 22 октября 2017 г.. Получено 17 декабря 2017.
- ^ а б «Список запрещенных лекарств NCAA 2018–19». Национальная студенческая спортивная ассоциация. 10 июня 2015 г.. Получено 22 августа 2018.
- ^ а б Исследовательский персонал NCAA (январь 2006 г.). "Исследование NCAA привычек студентов-спортсменов к употреблению психоактивных веществ" (PDF). Национальная студенческая спортивная ассоциация. п. 7. В архиве (PDF) с оригинала 10 мая 2016 г.. Получено 24 июн 2016.
- ^ а б c Круз-Джентофт AJ (2018). «Бета-гидрокси-бета-метилбутират (HMB): от экспериментальных данных до клинических доказательств при саркопении». Современная наука о белках и пептидах. 18 (7): 668–672. Дои:10.2174/1389203718666170529105026. PMID 28554316.
HMB широко используется молодыми спортсменами в качестве эргогенной добавки. ... Это исследование показывает, что у здоровых пожилых людей добавки HMB могут сохранять мышечную массу в течение 10 дней постельного режима. Эти результаты обнадеживают, но они должны быть подтверждены другими группами.
- ^ а б c d е Аржилес Дж. М., Кампос Н., Лопес-Педроса Дж. М., Руэда Р., Родригес-Маньяс Л. (сентябрь 2016 г.). «Скелетные мышцы регулируют обмен веществ через межорганные взаимодействия: роль в здоровье и болезнях». Журнал Американской ассоциации медицинских директоров. 17 (9): 789–796. Дои:10.1016 / j.jamda.2016.04.019. PMID 27324808.
Исследования показывают, что диетический белок и лейцин или его метаболит β-гидрокси β-метилбутират (HMB) могут улучшить мышечную функцию, в свою очередь улучшая функциональную работоспособность. ... Они определили, что метаболит лейцина β-гидрокси β-метилбутират (HMB) является мощным стимулятором синтеза белка, а также ингибитором распада белка в крайних случаях кахексии. ... Растет количество доказательств того, что HMB может помочь замедлить или даже обратить вспять потерю мышечной массы, наблюдаемую при саркопении, и улучшить показатели мышечной силы. ... Однако диетический лейцин не обеспечивает большое количество HMB: только небольшая часть, всего 5%, катаболизированного лейцина метаболизируется в HMB. ... Таким образом, хотя диетический лейцин сам по себе может привести к умеренной стимуляции синтеза белка за счет производства небольшого количества HMB, прямое употребление HMB более сильно влияет на такую передачу сигналов, что приводит к заметному увеличению мышечной массы. ... Действительно, огромное количество исследований показали, что добавление HMB к диете может обратить вспять некоторую потерю мышечной массы, наблюдаемую при саркопении и гиперкатаболической болезни. ... Общее лечение атрофии мышц должно включать диетические добавки с HMB, хотя оптимальная дозировка для каждого состояния все еще исследуется. ...
Рисунок 4: Лечение саркопении. В настоящее время рекомендуется, чтобы пациенты с риском или страдающие от саркопении придерживались диеты с высоким содержанием белка, выполняли упражнения с отягощениями и принимали добавки метаболита лейцина HMB. - ^ Ланди Ф., Кальвани Р., Тосато М., Мартоне А.М., Ортолани Э., Савера Г., Д'Анджело Э., Систо А., Марцетти Э. (май 2016 г.). «Потребление белка и здоровье мышц в пожилом возрасте: от биологической достоверности до клинических данных». Питательные вещества. 8 (5): 295. Дои:10.3390 / nu8050295. ЧВК 4882708. PMID 27187465.
HMB представляет собой активный метаболит лейцина, который активирует сигнальный путь mTOR в мышцах.После абсорбции диетический лейцин превращается в α-кетоизокапроат (KIC), который далее метаболизируется в изовалерил-КоА или HMB. В нормальных условиях большая часть KIC превращается в изовалерил-КоА, в то время как только около 5% лейцина метаболизируется до HMB. Это означает, что для достижения фармакологического уровня HMB это соединение необходимо вводить напрямую, а не путем увеличения дозировки лейцина. ... HMB оказывает свое действие через защитные, антикатаболические механизмы и напрямую влияет на синтез белка. Было также показано, что HMB стабилизирует мембрану мышечных клеток, модулирует деградацию белка и повышает синтез белка [68].
- ^ Муллин Г.Е. (февраль 2014 г.). «Пищевые добавки для спортсменов: потенциальное применение при недоедании». Питание в клинической практике. 29 (1): 146–147. Дои:10.1177/0884533613516130. PMID 24336486.
На рынке представлен ряд продуктов питания, которые рекламируются как улучшающие спортивные результаты. HMB представляется наиболее многообещающим и имеет клиническое применение для улучшения мышечной массы и функции. Необходимы дальнейшие исследования с использованием этого нутрицевтика для предотвращения и / или улучшения недостаточности питания при истощении мышц.
- ^ а б Mochamat, Cuhls H, Marinova M, Kaasa S, Stieber C, Conrad R, Radbruch L, Mücke M (июль 2016 г.). «Систематический обзор роли витаминов, минералов, белков и других добавок в лечении кахексии при раке: проект Европейского центра исследований кахексии паллиативной помощи». Журнал кахексии, саркопении и мышц. 8 (1): 25–39. Дои:10.1002 / jcsm.12127. ЧВК 5326814. PMID 27897391.
Глядя на исследования белков и других пищевых добавок, комбинация HMB, аргинина и глутамина показала интересные результаты ... В одном исследовании 32 пациента набрали в среднем около 2 кг массы тела [21]. Это исследование было одним из трех исследований, подтверждающих положительный эффект этой комбинации при различных диагнозах / состояниях, таких как пациенты с ВИЧ / СПИДом и здоровые взрослые [40]. Другое исследование, проведенное на гораздо большей выборке из около 470 онкологических больных, не обнаружило значительных различий в отношении LBM через 8 недель, однако сильная тенденция в направлении увеличения LBM, измеренная как по биоимпедансу, так и по измерениям кожных складок . [22] Таким образом, влияние комбинации HMB, аргинина и глутамина на прибавку в весе должно быть изучено в дальнейших исследованиях на онкологических больных с периодом времени в несколько месяцев.
- ^ а б Рахман А., Вилунд К., Фитчен П.Дж., Джиджибхой К., Агарвала Р., Дровер Дж. В., Муртзакис М. (июль 2014 г.). «Пожилые люди со слабостью, приобретенной в ОИТ: потенциальная роль добавок β-гидрокси-β-метилбутирата (HMB)?». JPEN. Журнал парентерального и энтерального питания. 38 (5): 567–575. Дои:10.1177/0148607113502545. PMID 24072740.
Более 20 публикаций на людях продемонстрировали пользу от добавок HMB, связанную с увеличением безжировой массы тела без увеличения веса, улучшенными маркерами мышечной силы и уменьшением возникновения мышечной болезненности при тренировках и снижением маркеров мышечного повреждения. ... Одним из предполагаемых клеточных механизмов HMB является стабилизация холестериновой мембраны в мышечных клетках. HMB метаболизируется до β-гидрокси-β-метилглутарил-коэнзима A (HMG-CoA) в цитозоле мышечных клеток, который, в свою очередь, превращается в холестерин. ... Мышцы вырабатывают собственный холестерин для поддержания целостности клеточной мембраны, как правило, из HMG-CoA, потому что они не могут удовлетворить свои потребности в холестерине путем всасывания из кровотока.
- ^ а б c Luckose F, Pandey MC, Radhakrishna K (2015). «Влияние производных аминокислот на физическую, умственную и физиологическую активность». Критические обзоры в области пищевой науки и питания. 55 (13): 1793–1807. Дои:10.1080/10408398.2012.708368. PMID 24279396. S2CID 22657268.
HMB, производное лейцина, предотвращает повреждение мышц и увеличивает мышечную силу за счет уменьшения протеолиза в мышцах, вызванного физической нагрузкой, а также помогает увеличить безжировую массу тела. ... HMB превращается в HMB-CoA, который затем используется для синтеза холестерина в мышечных клетках (Nissen and Abumrad, 1997). Холестерин необходим для роста, восстановления и стабилизации клеточных мембран во время упражнений (Chen, 1984). ... Исследования метаанализа и отдельные проведенные исследования подтверждают использование HMB в качестве эффективного средства для увеличения силы тела, состава тела и предотвращения повреждения мышц во время силовых тренировок.
- ^ а б c Рахими М.Х., Мохаммади Х., Эшаги Х., Аскари Г., Мирагаджани М. (2018). «Влияние добавок бета-гидрокси-бета-метилбутирата на восстановление после повреждения мышц, вызванного физической нагрузкой: систематический обзор и метаанализ». Журнал Американского колледжа питания. 37 (7): 640–649. Дои:10.1080/07315724.2018.1451789. PMID 29676656. S2CID 4991601.
Текущие данные выявили зависящий от времени эффект HMB на снижение уровней LDH и CK в сыворотке крови у взрослых. Следовательно, HMB можно рассматривать как приоритетное средство восстановления после повреждения мышц при вмешательствах.
- ^ Санчес-Мартинес Дж., Сантос-Лозано А., Гарсия-Эрмосо А., Садарангани К. П., Кристи-Монтеро С. (июль 2018 г.). «Влияние добавок бета-гидрокси-бета-метилбутирата на силу и состав тела тренированных и конкурентоспособных спортсменов: метаанализ рандомизированных контролируемых испытаний». Журнал науки и медицины в спорте. 21 (7): 727–735. Дои:10.1016 / j.jsams.2017.11.003. PMID 29249685.
- ^ а б «Кому не следует принимать ИСБ?». Metabolic Technologies, Inc. 11 сентября 2014 г. В архиве из оригинала 26 августа 2016 г.. Получено 23 августа 2016.
Беременным и кормящим женщинам не рекомендуется принимать HMB, поскольку исследования безопасности для этих групп населения еще не проводились.
- ^ а б Брук М.С., Уилкинсон Д.И., Филлипс Б.Е., Перес-Шиндлер Дж., Филп А., Смит К., Атертон П.Дж. (январь 2016 г.). «Гомеостаз и пластичность скелетных мышц в молодости и старении: влияние питания и упражнений». Acta Physiologica. 216 (1): 15–41. Дои:10.1111 / apha.12532. ЧВК 4843955. PMID 26010896.
Механизмы, лежащие в основе анаболических эффектов приема пищи, включают как стимуляцию МПС (Rennie et al. 1982), так и подавление МПВ (Wilkes et al. 2009). Сильное увеличение MPS почти полностью обеспечивается незаменимыми аминокислотами (EAA) (Smith et al., 1992) с разветвленной цепью AA (BCAA: лейцин, изолейцин и валин), в частности лейцином [и его метаболитом (ами), например β-гидрокси β-метилмасляная кислота (HMB) (Van Koevering & Nissen 1992)] играет центральную роль в этих эффектах (Wilkinson et al. 2013). Хотя механизмы, лежащие в основе уникальных анаболических свойств лейцина, не полностью определены, недавняя работа на дрожжах и культивируемых клетках млекопитающих продемонстрировала, что лейцил-тРНК-синтетаза находится перед активацией до сих пор «клеточного сенсора АК», механической мишени комплекса рапамицина 1 (mTORC1) в ответ на лейцин (Bonfils et al. 2012, Han et al. 2012). Это было подтверждено экспериментами, показавшими, что из всех EAA лейцин является наиболее эффективным EAA в повышении активности (т.е. фосфорилирования) mTORC1 (Atherton et al. 2010b) и его субстратов.
- ^ а б c Филлипс С.М. (июль 2015 г.). «Пищевые добавки в поддержку упражнений с отягощениями для борьбы с возрастной саркопенией». Достижения в области питания. 6 (4): 452–460. Дои:10.3945 / ан.115.008367. ЧВК 4496741. PMID 26178029.
- ^ а б c Kornasio R, Riederer I, Butler-Browne G, Mouly V, Uni Z, Halevy O (май 2009 г.). «Бета-гидрокси-бета-метилбутират (HMB) стимулирует пролиферацию, дифференциацию и выживание миогенных клеток через пути MAPK / ERK и PI3K / Akt». основной источник. Biochimica et Biophysica Acta (BBA) - Исследование молекулярных клеток. 1793 (5): 755–763. Дои:10.1016 / j.bbamcr.2008.12.017. PMID 19211028.
- ^ а б c "Реакция KEGG: R10759". Киотская энциклопедия генов и геномов. Kanehisa Laboratories. В архиве из оригинала на 1 июля 2016 г.. Получено 24 июн 2016.
- ^ а б c Mock DM, Stratton SL, Horvath TD, Bogusiewicz A, Matthews NI, Henrich CL, Dawson AM, Spencer HJ, Owen SN, Boysen G, Moran JH (ноябрь 2011 г.). «Экскреция с мочой 3-гидроксиизовалериановой кислоты и 3-гидроксиизовалерилкарнитина увеличивается в ответ на дозу лейцина у людей с незначительным дефицитом биотина». основной источник. Журнал питания. 141 (11): 1925–1930. Дои:10.3945 / jn.111.146126. ЧВК 3192457. PMID 21918059.
Снижение активности МКЦ нарушает катализ на важном этапе митохондриального катаболизма лейцина ВСАА. Нарушение метаболизма переводит метилкротонил-КоА в 3-гидроксиизовалерил-КоА в реакции, катализируемой еноил-КоА-гидратазой (22, 23). Накопление 3-гидроксиизовалерил-КоА может подавлять клеточное дыхание либо напрямую, либо посредством воздействия на соотношение ацил-КоА: свободный КоА, если не происходит дальнейшего метаболизма и детоксикации 3-гидроксиизовалерил-КоА (22). Перенос карнитина с помощью 4 карнитин-ацил-CoA трансфераз, распределенных в субклеточных компартментах, вероятно, служит важным резервуаром для ацильных фрагментов (39–41). 3-Гидроксиизовалерил-КоА, вероятно, детоксифицируется карнитин-ацетилтрансферазой, продуцирующей 3HIA-карнитин, который транспортируется через внутреннюю митохондриальную мембрану (и, следовательно, эффективно из митохондрий) через карнитин-ацилкарнитинтранслоказу (39). Считается, что 3HIA-карнитин либо непосредственно деацилируется гидролазой до 3HIA, либо подвергается второму обмену КоА с образованием 3-гидроксиизовалерил-КоА с последующим высвобождением 3HIA и свободного КоА тиоэстеразой.
- ^ а б c d е ж грамм час я j k л м Кольмайер М (май 2015 г.). «Лейцин». Метаболизм питательных веществ: структуры, функции и гены (2-е изд.). Академическая пресса. С. 385–388. ISBN 978-0-12-387784-0. В архиве из оригинала 22 марта 2018 г.. Получено 6 июн 2016.
Энергетическое топливо: в конечном итоге большая часть лея расщепляется, обеспечивая около 6,0 ккал / г. Около 60% проглоченного лей окисляется в течение нескольких часов ... Кетогенез: значительная часть (40% проглоченной дозы) превращается в ацетил-КоА и тем самым способствует синтезу кетонов, стероидов, жирных кислот и других соединения
Рисунок 8.57: Метаболизм L-лейцин В архиве 22 марта 2018 в Wayback Machine - ^ «Метаболизм лейцина». БРЕНДА. Technische Universität Braunschweig. Архивировано из оригинал 17 августа 2016 г.. Получено 12 августа 2016.
- ^ "Реакция KEGG: R04137". Киотская энциклопедия генов и геномов. Kanehisa Laboratories. В архиве из оригинала на 1 июля 2016 г.. Получено 24 июн 2016.
- ^ «Homo sapiens: реакция 4-гидроксифенилпируват диоксигеназы». MetaCyc. SRI International. 20 августа 2012 г.. Получено 6 июн 2016.
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты «3-Гидроксиизовалериановая кислота». HMDB версии 4.0. База данных человеческого метаболома. 7 декабря 2017. В архиве из оригинала 5 декабря 2017 г.. Получено 26 декабря 2017.
- ^ «3-гидроксиизовалерат». Химические объекты, представляющие биологический интерес. Европейский институт биоинформатики. 16 сентября 2014 г. В архиве с оригинала на 1 декабря 2017 г.. Получено 20 августа 2016.
- ^ Заявка WO 2015094925, White TO, «Стабильная заполненная жидкостью твердая капсула, содержащая бета-гидрокси-бета-метилмасляную кислоту», опубликовано 25 июня 2015 г., передано Capsugel Belgium Nv.
- ^ «Бета-гидроксиизовалериановая кислота». Химическая книга. В архиве с оригинала 21 августа 2016 г.. Получено 20 августа 2016.
- ^ а б «3-гидроксиизовалериановая кислота». Химические объекты, представляющие биологический интерес. Европейский институт биоинформатики. 23 октября 2015 г. В архиве из оригинала 12 марта 2016 г.. Получено 20 августа 2016.
- ^ а б Самая ранняя ссылка на синтез β-гидрокси β-метилмасляной кислоты в Reaxys химическая база данных по состоянию на сентябрь 2016 года:
Сайцев М, Сайцев А (1877). "Синтез аллилдиметилкарбинолов" [Синтез аллилдиметилкарбинолов]. Annalen der Chemie Юстуса Либиха (на немецком). 185 (2–3): 151–169. Дои:10.1002 / jlac.18771850204. - ^ Щироков А. (январь 1881 г.). "Ueber die β-Dipropyl- und β-Diäthyläthylenmilchsäure und über die Oxydation des Allyldimethylcarbinols und Diallylcarbinols mit übermangansaurem Kalium" [О β-дипропил- и β-диэтиленилмолочной кислоте и об окислении аллилдиметилкарбинола и диаллилкарбинола избытком калия]. Journal für Praktische Chemie (на немецком). 23 (1): 196–208. Дои:10.1002 / prac.18810230115.
- ^ Реформатский Б. (30 октября 1889 г.). "Synthese einiger Glycerine mittelst unterchloriger Säure" [Синтез некоторых глицерина хлорноватистой кислотой]. Journal für Praktische Chemie (на немецком). 40 (1): 396–419. Дои:10.1002 / prac.18890400137.
- ^ Макмерри, Джон Э. (2010). «Окисление алкенов: эпоксидирование, гидроксилирование и расщепление». Основы органической химии (7-е изд.). Cengage Learning. С. 124–126, 142. ISBN 9781439049716.
- ^ Кондаков Я. (1892). «О действии минеральных кислот на диметилаллилы». Журнал Русскаго Физико-Химического Общества (Журнал Русского Физико-Химического Общества) (по-русски). 1: 508–513. отведено Гроссет (1893 г.). "Ueber die Einwirkung von Mineralsauren auk Dimethylallen" [О действии минеральных кислот на диметилаллилы]. Berichte der Deutschen Chemischen Gesellschaft (на немецком). 26 (4): 96. Дои:10.1002 / cber.18930260412.
- ^ Грешем Т.Л., Янсен Дж. Э., Шейвер Ф. В., Беирс В. Л. (январь 1954 г.). «β-Пропиолактон. XIV. β-Изовалеролактон». Журнал Американского химического общества. 76 (2): 486–488. Дои:10.1021 / ja01631a045.
- ^ Заявка WO 2012140276, Noti C, Schmid L, Rittiner B, Hanselmann P, Bierstedt A, «Процесс получения 3-гидрокси-3-метилмасляной кислоты или ее солей кальция», опубликовано 10 января 2013 г., передано Lonza Ltd.
- ^ а б Кон М. (сентябрь 1903 г.). "Zur Kenntnis des Diacetonalkohols und des Mesityloxyds" [Знание диацетоновых спиртов и мезитилоксида]. Monatshefte für Chemie und Verwandte Teile Anderer Wissenschaften. 24 (9): 765–772. Дои:10.1007 / BF01526057. S2CID 96317019.
- ^ Дорайсвами Л.К. (февраль 2001 г.). «Пример 5.2». Органический синтез. Нью-Йорк: Издательство Оксфордского университета. С. 102–124. ISBN 978-0-19-509689-7.
- ^ Кочи JK (декабрь 2012 г.). «Гомолитический механизм в металлическом катализе». Металлоорганические механизмы и катализ: роль реакционноспособных промежуточных продуктов в органических процессах. Нью-Йорк: Эльзевир. п. 67. ISBN 978-0-323-14410-0. В архиве из оригинала от 22 марта 2018 г.
- ^ Ли И.Ю., Ниссен С.Л., Розазза ДжП (ноябрь 1997 г.). "Превращение бета-метилмасляной кислоты в бета-гидрокси-бета-метилмасляную кислоту путем Galactomyces reessii". основной источник. Прикладная и экологическая микробиология. 63 (11): 4191–4195. Дои:10.1128 / AEM.63.11.4191-4195.1997. ЧВК 168736. PMID 9361403.
- ^ а б c Ehling S, Reddy TM (сентябрь 2015 г.). «Прямой анализ лейцина и его метаболитов β-гидрокси-β-метилмасляной кислоты, α-кетоизокапроновой кислоты и α-гидроксиизокапроновой кислоты в грудном молоке человека с помощью жидкостной хроматографии-масс-спектрометрии». основной источник. Журнал сельскохозяйственной и пищевой химии. 63 (34): 7567–7573. Дои:10.1021 / acs.jafc.5b02563. PMID 26271627.
- ^ а б Ehling S, Reddy TM (февраль 2014 г.). «Исследование присутствия β-гидрокси-β-метилмасляной кислоты и α-гидроксиизокапроновой кислоты в цельном молоке крупного рогатого скота и кисломолочных продуктах с помощью утвержденного метода жидкостной хроматографии-масс-спектрометрии». основной источник. Журнал сельскохозяйственной и пищевой химии. 62 (7): 1506–1511. Дои:10.1021 / jf500026s. PMID 24495238.
- ^ Ружичка Л., Далма Г., Энгель Б.Г., Скотт В.Е. (1941). "Zur Kenntnis der Erythrophleum-Alkaloide. (5. Mitteilung). Identifizierung der niedermolekularen Spaltsäure des Coumingins" [Относительно алкалоидов эритрофлеума. (5-е сообщение). Идентификация низкомолекулярных кислот отщепления от кумингина. Helvetica Chimica Acta (на немецком). 24 (1): 1449–1458. Дои:10.1002 / hlca.194102401171.
- ^ Танака К., Орр Дж. К., Иссельбахер К. Дж. (Май 1968 г.). «Определение бета-гидроксиизовалериановой кислоты в моче пациента с изовалериановой ацидемией». основной источник. Biochimica et Biophysica Acta (BBA) - липиды и липидный метаболизм. 152 (3): 638–41. Дои:10.1016/0005-2760(68)90107-0. PMID 5656832.
- ^ Танака К. (1975). «Нарушения обмена органических кислот». В Gaull GE (ред.). Биология дисфункции мозга, том 3. Бостон, Массачусетс: Springer США. С. 145–214. Дои:10.1007/978-1-4684-2673-1_3. ISBN 978-1-4684-2675-5.
- ^ а б c d «Предложение Фонда экономического развития штата Айова по расширению ценностей штата Айова: 2011 финансовый год» (PDF). Университет Айовы. С. 13–16. В архиве (PDF) из оригинала на 1 сентября 2016 г.. Получено 1 сентября 2016.
- ^ «Патенты, переданные компании Metabolic Technologies, Inc». Патент Justia.
По состоянию на март 2018 г.[Обновить] выданные патенты включают: US8815280, US9259430, US9539224, US9707241, и US9770424.
внешние ссылки
| Викискладе есть медиафайлы по теме Бета-гидрокси бета-метилбутират. |
- Бета-гидроксиизовалериановая кислота в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)