WikiDer > Триптамин
 | |
 | |
| Имена | |
|---|---|
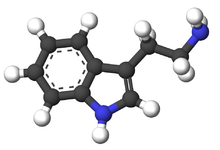
| Название ИЮПАК 2-(1ЧАС-Индол-3-ил) этанамин | |
| Идентификаторы | |
3D модель (JSmol) | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.000.464 |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C10ЧАС12N2 | |
| Молярная масса | 160.220 г · моль−1 |
| Внешность | от белого до оранжевого кристаллического порошка[1] |
| Температура плавления | 113-116˚C[1] |
| Точка кипения | 137 ° С (279 ° F, 410 К) (0,15 мм рт. Ст.)[1] |
| незначительная растворимость в воде[1] | |
| Опасности | |
| точка возгорания | 185˚C[1] |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Триптамин это моноамин алкалоид. Он содержит индол кольцевая структура и конструктивно похожа на аминокислота триптофан, от которого и произошло название. Триптамин содержится в след суммы в мозги из млекопитающие и предполагается, что он играет роль нейромодулятор или же нейротрансмиттер.[2] Подобно другим следы аминов, триптамин связывается с человеческим следовой амин-ассоциированный рецептор 1 (TAAR1) как агонист.[3]
Триптамин - это общая функциональная группа в наборе соединений, вместе называемых замещенные триптамины. В этот набор входит много биологически активный соединения, включая нейротрансмиттеры и психоделические препараты.
Концентрация триптамина в головном мозге крысы составляет около 3,5. пмоль/грамм.[4]
Растения, содержащие триптамин
Многие растения содержат небольшое количество триптамина. Это сырье для метаболических путей, влияющих на рост растений и микробиом. Например, он встречается как возможное промежуточное звено в одном биосинтетический путь к растительному гормону индол-3-уксусная кислота.[5] Более высокие концентрации можно найти во многих Акация разновидность.
Фармакология
Триптамин является агонистом hTAAR1.[3] Он действует как неизбирательный агонист серотониновых рецепторов и агент, высвобождающий серотонин-норэпинефрин-дофамин (SNDRA), с предпочтением вызывать серотонин и дофамин релиз над норэпинефрин релиз.[6][7][8]
Было показано, что триптамин действует как неконкурентный ингибитор серотонин N-ацетилтрансфераза (SNAT) у комаров.[9] SNAT катализирует анаболический метаболизм серотонина в N-ацетилсеротонин, еще один нейромодулятор (в частности, нейротрофический фактор через TrkB агонизм) и непосредственный предшественник мелатонин.
Триптамин быстро метаболизируется МАО-А и МАО-Б,[10] и по этой причине имеет очень короткий in vivo период полураспада.
Синтез
В Синтез триптамина Абрамовича – Шапиро является органическая реакция для синтеза триптамина.[11]
Смотрите также
Рекомендации
- ^ а б c d е http://www.chemicalbook.com/ProductChemicalPropertiesCB8192006_EN.htm[требуется полная цитата]
- ^ Джонс Р.С. (1982). «Триптамин: нейромодулятор или нейромедиатор в головном мозге млекопитающих?». Прогресс в нейробиологии. 19 (1–2): 117–139. Дои:10.1016/0301-0082(82)90023-5. PMID 6131482. S2CID 24509577.
- ^ а б Хан MZ, Nawaz W (октябрь 2016 г.). «Новые роли человеческих следовых аминов и человеческих следовых амино-ассоциированных рецепторов (hTAAR) в центральной нервной системе». Биомед. Фармаколог. 83: 439–449. Дои:10.1016 / j.biopha.2016.07.002. PMID 27424325.
- ^ Цзян, Чжэнь; Матч, Элейн; Блейн, Питер Дж .; Уильямс, Фейт М. (2006). «Преобразование трихлорэтилена в хлорал с использованием профессиональных уровней». Токсикология. 226 (1): 76–77. Дои:10.1016 / j.tox.2006.05.102.
- ^ Нобутака Такахаси (1986). Химия растительных гормонов. CRC Press. ISBN 9780849354700.
- ^ Вельфель, Рейнхард; Грефе, Карл-Хайнц (1992). «Доказательства различных триптаминов и родственных соединений, действующих в качестве субстратов переносчика 5-гидрокситриптамина тромбоцитов». Архив фармакологии Наунин-Шмидеберг. 345 (2): 129–36. Дои:10.1007 / BF00165727. PMID 1570019. S2CID 2984583.
- ^ Симадзу, S; Микля, Я (2004). «Фармакологические исследования эндогенных усиливающих веществ: бета-фенилэтиламин, триптамин и их синтетические производные». Прогресс в нейропсихофармакологии и биологической психиатрии. 28 (3): 421–7. Дои:10.1016 / j.pnpbp.2003.11.016. PMID 15093948. S2CID 37564231.
- ^ Blough, Bruce E .; Ландавазо, Антонио; Partilla, John S .; Декер, Энн М .; Пейдж, Кевин М .; Baumann, Michael H .; Ротман, Ричард Б. (2014). «Альфа-этилтриптамины как двойные высвобождающие дофамин-серотонин». Письма по биоорганической и медицинской химии. 24 (19): 4754–4758. Дои:10.1016 / j.bmcl.2014.07.062. ISSN 0960-894X. ЧВК 4211607. PMID 25193229.
- ^ Кху Х.Г., Вонг КП (1994). "Производство ацетил-КоА и N-ацетилирование серотонина (5HT) у комара Aedes togoi ». Биохимия и молекулярная биология насекомых. 24 (5): 445–51. Дои:10.1016/0965-1748(94)90039-6. PMID 7911372.
- ^ Салливан, Джеймс П .; Макдоннелл, Леонард; Hardiman, Orla M .; Фаррелл, Майкл А .; Филлипс, Джек П .; Типтон, Кейт Ф. (1986). «Окисление триптамина двумя формами моноаминоксидазы в тканях человека». Биохимическая фармакология. 35 (19): 3255–60. Дои:10.1016/0006-2952(86)90421-1. PMID 3094536.
- ^ Абрамович, Р. А .; Шапиро, Д. (1956). «880. Триптамины, карболины и родственные соединения. Часть II. Удобный синтез триптаминов и β-карболинов». Журнал химического общества: 4589–92. Дои:10.1039 / JR9560004589.
внешняя ссылка
- Часто задаваемые вопросы о триптамине
- Триптаминовые галлюциногены и сознание
- Триптаминд Психоактивные вещества, справочный сайт о триптамине и других психоактивных веществах.
- Вход триптамина (Т) в TiHKAL • информация
