WikiDer > Панкреатический рак
| Панкреатический рак | |
|---|---|
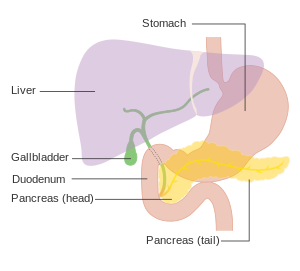 | |
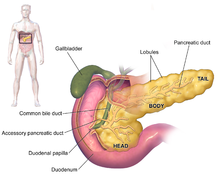
| Схема, показывающая положение поджелудочной железы за желудком (на этой схеме она прозрачна). | |
| Специальность | Гастроэнтерология Гепатология Онкология |
| Симптомы | Желтая кожа, брюшной или же боль в спине, необъяснимая потеря веса, светлый табуреты, темная моча, потеря аппетита[1] |
| Обычное начало | После 40 лет[2] |
| Факторы риска | Курение табака, ожирение, сахарный диабет, некоторые редкие генетический условия[2] |
| Диагностический метод | Медицинская визуализация, анализы крови, биопсия ткани[3][4] |
| Профилактика | Не курить, поддерживать здоровый вес, низкий красное мясо рацион питания[5] |
| Уход | Хирургия, лучевая терапия, химиотерапия, паллиативная помощь[1] |
| Прогноз | Пятилетняя выживаемость 6%[6] |
| Частота | 393,800 (2015)[7] |
| Летальные исходы | 411,600 (2015)[8] |
Панкреатический рак возникает, когда клетки в поджелудочная железа, железистый орган позади желудок, начинают бесконтрольно размножаться и образуют масса. Эти раковый клетки имеют способность вторгаться другие части тела.[9] Известно несколько типов рака поджелудочной железы.[10] Самый распространенный, аденокарцинома поджелудочной железы, составляет около 90% случаев,[11] и термин «рак поджелудочной железы» иногда используется для обозначения только этого типа.[10] Эти аденокарциномы начинаются в той части поджелудочной железы, которая производит пищеварительные ферменты.[10] Несколько других типов рака, которые в совокупности представляют большинство неаденокарцином, также могут возникать из этих клеток.[10] Около 1–2% случаев рака поджелудочной железы нейроэндокринные опухоли, которые возникают в результате продуцирования гормонов клетки поджелудочной железы.[10] Обычно они менее агрессивны, чем аденокарцинома поджелудочной железы.[10]
Признаки и симптомы наиболее распространенной формы рака поджелудочной железы могут включать: желтая кожа, брюшной или же боль в спине, необъяснимая потеря веса, светлый табуреты, темная моча и потеря аппетита.[1] Обычно на ранних стадиях болезни симптомы не проявляются, а симптомы специфический достаточно, чтобы предположить, что рак поджелудочной железы обычно не развивается, пока болезнь не достигнет запущенной стадии.[1][2] К моменту постановки диагноза рак поджелудочной железы часто распространять к другим частям тела.[10][12]
Рак поджелудочной железы редко возникает в возрасте до 40 лет, и более половины случаев аденокарциномы поджелудочной железы возникает у лиц старше 70 лет.[2] Факторы риска рака поджелудочной железы включают: курение табака, ожирение, сахарный диабет, и некоторые редкие генетические условия.[2] Около 25% случаев связаны с курением,[3] и 5–10% связаны с унаследованные гены.[2] Рак поджелудочной железы обычно диагностируется при сочетании следующих факторов: медицинская визуализация такие методы, как УЗИ или же компьютерная томография, анализы крови и исследование образцов тканей (биопсия).[3][4] Болезнь разделены на этапы, от раннего (I этап) до позднего (IV этап).[12] Скрининг для населения в целом эффективность не обнаружена.[13]
Риск развития рака поджелудочной железы ниже у некурящих и людей, которые поддерживают здоровый вес и ограничивают потребление красный или же обработанное мясо.[5] Шансы курильщиков на развитие болезни уменьшаются, если они бросают курить, и почти возвращаются к таковым для остального населения через 20 лет.[10] Рак поджелудочной железы можно вылечить хирургическим путем, лучевая терапия, химиотерапия, паллиативная помощь, или их сочетание.[1] Варианты лечения частично зависят от стадии рака.[1] Хирургия - единственное лечение, которое может вылечить аденокарциному поджелудочной железы,[12] а также может быть сделано для улучшения качество жизни без возможности излечения.[1][12] Контроль над болью иногда необходимы лекарства для улучшения пищеварения.[12] Ранняя паллиативная помощь рекомендуется даже тем, кто получает лечение, направленное на излечение.[14]
В 2015 году от рака поджелудочной железы всех типов во всем мире умерло 411 600 человек.[8] Рак поджелудочной железы - пятая по частоте причина смерти от рака в Великобритании.[15] и третий по распространенности в США.[16] Заболевание чаще всего встречается в развитых странах, где в 2012 году возникло около 70% новых случаев.[10] Аденокарцинома поджелудочной железы обычно имеет очень плохой прогноз; после постановки диагноза 25% людей живут один год, а 5% - пять лет.[6][10] При ранней диагностике рака пятилетняя выживаемость возрастает примерно до 20%.[17] Нейроэндокринный рак дает лучшие результаты; через пять лет после постановки диагноза 65% диагностированных остаются живы, хотя выживаемость значительно варьируется в зависимости от типа опухоли.[10]
Типы

Многие типы рака поджелудочной железы можно разделить на две общие группы. Подавляющее большинство случаев (около 95%) происходит в той части поджелудочной железы, которая производит пищеварительные ферменты, известный как экзокринный компонент. Описано несколько подтипов экзокринного рака поджелудочной железы, но их диагностика и лечение имеют много общего. Небольшое количество раковых заболеваний, возникающих в гормон-производство (эндокринный) ткани поджелудочной железы имеют разные клинические характеристики и называются нейроэндокринные опухоли поджелудочной железы, иногда сокращенно «PanNETs». Обе группы встречаются в основном (но не исключительно) у людей старше 40 лет и немного чаще встречаются у мужчин, но некоторые редкие подтипы встречаются в основном у женщин или детей.[18][19]
Экзокринный рак
В экзокринной группе преобладают панкреатические. аденокарцинома (варианты этого названия могут добавлять «инвазивный» и «протоковый»), который на сегодняшний день является наиболее распространенным типом, составляющим около 85% всех случаев рака поджелудочной железы.[2] Почти все они начинаются в протоках поджелудочной железы, как протоковая аденокарцинома поджелудочной железы (PDAC).[20] И это несмотря на то, что ткань, из которой он возникает - проток поджелудочной железы. эпителий - представляет менее 10% поджелудочной железы по объему клеток, потому что он составляет только протоки (обширная, но капиллярно-подобная система протоков, расширяющаяся веером) внутри поджелудочной железы.[21] Этот рак возникает в протоках, несущих секреты (например, ферменты и бикарбонат) от поджелудочной железы. Около 60–70% аденокарцином возникает в головка поджелудочной железы.[2]
Следующий по распространенности тип, ацинарно-клеточная карцинома поджелудочной железы, возникает в скопления клеток которые производят эти ферменты, и составляют 5% случаев экзокринного рака поджелудочной железы.[22] Подобно «функционирующему» эндокринному раку, описанному ниже, ацинарно-клеточная карцинома может вызывать избыточное производство определенных молекул, в данном случае пищеварительных ферментов, которые могут вызывать такие симптомы, как кожная сыпь и боль в суставах.
Цистаденокарциномы составляют 1% случаев рака поджелудочной железы, и у них лучший прогноз, чем у других экзокринных типов.[22]
Панкреатобластома - редкая форма, чаще всего встречающаяся в детстве, с относительно хорошим прогнозом. Другие экзокринные виды рака включают: аденосквамозная карцинома, карциномы из перстневых клеток, гепатоидные карциномы, коллоидные карциномы, недифференцированный карциномы и недифференцированные карциномы с остеокласт-подобно гигантские клетки. Солидная псевдопапиллярная опухоль редкий низкийоценка новообразование, которое в основном поражает молодых женщин и обычно имеет очень хороший прогноз.[2][23]
Муцинозно-кистозные новообразования поджелудочной железы представляют собой широкую группу опухолей поджелудочной железы с различным злокачественным потенциалом. Их выявляют все чаще, поскольку компьютерная томография становится все более мощной и распространенной, и продолжается обсуждение того, как лучше всего их оценивать и лечить, учитывая, что многие из них доброкачественные.[24]
Нейроэндокринный
Небольшое количество опухолей, которые возникают в других частях поджелудочной железы, в основном нейроэндокринные опухоли поджелудочной железы (ПанНЕТ).[25] Нейроэндокринные опухоли (NET) - это разнообразная группа доброкачественный или злокачественный опухоли, возникающие из-за нейроэндокринные клетки, которые отвечают за интеграцию нервный и эндокринные системы. НЭО могут начинаться в большинстве органов тела, включая поджелудочную железу, где все различные злокачественные новообразования считаются редкий. PanNET подразделяются на «функционирующие» и «нефункционирующие» типы в зависимости от того, в какой степени они производят гормоны. Функциональные типы выделяют гормоны, такие как инсулин, гастрин, и глюкагон в кровоток, часто в больших количествах, вызывая серьезные симптомы, такие как низкий уровень сахара в крови, но также способствует относительно раннему обнаружению. Наиболее часто функционирующие сети PanNET: инсулиномы и гастриномы, названный в честь гормонов, которые они выделяют. Неработающие типы не выделяют гормоны в достаточном количестве, чтобы вызвать явные клинические симптомы, поэтому нефункционирующие PanNET часто диагностируются только после того, как рак распространился на другие части тела.[26]
Как и в случае с другими нейроэндокринными опухолями, история терминологии и классификации PanNET сложна.[25] PanNETs иногда называют «раком островковых клеток»,[27] хотя теперь известно, что они на самом деле не возникают из островковые клетки как думали ранее.[26]
Признаки и симптомы
Поскольку рак поджелудочной железы обычно не вызывает распознаваемых симптомов на ранних стадиях, болезнь обычно не диагностируется, пока она не распространилась за пределы самой поджелудочной железы.[4] Это одна из основных причин в целом низкой выживаемости. Исключением являются функционирующие сети PanNET, где избыточное производство различных активных гормонов может вызывать симптомы (которые зависят от типа гормона).[28]
Принимая во внимание, что заболевание редко диагностируется до 40 лет, общие симптомы аденокарциномы поджелудочной железы, возникающие до постановки диагноза, включают:
- Боль в верхней части живота или обратно, часто распространяясь от живота к спине. Местонахождение боли может указывать на ту часть поджелудочной железы, где расположена опухоль. Боль может усиливаться ночью и со временем усиливаться, становясь сильной и непрекращающейся.[22] Это можно немного облегчить, наклонившись вперед. В Великобритании около половины новых случаев рака поджелудочной железы диагностируется после посещения отделения неотложной помощи больницы по поводу боли или желтухи. Примерно у двух третей людей боль в животе является основным симптомом, из которых 46% от общего числа сопровождается желтухой, а у 13% - желтухой без боли.[12]
- Желтуха, желтый оттенок белки глаз или кожи, с болью или без нее, и, возможно, в сочетании с потемнением мочи, возникает, когда рак головки поджелудочной железы препятствует общий желчный проток поскольку он проходит через поджелудочную железу.[29]
- Необъяснимая потеря веса, либо из потеря аппетита, или потеря экзокринной функции, приводящая к плохое пищеварение.[12]
- Опухоль может сдавливать соседние органы, нарушая процессы пищеварения и затрудняя желудок опустошить, что может вызвать тошнота и чувство сытости. Непереваренный жир вызывает неприятный запах, жирный кал которые трудно смыть.[12] Запор также обычное дело.[30]
- По крайней мере, у 50% людей с аденокарциномой поджелудочной железы сахарный диабет на момент диагностики.[2] Хотя длительный диабет является известным фактором риска рака поджелудочной железы (см. Факторы риска), рак сам по себе может вызвать диабет, и в этом случае недавнее начало диабета можно рассматривать как ранний признак заболевания.[31] Люди старше 50 лет, у которых развивается диабет, имеют в восемь раз больший риск развития аденокарциномы поджелудочной железы в течение трех лет, после чего относительный риск снижается.[12]
Другие выводы
- Синдром Труссо, при котором тромбы образуются спонтанно в портальные кровеносные сосудыглубокие вены конечностей или поверхностные вены на любом участке тела могут быть связаны с раком поджелудочной железы и обнаруживаются примерно в 10% случаев.[3]
- Клиническая депрессия сообщалось о связи с раком поджелудочной железы примерно в 10–20% случаев и может быть препятствием для оптимального лечения. Иногда депрессия проявляется еще до того, как диагностируется рак, что позволяет предположить, что она может быть вызвана биологией заболевания.[3]
К другим частым проявлениям заболевания относятся слабость и легкая утомляемость, сухость во рту, проблемы со сном и ощутимый брюшная масса.[30]
Симптомы распространения

Распространение рака поджелудочной железы на другие органы (метастаз) также может вызывать симптомы. Обычно аденокарцинома поджелудочной железы сначала распространяется на близлежащие лимфатический узел, а затем в печень или в брюшная полость, толстая кишка, или легкие.[3] В редких случаях он распространяется на кости или мозг.[32]
Рак поджелудочной железы также может быть вторичный рак которые распространились из других частей тела. Это необычно и встречается только в 2% случаев рака поджелудочной железы. Рак почки на сегодняшний день является наиболее распространенным раком, распространяющимся на поджелудочную железу, за которым следует колоректальный рак, а затем рак кожа, грудь, и легкое. В таких случаях может быть выполнено хирургическое вмешательство на поджелудочной железе в надежде на излечение или облегчение симптомов.[33]
Факторы риска
Факторы риска К аденокарциноме поджелудочной железы относятся:[2][10][12][34][35]
- Возраст, пол и этническая принадлежность - риск развития рака поджелудочной железы увеличивается с возрастом. Большинство случаев возникают после 65 лет,[10] в то время как случаи до 40 лет - редкость. Заболевание несколько чаще встречается у мужчин, чем у женщин.[10] В Соединенных Штатах это более чем в 1,5 раза чаще встречается в афро-американцы, хотя заболеваемость в Африке низкая.[10]
- Курение сигарет является наиболее установленным предотвратимым фактором риска рака поджелудочной железы, который примерно вдвое увеличивает риск среди курильщиков-длительных курильщиков, причем риск увеличивается с увеличением количества выкуриваемых сигарет и количества лет курения. Риск медленно снижается после Отказ от курения, требуется около 20 лет, чтобы вернуться почти к уровню некурящих.[36]
- Ожирение - а индекс массы тела более 35 увеличений относительный риск примерно наполовину.[12] [37]
- Семейный анамнез - 5–10% случаев рака поджелудочной железы имеют наследственный компонент, когда у людей есть семейный анамнез рака поджелудочной железы.[2][38] Риск значительно возрастает, если более одного родственник первой степени имели заболевание, и более скромно, если они заболели до 50 лет.[4] Большинство из гены вовлеченных не выявлено.[2][39] Наследственный панкреатит дает значительно увеличенный риск жизни рака поджелудочной железы 30–40% к 70 годам.[3] Скрининг на ранний рак поджелудочной железы может быть предложен людям с наследственным панкреатитом на исследовательской основе.[40] Некоторые люди могут выбрать хирургическое удаление поджелудочной железы, чтобы предотвратить развитие рака в будущем.[3]
- Рак поджелудочной железы был связан с другими редкими наследственными синдромами: Синдром Пейтца-Егерса из-за мутаций в STK11 ген-супрессор опухоли (очень редко, но очень сильный фактор риска); синдром диспластического невуса (или синдром семейной атипичной множественной родинки и меланомы, FAMMM-PC) из-за мутаций в CDKN2A ген-супрессор опухолей; аутосомно-рецессивный атаксия-телеангиэктазия и аутосомно-доминантно наследуемые мутации в BRCA2 и PALB2 гены; наследственный неполипозный рак толстой кишки (Синдром Линча); и семейный аденоматозный полипоз. PanNET были связаны с множественная эндокринная неоплазия 1 типа (MEN1) и фон Хиппель Линдау синдромы.[2][3][4]
- Хронический панкреатит риск почти утроился, и, как и в случае с диабетом, впервые возникший панкреатит может быть симптомом опухоли.[3] Риск рака поджелудочной железы у людей с семейным панкреатитом особенно высок.[3][39]
- Сахарный диабет является фактором риска рака поджелудочной железы и (как указано в Признаки и симптомы раздел) впервые возникший диабет также может быть ранним признаком заболевания. Люди, у которых был диагностирован диабет 2 типа на срок более 10 лет может иметь 50% повышенный риск по сравнению с людьми без диабета.[3]
- Специфический типы еды (в отличие от ожирения) явно не доказано, что они увеличивают риск рака поджелудочной железы.[2][41] Диетические факторы, для которых некоторые данные показывают немного повышенный риск, включают: обработанное мясо, красное мясо, а также мясо, приготовленное при очень высоких температурах (например, путем жарки, жарки или гриля).[41][42]
Алкоголь
Чрезмерное употребление алкоголя является основной причиной хронический панкреатит, который, в свою очередь, предрасполагает к раку поджелудочной железы, но значительные исследования не смогли убедительно установить потребление алкоголя как прямой фактор риска рака поджелудочной железы. В целом, связь неизменно слабая, и большинство исследований не обнаружили никакой связи с курением. сбивать с толку фактор. Доказательства более убедительны в отношении связи с пьянством, по крайней мере, шести порций в день.[3][43]
Патофизиология

Предрак

Считается, что экзокринный рак возникает из-за нескольких типов предраковый поражения в поджелудочной железе, но эти поражения не всегда прогрессируют до рака, и не все из них выявляются как побочный продукт все более широкого использования компьютерной томографии по другим причинам.[3] Помимо серозные цистаденомы поджелудочной железы, которые почти всегда являются доброкачественными, различают четыре типа предраковых поражений.
Первый - панкреатический интраэпителиальная неоплазия. Эти поражения представляют собой микроскопические аномалии поджелудочной железы и часто обнаруживаются в вскрытия людей без диагностированного рака. Эти поражения могут прогрессировать от от низкого до высокого класса а затем к опухоли. Более чем в 90% случаев всех классов имеется неисправный KRAS гена, а во 2 и 3 классах повреждают еще три гена - CDKN2A (p16), p53, и SMAD4 - встречаются все чаще.[2]
Второй тип - это внутрипротоковое папиллярное муцинозное новообразование (IPMN). Это макроскопические поражения, которые встречаются примерно у 2% всех взрослых. К 70 годам этот показатель возрастает примерно до 10%. Риск развития инвазивного рака у этих поражений составляет около 25%. Они могут иметь KRAS генные мутации (40–65% случаев) и в GNAS Альфа-субъединица Gs и RNF43, влияя на Сигнальный путь Wnt.[2] Даже при хирургическом удалении остается значительно повышенный риск последующего развития рака поджелудочной железы.[3]
Третий тип, муцинозное кистозное новообразование поджелудочной железы (MCN), в основном встречается у женщин и может оставаться доброкачественным или прогрессировать до рака.[44] Если эти поражения становятся большими, вызывают симптомы или имеют подозрительные признаки, их обычно можно успешно удалить хирургическим путем.[3]
Четвертый тип рака поджелудочной железы - это внутрипротоковое тубулопапиллярное новообразование. Этот тип был признан ВОЗ в 2010 г. и составляет около 1–3% всех новообразований поджелудочной железы. Средний возраст постановки диагноза составляет 61 год (от 35 до 78 лет). Около 50% этих поражений становятся инвазивными. Диагноз зависит от гистологии, поскольку эти поражения очень трудно отличить от других поражений ни по клиническим, ни по радиологическим признакам.[45]
Инвазивный рак
Генетические события, обнаруженные при аденокарциноме протоков, хорошо описаны и полностью секвенирование экзома было сделано для распространенных типов опухолей. В большинстве аденокарцином обнаружено, что каждый из четырех генов мутирован: KRAS (в 95% случаев), CDKN2A (также в 95%), TP53 (75%), и SMAD4 (55%). Последнее из них особенно связано с плохим прогнозом.[3] SWI / SNF мутации /удаления встречаются примерно в 10–15% аденокарцином.[2] Также были исследованы генетические изменения в некоторых других типах рака поджелудочной железы и предраковых поражениях.[3] Анализ транскриптомики и секвенирование мРНК для распространенных форм рака поджелудочной железы показали, что 75% человеческих генов выразил в опухолях примерно 200 генов более специфично экспрессируются при раке поджелудочной железы по сравнению с другими типами опухолей.[46][47]
ПанНЕТ
Гены, часто обнаруживаемые мутировавшими в PanNET, отличаются от генов экзокринного рака поджелудочной железы.[48] Например, KRAS мутация в норме отсутствует. Вместо наследственного MEN1 генные мутации вызывают Синдром МЕН1, при котором первичные опухоли возникают в двух или более эндокринные железы. Около 40–70% людей, рожденных с MEN1 мутации в конечном итоге развивают PanNet.[49] Другие гены, которые часто мутируют, включают: DAXX, mTOR, и ATRX.[26]
Диагностика

Симптомы аденокарциномы поджелудочной железы обычно не проявляются на ранних стадиях заболевания и не являются индивидуальными отличительными признаками заболевания.[3][12][29] Симптомы при постановке диагноза различаются в зависимости от расположения рака в поджелудочной железе, который анатомы делят (слева направо на большинстве диаграмм) на толстую голову, шею и сужающееся тело, заканчивающееся хвостом.
Независимо от локализации опухоли наиболее частым симптомом является необъяснимая потеря веса, которая может быть значительной. Значительное меньшинство (от 35% до 47%) людей, у которых диагностировано заболевание, испытывали тошноту, рвоту или чувство слабости. Опухоли в головке поджелудочной железы обычно также вызывают желтуху, боль, потеря аппетита, темная моча и светлый стул. Опухоли в теле и хвосте также обычно вызывают боль.[29]
Иногда у людей недавно развился атипичный диабет 2 типа, который трудно контролировать, - история недавнего, но необъяснимого воспаления кровеносных сосудов, вызванного сгустками крови (тромбофлебит) известный как Знак Труссо, или предыдущая атака панкреатит.[29] Врач может заподозрить рак поджелудочной железы, если начало диабета у человека старше 50 лет сопровождается типичными симптомами, такими как необъяснимая потеря веса, постоянная боль в животе или спине, несварение желудка, рвота или жирный кал.[12] Желтуха, сопровождающаяся безболезненным отеком желчный пузырь (известный как Знак Курвуазье) также может вызвать подозрение и помочь различать рак поджелудочной железы от камни в желчном пузыре.[50]
Медицинская визуализация методы, такие как компьютерная томография (Компьютерная томография) и эндоскопическое ультразвуковое исследование (EUS) используются как для подтверждения диагноза, так и для принятия решения о том, можно ли удалить опухоль хирургическим путем (ее "резектабельность").[12] На контрастная компьютерная томографиярак поджелудочной железы обычно показывает постепенно увеличивающееся поглощение радиоконтраста, а не быстрое вымывание, как в нормальной поджелудочной железе, или отсроченное вымывание, как при хроническом панкреатите.[51] Магнитно-резонансная томография и позитронно-эмиссионная томография также может использоваться,[2] и магнитно-резонансная холангиопанкреатография может быть полезно в некоторых случаях.[29] УЗИ брюшной полости менее чувствителен и не учитывает небольшие опухоли, но может определять рак, распространившийся на печень, и скопление жидкости в брюшной полости (асцит).[12] Его можно использовать для быстрого и дешевого первого обследования перед другими методами.[52]

Биопсия тонкая игла, часто под контролем эндоскопического ультразвука, может использоваться там, где есть неуверенность в диагнозе, но гистологический Для оперативного удаления опухоли диагноз обычно не требуется.[12]
Функциональные пробы печени может показать комбинацию результатов, указывающих на обструкцию желчных протоков (повышенная конъюгированный билирубин, γ-глутамилтранспептидаза и щелочная фосфатаза уровней). CA19-9 (углеводный антиген 19.9) представляет собой онкомаркер это часто повышается при раке поджелудочной железы. Однако ему не хватает чувствительность и специфичностьне в последнюю очередь потому, что 5% людей не имеют Льюис (а) антиген и не может производить CA19-9. Он имеет чувствительность 80% и специфичность 73% при обнаружении аденокарциномы поджелудочной железы и используется для следующих известных случаев, а не для диагностики.[2][12]
Гистопатология
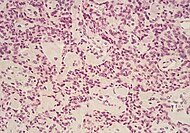
Наиболее распространенная форма рака поджелудочной железы (аденокарцинома) обычно характеризуется умеренно плохо дифференцированный железистые структуры при микроскопическом исследовании. Обычно существует значительная десмоплазия или образование плотного фиброзного строма или структурная ткань, состоящая из ряда типы клеток (включая миофибробласты, макрофаги, лимфоциты и тучные клетки) и депонированный материал (например, коллаген I типа и гиалуроновая кислота). Это создает микросреда опухоли это не хватает кровеносный сосуд (гиповаскулярный) и так кислород (опухолевая гипоксия).[2] Считается, что это предотвращает попадание в опухоль многих химиотерапевтических препаратов, поскольку это один из факторов, затрудняющих лечение рака.[2][3]
| Тип рака | Относительная заболеваемость[11] | Результаты микроскопии[11] | Микрофотография | Иммуногистохимия маркеры[11] | Генетические изменения[11] |
|---|---|---|---|---|---|
| Аденокарцинома протоков поджелудочной железы (PDAC) | 90% | Железы и десмоплазия | 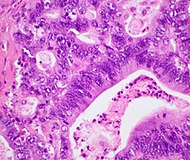 | ||
| Ацинарно-клеточная карцинома поджелудочной железы (АКК) | От 1% до 2% | Гранулированный вид | 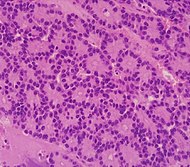 | ||
| Аденосквамозная карцинома | От 1% до 4%[53] | Сочетание железистых и плоскоклеточных клеток эпителиальный клетки. |  | Положительно для: Отрицательный для: | |
| Нейроэндокринная опухоль поджелудочной железы | 5% | Множественные гнезда опухолевых клеток | Гастринома | ||
| Предварительный рак ниже для сравнения: | |||||
| Предрак: Внутрипротоковое папиллярное муцинозное новообразование (IPMN) | 3% | Клетки муцинозного эпителия.[54] Рост в протоки поджелудочной железы.[55] | 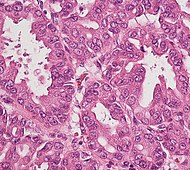 | ||
Постановка
Экзокринный рак
Рак поджелудочной железы обычно постановочный после компьютерная томография.[29] Наиболее широко используемой системой определения стадии рака поджелудочной железы является система, разработанная Американский объединенный комитет по раку (AJCC) вместе с Союз по международному контролю рака (UICC). Система стадирования AJCC-UICC определяет четыре основных стадии, от ранней до поздней стадии заболевания, на основе Классификация TNM из Тразмер умора, распространяется на лимфу Nоды и Mэтастаз.[56]
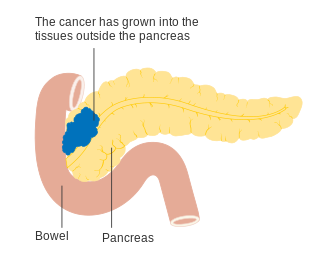
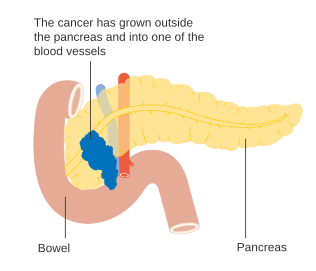
Чтобы принять решение о лечении, опухоли также делятся на три более широкие категории в зависимости от того, представляется ли возможным хирургическое удаление: таким образом, опухоли считаются «операбельными», «погранично резектабельными» или «неоперабельными».[57] Когда заболевание все еще находится на ранней стадии (стадии I и II AJCC-UICC), без распространения на крупные кровеносные сосуды или отдаленные органы, такие как печень или легкие, при желании пациента обычно может быть выполнено хирургическое удаление опухоли. для проведения этой серьезной операции и считается достаточно пригодным.[12] Система стадирования AJCC-UICC позволяет различать опухоли стадии III, которые считаются «погранично резектабельными» (когда хирургическое вмешательство технически возможно, поскольку чревная ось и верхняя брыжеечная артерия все еще бесплатны) и «неоперабельные» (из-за более распространенной болезни); с точки зрения более подробной классификации TNM эти две группы соответствуют T3 и T4 соответственно.[3]
- Стадия рака поджелудочной железы (классификация TNM)
Местнораспространенные аденокарциномы распространились на соседние органы, которые могут быть одним из следующих (примерно в порядке убывания частоты): двенадцатиперстная кишка, желудок, поперечная ободочная кишка, селезенка, надпочечник, или же почка. Очень часто они также распространяются на важную кровь или лимфатические сосуды и нервы, которые проходят близко к поджелудочной железе, что значительно усложняет операцию. Типичными местами распространения метастазов (стадия IV болезни) являются печень, брюшная полость и легкие, все из которых встречаются в 50% или более запущенных случаев.[58]
ПанНЕТ
В классификации опухолей пищеварительной системы ВОЗ от 2010 г. все нейроэндокринные опухоли поджелудочной железы (PanNET) классифицируются по трем категориям в зависимости от степени их поражения. клеточная дифференциация (от «NET G1» до плохо дифференцированного «NET G3»).[19] Соединенные штаты. Национальная комплексная онкологическая сеть рекомендует использовать ту же систему стадирования AJCC-UICC, что и аденокарцинома поджелудочной железы.[59]:52 При использовании этой схемы поэтапные результаты для PanNET отличаются от таковых для экзокринного рака.[60] Европейское общество нейроэндокринных опухолей предложило другую систему TNM для PanNET.[19]
Профилактика и скрининг
Помимо отказа от курения, Американское онкологическое общество рекомендует поддерживать здоровый вес и увеличивать потребление фруктов, овощей и цельное зерно, уменьшая потребление красного и обработанное мясо, хотя нет убедительных доказательств того, что это конкретно предотвратит или уменьшит рак поджелудочной железы.[61] Обзор исследований 2014 года показал, что существуют доказательства того, что потребление цитрусовые и куркумин снижение риска рака поджелудочной железы, хотя цельные зерна, возможно, дали положительный эффект, фолиевая кислота, селен, и нежареную рыбу.[43]
Для населения в целом скрининг больших групп не считается эффективным и может быть вредным с 2019 г.[62] хотя оцениваются более новые методы и проверка узконаправленных групп.[63][64] Тем не менее, регулярное обследование с помощью эндоскопического УЗИ и МРТ / КТ рекомендуется тем, кто имеет высокий риск по наследственной генетике.[4][52][64][65]
Управление
Экзокринный рак
Ключевой оценкой, которая проводится после постановки диагноза, является возможность хирургического удаления опухоли (см. Постановка), так как это единственное лекарство от рака. Может ли быть предложена хирургическая резекция, зависит от того, насколько распространился рак. Точное расположение опухоли также является важным фактором, и КТ может показать, как она связана с основными кровеносными сосудами, проходящими близко к поджелудочной железе. Также необходимо оценить общее состояние здоровья человека, хотя возраст сам по себе не является препятствием для операции.[3]
Химиотерапия и, в меньшей степени, лучевая терапия, вероятно, будут предложены большинству людей, независимо от того, возможна ли операция. Специалисты советуют, чтобы лечение рака поджелудочной железы находилось в руках врача. мультидисциплинарная команда включая специалистов по нескольким направлениям онкология, и поэтому лучше всего проводить в крупных центрах.[2][3]
Хирургия
Операция с целью излечения возможна только примерно в одной пятой (20%) новых случаев.[12] Хотя компьютерная томография помогает, на практике бывает сложно определить, можно ли полностью удалить опухоль (ее «операбельность»), и только во время операции может стать очевидным, что невозможно успешно удалить опухоль без повреждения других жизненно важных тканей. . Возможность хирургической резекции может быть предложена, зависит от различных факторов, в том числе от точной степени анатомического соседства или поражения венозный или же артериальный кровеносный сосуд,[2] а также хирургический опыт и тщательный анализ прогнозируемого послеоперационного восстановления.[66][67] Возраст человека не сам по себе повод не оперировать, а его общая статус производительности должен быть достаточным для крупной операции.[12]
Одной из конкретных характеристик, которые оцениваются, является обнадеживающее присутствие или обескураживающее отсутствие чистого слоя или плоскости жира, создающего барьер между опухолью и сосудами.[3] Традиционно оценивается близость опухоли к основным венозным или артериальным сосудам с точки зрения «опоры» (определяемой как опухоль, касающаяся не более половины окружности кровеносного сосуда без какого-либо жира для ее отделения), «оболочки» (когда опухоль охватывает большую часть окружности сосуда) или полное поражение сосуда.[68]:22 В некоторых случаях возможна резекция, включающая закрытые участки кровеносных сосудов,[69][70] особенно если предварительные неоадъювантная терапия возможно,[71][72][73] используя химиотерапию[67][68]:36[74] и / или лучевая терапия.[68]:29–30
Даже если операция кажется успешной, раковые клетки часто обнаруживаются по краям ("поля") удаленных тканей, когда патолог исследует их под микроскопом (это всегда будет сделано), что указывает на то, что рак не был удален полностью.[2] Более того, раковые стволовые клетки обычно не очевидны под микроскопом, и если они присутствуют, они могут продолжать развиваться и распространяться.[75][76] Исследовательский лапароскопия (небольшая хирургическая процедура под контролем камеры) может быть проведена, чтобы получить более четкое представление об исходе полной операции.[77]
При раке с поражением головки поджелудочной железы Процедура Уиппла это наиболее часто применяемое лечебное хирургическое лечение. Это серьезная операция, которая включает удаление головки поджелудочной железы и дуоденума вместе («панкреатодуоденэктомия»), обход для еды из желудка в тощая кишка («гастроэюностомия») и прикрепление петли тощей кишки к пузырный проток для отвода желчи («холецисто-ейностомия»). Это может быть выполнено, только если человек может пережить серьезную операцию, и если рак локализован без вторжения в местные структуры или метастазирования. Следовательно, это может быть выполнено только в меньшинстве случаев. Рак хвоста поджелудочной железы можно удалить с помощью процедуры, известной как дистальная панкреатэктомия, что часто также влечет за собой удаление селезенки.[2][3] В настоящее время это часто можно сделать с помощью малоинвазивная хирургия.[2][3]
Хотя лечебная хирургия больше не влечет за собой очень высокий уровень смертности, имевший место до 1980-х годов, значительную часть людей (около 30–45%) по-прежнему необходимо лечить от послеоперационных заболеваний, которые не вызваны самим раком. Самый распространенный осложнение хирургии затрудненное опорожнение желудка.[3] Некоторые более ограниченные хирургические процедуры также могут использоваться для облегчения симптомов (см. Паллиативная помощь): например, если рак поражает или сдавливает двенадцатиперстную кишку или двоеточие. В таких случаях операция шунтирования может преодолеть обструкцию и улучшить качество жизни, но не предназначена для лечения.[12]
Химиотерапия
После операции, адъювант химиотерапия с гемцитабин или же 5-ФУ могут быть предложены, если человек достаточно подходитпосле периода восстановления от одного до двух месяцев.[4][52] У людей, которые не подходят для лечебной хирургии, химиотерапия может использоваться для продления жизни или улучшения его качество.[3] Перед операцией неоадъювантный химиотерапия или химиолучевая терапия может использоваться в случаях, которые считаются «пограничными операбельными» (см. Постановка), чтобы снизить риск рака до уровня, при котором операция может принести пользу. В других случаях неоадъювантной терапии остается спорным, так как она задерживает операцию.[3][4][78]
Гемцитабин был одобрен в США. Управление по контролю за продуктами и лекарствами (FDA) в 1997 году, после клиническое испытание сообщили об улучшении качества жизни и 5-недельном улучшении средняя продолжительность выживания у людей с запущенным раком поджелудочной железы.[79] Это был первый химиотерапевтический препарат, одобренный Управлением по контролю за продуктами и лекарствами США, в первую очередь, в качестве конечной точки клинических испытаний по предотвращению выживания.[80] Химиотерапия с использованием одного гемцитабина была стандартом в течение примерно десяти лет, так как ряд испытаний, тестирующих его в сочетании с другими препаратами, не продемонстрировали значительно лучших результатов. Однако комбинация гемцитабина с эрлотиниб Было обнаружено, что он незначительно увеличивает выживаемость, и в 2005 году эрлотиниб был лицензирован FDA для использования при раке поджелудочной железы.[81]
В ФОЛЬФИРИНОКС режим химиотерапии Было установлено, что использование четырех препаратов более эффективно, чем гемцитабин, но со значительными побочными эффектами, и поэтому подходит только для людей с хорошей работоспособностью. Это также верно для паклитаксел, связанный с белком (наб-паклитаксел), который был лицензирован FDA в 2013 году для использования с гемцитабином при раке поджелудочной железы.[82] К концу 2013 года и FOLFIRINOX, и наб-паклитаксел с гемцитабином считались хорошим выбором для тех, кто способен переносить побочные эффекты, а гемцитабин оставался эффективным вариантом для тех, кто этого не делал. Ожидается очное испытание двух новых вариантов, а испытания других вариантов продолжаются. Однако изменения последних нескольких лет увеличили время выживания лишь на несколько месяцев.[79] Клинические испытания часто проводятся для новых адъювантных методов лечения.[4]
Лучевая терапия
Роль лучевая терапия как вспомогательное (адъювантное) лечение после потенциально излечивающей хирургии вызывает споры с 1980-х годов.[3] В Европейское общество медицинской онкологии рекомендует использовать адъювантную лучевую терапию только для людей, участвующих в клинических испытаниях.[52] However, there is a continuing tendency for clinicians in the US to be more ready to use adjuvant radiotherapy than those in Europe. Many clinical trials have tested a variety of treatment combinations since the 1980s, but have failed to settle the matter conclusively.[3][4]
Radiotherapy may form part of treatment to attempt to shrink a tumor to a resectable state, but its use on unresectable tumors remains controversial as there are conflicting results from clinical trials. The preliminary results of one trial, presented in 2013, "markedly reduced enthusiasm" for its use on locally advanced tumors.[2]
PanNETs
Treatment of PanNETs, including the less common злокачественный types, may include a number of approaches.[59][83][84][85] Some small tumors of less than 1 cm. that are identified incidentally, for example on a CT scan performed for other purposes, may be followed by watchful waiting.[59] This depends on the assessed risk of surgery which is influenced by the site of the tumor and the presence of other medical problems.[59] Tumors within the pancreas only (localized tumors), or with limited metastases, for example to the liver, may be removed by surgery. The type of surgery depends on the tumor location, and the degree of spread to lymph nodes.[19]
For localized tumors, the surgical procedure may be much less extensive than the types of surgery used to treat pancreatic adenocarcinoma described above, but otherwise surgical procedures are similar to those for exocrine tumors. The range of possible outcomes varies greatly; some types have a very high survival rate after surgery while others have a poor outlook. As all this group are rare, guidelines emphasize that treatment should be undertaken in a specialized center.[19][26] Use of liver transplantation may be considered in certain cases of liver metastasis.[86]
For functioning tumors, the somatostatin analog class of medications, such as octreotide, can reduce the excessive production of hormones.[19] Ланреотид can slow tumor growth.[87] If the tumor is not amenable to surgical removal and is causing symptoms, таргетная терапия с everolimus или же сунитиниб can reduce symptoms and slow progression of the disease.[26][88][89] Стандарт цитотоксический chemotherapy is generally not very effective for PanNETs, but may be used when other drug treatments fail to prevent the disease from progressing,[26] or in poorly differentiated PanNET cancers.[90]
Radiation therapy is occasionally used if there is pain due to anatomic extension, such as метастаз to bone. Some PanNETs absorb specific пептиды or hormones, and these PanNETs may respond to ядерная медицина therapy with радиоактивно меченый peptides or hormones such as iobenguane (iodine-131-MIBG).[91][92][93][94] Радиочастотная абляция (RFA), криоабляция, и hepatic artery embolization также могут быть использованы.[95][96]
Паллиативная помощь
Паллиативная помощь is medical care which focuses on treatment of symptoms from serious illness, such as cancer, and improving quality of life.[97] Because pancreatic adenocarcinoma is usually diagnosed after it has progressed to an advanced stage, palliative care as a treatment of symptoms is often the only treatment possible.[98]
Palliative care focuses not on treating the underlying cancer, but on treating symptoms such as боль or nausea, and can assist in decision-making, including when or if хоспис will be beneficial.[99] Pain can be managed with medications such as опиоиды or through procedural intervention, by a блокада нерва на чревное сплетение (КПБ). This alters or, depending on the technique used, destroys the nerves that transmit pain from the abdomen. CPB is a safe and effective way to reduce the pain, which generally reduces the need to use opioid painkillers, which have significant negative side effects.[3][100]
Other symptoms or complications that can be treated with palliative surgery are obstruction by the tumor of the intestines or желчные протоки. For the latter, which occurs in well over half of cases, a small metal tube called a стент may be inserted by endoscope to keep the ducts draining.[29] Palliative care can also help treat depression that often comes with the diagnosis of pancreatic cancer.[3]
Both surgery and advanced inoperable tumors often lead to пищеварительная система disorders from a lack of the exocrine products of the pancreas (exocrine insufficiency). These can be treated by taking панкреатин which contains manufactured pancreatic enzymes, and is best taken with food.[12] Difficulty in emptying the stomach (delayed gastric emptying) is common and can be a serious problem, involving hospitalization. Treatment may involve a variety of approaches, including draining the stomach by nasogastric aspiration and drugs called ингибиторы протонной помпы или же Н2 антагонисты, which both reduce production of Желудочный сок.[12] Medications like метоклопрамид can also be used to clear stomach contents.
Результаты
| Clinical stage | U.S. five-year survival (%) for 1992–1998 diagnoses | |
|---|---|---|
| Exocrine pancreatic cancer | Neuroendocrine treated with surgery | |
| IA / I | 14 | 61 |
| IB | 12 | |
| IIA / II | 7 | 52 |
| МИБ | 5 | |
| III | 3 | 41 |
| IV | 1 | 16 |
Pancreatic adenocarcinoma and the other less common exocrine cancers have a very poor прогноз, as they are normally diagnosed at a late stage when the cancer is already locally advanced or has spread to other parts of the body.[2] Outcomes are much better for PanNETs: Many are benign and completely without clinical symptoms, and even those cases not treatable with surgery have an average пятилетняя выживаемость of 16%,[57] although the outlook varies considerably according to the type.[28]
For locally advanced and метастатический pancreatic adenocarcinomas, which together represent over 80% of cases, numerous trials comparing chemotherapy regimes have shown increased survival times, but not to more than one year.[2][79] Overall five-year survival for pancreatic cancer in the US has improved from 2% in cases diagnosed in 1975–1977, and 4% in 1987–1989 diagnoses, to 6% in 2003–2009.[101] In the less than 20% of cases of pancreatic adenocarcinoma with a diagnosis of a localized and small cancerous growth (less than 2 cm in Stage T1), about 20% of Americans survive to five years.[17]
About 1500 genes are linked to outcomes in pancreatic adenocarcinoma. These include both unfavorable genes, where high expression is related to poor outcome, for example C-Met и MUC-1, and favorable genes where high expression is associated with better survival, for example the фактор транскрипции PELP1.[46][47]
Распределение
In 2015, pancreatic cancers of all types resulted in 411,600 deaths globally.[8] In 2014, an estimated 46,000 people in the US are expected to be diagnosed with pancreatic cancer and 40,000 to die of it.[2] Although it accounts for only 2.5% of new cases, pancreatic cancer is responsible for 6% of cancer deaths each year.[102] It is the seventh highest cause of death from cancer worldwide.[10] Pancreatic cancer is the fifth most common cause of death from cancer in the United Kingdom,[15] and the third most common in the United States.[16]
Globally pancreatic cancer is the 11th most common cancer in women and the 12th most common in men.[10] The majority of recorded cases occur in развитые страны.[10] People from the United States have an average риск жизни of about 1 in 67 (or 1.5%) of developing the disease,[103] slightly higher than the figure for the UK.[104] The disease is more common in men than women,[2][10] though the difference in rates has narrowed over recent decades, probably reflecting earlier increases in female smoking. In the United States the risk for афро-американцы is over 50% greater than for белые, but the rates in Africa and Восточная Азия are much lower than those in North America or Europe. The United States, Central, and eastern Europe, and Аргентина и Уругвай all have high rates.[10]
PanNETs
Ежегодный заболеваемость of clinically recognized PanNETs is low (about 5 per one million person-years) and is dominated by the non-functioning types.[23] Somewhere between 45% and 90% of PanNETs are thought to be of the non-functioning types.[19][26] Исследования вскрытия имеют uncovered small PanNETs rather frequently, suggesting that the распространенность of tumors that remain inert and бессимптомный may be relatively high.[26] Overall PanNETs are thought to account for about 1 to 2% of all pancreatic tumors.[23] The definition and classification of PanNETs has changed over time, affecting what is known about their эпидемиология and clinical relevance.[48]
История
Recognition and diagnosis
The earliest recognition of pancreatic cancer has been attributed to the 18th-century Italian scientist Джованни Баттиста Морганьи, the historical father of modern-day anatomic pathology, who claimed to have traced several cases of cancer in the pancreas. Many 18th and 19th-century physicians were skeptical about the existence of the disease, given the similar appearance of pancreatitis. Немного отчеты о случаях were published in the 1820s and 1830s, and a genuine гистопатологический diagnosis was eventually recorded by the American clinician Jacob Mendes Da Costa, who also doubted the reliability of Morgagni's interpretations. By the start of the 20th century, cancer of the head of the pancreas had become a well-established diagnosis.[105]
Regarding the recognition of PanNETs, the possibility of cancer of the islet cells was initially suggested in 1888. The first case of hyperinsulinism due to a tumor of this type was reported in 1927. Recognition of a non-insulin-secreting type of PanNET is generally ascribed to the American surgeons, R. M. Zollinger and E. H. Ellison, who gave their names to Синдром Золлингера-Эллисона, after postulating the existence of a gastrin-secreting pancreatic tumor in a report of two cases of unusually severe peptic ulcers published in 1955.[105] In 2010, the WHO recommended that PanNETs be referred to as "neuroendocrine" rather than "endocrine" tumors.[25]
Small precancerous neoplasms for many pancreatic cancers are being detected at greatly increased rates by modern medical imaging. One type, the intraductal papillary mucinous neoplasm (IPMN) was first described by Japanese researchers in 1982. It was noted in 2010 that: "For the next decade, little attention was paid to this report; however, over the subsequent 15 years, there has been a virtual explosion in the recognition of this tumor."[58]
Хирургия
The first reported partial pancreaticoduodenectomy was performed by the Italian surgeon Алессандро Кодивилья in 1898, but the patient only survived 18 days before succumbing to complications. Early operations were compromised partly because of mistaken beliefs that people would die if their duodenum were removed, and also, at first, if the flow of pancreatic juices stopped. Later it was thought, also mistakenly, that the pancreatic duct could simply be tied up without serious adverse effects; in fact, it will very often leak later on. In 1907–1908, after some more unsuccessful operations by other surgeons, experimental procedures were tried on corpses by French surgeons.[106]
In 1912 the German surgeon Вальтер Кауш was the first to remove large parts of the duodenum and pancreas together (в блоке). This was in Breslau, now Вроцлав в Польше. In 1918 it was demonstrated, in operations on dogs, that it is possible to survive even after complete removal of the duodenum, but no such result was reported in human surgery until 1935, when the American surgeon Allen Oldfather Whipple published the results of a series of three operations at Колумбийская пресвитерианская больница в Нью-Йорке. Only one of the patients had the duodenum entirely removed, but he survived for two years before dying of metastasis to the liver. The first operation was unplanned, as cancer was only discovered in the operating theater. Whipple's success showed the way for the future, but the operation remained a difficult and dangerous one until recent decades. He published several refinements to his procedure, including the first total removal of the duodenum in 1940, but he only performed a total of 37 operations.[106]
The discovery in the late 1930s that витамин К предотвратить bleeding with jaundice, и развитие переливание крови as an everyday process, both improved post-operative survival,[106] but about 25% of people never left hospital alive as late as the 1970s.[107] In the 1970s a group of American surgeons wrote urging that the procedure was too dangerous and should be abandoned. Since then outcomes in larger centers have improved considerably, and mortality from the operation is often less than 4%.[21]
In 2006 a report was published of a series of 1,000 consecutive pancreatico-duodenectomies performed by a single surgeon from Больница Джона Хопкинса between 1969 and 2003. The rate of these operations had increased steadily over this period, with only three of them before 1980, and the median operating time reduced from 8.8 hours in the 1970s to 5.5 hours in the 2000s, and mortality within 30 days or in hospital was only 1%.[106][107] Another series of 2,050 operations at the Массачусетская больница общего профиля between 1941 and 2011 showed a similar picture of improvement.[108]
Направления исследований
Early-stage research on pancreatic cancer includes studies of генетика and early detection, treatment at different cancer stages, surgical strategies, and targeted therapies, such as inhibition of факторы роста, immune therapies, и вакцина.[39][109][110][111][112]
A key question is the timing of events as the disease develops and progresses – particularly the role of сахарный диабет,[109][31] and how and when the disease spreads.[113] The knowledge that new onset of diabetes can be an early sign of the disease could facilitate timely diagnosis and профилактика if a workable screening strategy can be developed.[109][31][114][115] The European Registry of Hereditary Pancreatitis and Familial Pancreatic Cancer (EUROPAC) trial is aiming to determine whether regular screening is appropriate for people with a family history of the disease.[116]
Keyhole surgery (лапароскопия) скорее, чем Процедура Уиппла, particularly in terms of recovery time, is being evaluated.[117] Irreversible electroporation is a relatively novel абляция technique with potential for downstaging and prolonging survival in persons with locally advanced disease, especially for tumors in proximity to peri-pancreatic vessels without risk of vascular trauma.[118][119]
Efforts are underway to develop new drugs, including those targeting molecular mechanisms for cancer onset,[120][121] стволовые клетки,[76] и распространение клеток.[121][122] A further approach involves the use of иммунотерапия, Такие как oncolytic viruses.[123] Galectin-specific mechanisms of the микросреда опухоли находятся в стадии изучения.[124]
Смотрите также
- Рак желудочно-кишечного тракта
- Сеть действий по борьбе с раком поджелудочной железы (organization in the US)
- Pancreatic Cancer Action (organization in the UK)
- Фонд Люстгартена по исследованию рака поджелудочной железы (organization in the US)
- List of people diagnosed with pancreatic cancer
Рекомендации
- ^ а б c d е ж грамм "Pancreatic Cancer Treatment (PDQ®) Patient Version". Национальный институт рака. Национальные институты здоровья. 17 апреля 2014 г. В архиве из оригинала 5 июля 2014 г.. Получено 8 июн 2014.
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае аф Ryan DP, Hong TS, Bardeesy N (September 2014). "Pancreatic adenocarcinoma". Медицинский журнал Новой Англии. 371 (11): 1039–49. Дои:10.1056/NEJMra1404198. PMID 25207767.
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае аф аг Wolfgang CL, Herman JM, Laheru DA, Klein AP, Erdek MA, Fishman EK, Hruban RH (September 2013). "Recent progress in pancreatic cancer". КА: Журнал онкологических заболеваний для клиницистов. 63 (5): 318–48. Дои:10.3322/caac.21190. ЧВК 3769458. PMID 23856911.
- ^ а б c d е ж грамм час я j Vincent A, Herman J, Schulick R, Hruban RH, Goggins M (August 2011). "Pancreatic cancer" (PDF). Ланцет. 378 (9791): 607–20. Дои:10.1016/S0140-6736(10)62307-0. ЧВК 3062508. PMID 21620466. Архивировано из оригинал (PDF) on 12 January 2015.
- ^ а б "Can pancreatic cancer be prevented?". Американское онкологическое общество. 11 июня 2014 г. В архиве из оригинала 13 ноября 2014 г.. Получено 13 ноября 2014.
- ^ а б "Cancer Facts & Figures 2010" (PDF). Американское онкологическое общество. 2010. Архивировано с оригинал (PDF) 14 января 2015 г.. Получено 5 декабря 2014. См. Стр. 4 for incidence estimates, and p. 19 for survival percentages.
- ^ Вос Т., Аллен С., Арора М., Барбер Р.М., Бхутта З.А., Браун А. и др. (Соавторы исследования ГББ 2015 по заболеваемости и распространенности заболеваний и травм) (октябрь 2016 г.). «Глобальная, региональная и национальная заболеваемость, распространенность и годы, прожитые с инвалидностью для 310 заболеваний и травм, 1990–2015 годы: систематический анализ для исследования глобального бремени болезней 2015». Ланцет. 388 (10053): 1545–1602. Дои:10.1016/S0140-6736(16)31678-6. ЧВК 5055577. PMID 27733282.
- ^ а б c Ван Х., Нагави М., Аллен С., Барбер Р.М., Бхутта З.А., Картер А. и др. (ГББ 2015 г. Смертность и причины смерти соавторов) (октябрь 2016 г.). «Ожидаемая продолжительность жизни на глобальном, региональном и национальном уровнях, смертность от всех причин и смертность от конкретных причин для 249 причин смерти, 1980–2015 гг .: систематический анализ для исследования глобального бремени болезней 2015 г.». Ланцет. 388 (10053): 1459–1544. Дои:10.1016 / с0140-6736 (16) 31012-1. ЧВК 5388903. PMID 27733281.
- ^ "What is Cancer? Defining Cancer". Национальный институт рака, Национальные институты здоровья. 7 March 2014. В архиве из оригинала 25 июня 2014 г.. Получено 5 декабря 2014.
- ^ а б c d е ж грамм час я j k л м п о п q р s т World Cancer Report. Всемирная организация здоровья. 2014. Chapter 5.7. ISBN 978-92-832-0429-9.
- ^ а б c d е Unless otherwise specified in boxes, reference is: Pishvaian MJ, Brody JR (March 2017). "Therapeutic Implications of Molecular Subtyping for Pancreatic Cancer". Онкология. 31 (3): 159–66, 168. PMID 28299752.
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Bond-Smith G, Banga N, Hammond TM, Imber CJ (May 2012). "Pancreatic adenocarcinoma". BMJ. 344 (may16 1): e2476. Дои:10.1136/bmj.e2476. PMID 22592847. S2CID 206894869.
- ^ "Draft Recommendation Statement: Pancreatic Cancer: Screening – US Preventive Services Task Force". www.uspreventiveservicestaskforce.org. Получено 11 февраля 2019.
- ^ Bardou M, Le Ray I (December 2013). "Treatment of pancreatic cancer: A narrative review of cost-effectiveness studies". Лучшие практики и исследования. Clinical Gastroenterology. 27 (6): 881–92. Дои:10.1016/j.bpg.2013.09.006. PMID 24182608.
- ^ а б "Cancer facts and figures – Why we exist – Pancreatic Cancer Research Fund". www.pcrf.org.uk. Получено 5 апреля 2019.
- ^ а б "Pancreatic Cancer – Cancer Stat Facts". SEER. Получено 4 апреля 2019.
- ^ а б "Pancreatic Cancer Treatment (PDQ®) Health Professional Version". Национальный институт рака. Национальные институты здоровья. 21 февраля 2014 г. В архиве из оригинала 22 октября 2014 г.. Получено 24 ноября 2014. "The highest cure rate occurs if the tumor is truly localized to the pancreas; however, this stage of disease accounts for less than 20% of cases. In cases with localized disease and small cancers (<2 cm) with no lymph-node metastases and no extension beyond the capsule of the pancreas, complete surgical resection is still associated with a low actuarial five-year survival rate of 18% to 24%."
- ^ Harris RE (2013). "Epidemiology of pancreatic cancer". Эпидемиология хронических заболеваний. Джонс и Бартлетт. С. 181–190. ISBN 978-0-7637-8047-0. В архиве из оригинала от 24 июня 2016 г.
- ^ а б c d е ж грамм Öberg K, Knigge U, Kwekkeboom D, Perren A, et al. (ESMO Guidelines Working Group) (October 2012). "Neuroendocrine gastro-entero-pancreatic tumors: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up". Анналы онкологии. 23 Suppl 7 (suppl 7): vii124-30. Дои:10.1093/annonc/mds295. PMID 22997445. (Таблица 5 outlines the proposed TNM staging system for PanNETs.)
- ^ Handbook of Pancreatic Cancer. Нью-Йорк: Спрингер. 2009. с. 288. ISBN 978-0-387-77497-8. В архиве с оригинала 10 сентября 2017 г.. Получено 12 июн 2016.
- ^ а б Govindan R (2011). DeVita, Hellman, and Rosenberg's Cancer: Cancer: Principles & Practice of Oncology (9-е изд.). Липпинкотт Уильямс и Уилкинс. Chapter 35: Cancer of the Pancreas: Surgical Management. ISBN 978-1-4511-0545-2. Online edition, with updates to 2014
- ^ а б c Tobias JS, Hochhauser D (2014). Cancer and its Management (7-е изд.). п. 297. ISBN 978-1-118-46871-5.
- ^ а б c "Types of Pancreas Tumors". The Sol Goldman Pancreas Cancer Research Center. Johns Hopkins Medicine. 2012 г. В архиве from the original on 8 October 2014. Получено 18 ноября 2014.
- ^ Farrell JJ, Fernández-del Castillo C (June 2013). "Pancreatic cystic neoplasms: management and unanswered questions". Гастроэнтерология. 144 (6): 1303–15. Дои:10.1053/j.gastro.2013.01.073. PMID 23622140.
- ^ а б c The PanNET denomination is in line with ВОЗ guidelines for the classification of tumors of the digestive system "WHO classification of tumours of the digestive system – NLM Catalog – NCBI". В архиве из оригинала 9 сентября 2017 г.. Получено 7 сентября 2017. published in 2010. Historically, PanNETs have also been referred to by a variety of terms, and are still commonly called "pancreatic endocrine tumors". Видеть: Klimstra DS, Modlin IR, Coppola D, Lloyd RV, Suster S (August 2010). "The pathologic classification of neuroendocrine tumors: a review of nomenclature, grading, and staging systems". Поджелудочная железа. 39 (6): 707–12. Дои:10.1097/MPA.0b013e3181ec124e. PMID 20664470. S2CID 3735444.
- ^ а б c d е ж грамм час Burns WR, Edil BH (March 2012). "Neuroendocrine pancreatic tumors: guidelines for management and update". Современные варианты лечения в онкологии. 13 (1): 24–34. Дои:10.1007/s11864-011-0172-2. PMID 22198808. S2CID 7329783.
- ^ В Рубрики медицинской тематики indexing system refers to "islet cell carcinoma", which is subdivided into gastrinoma, glucagonoma, соматостатинома, и VIPoma. See: 2014 MeSH tree at "Pancreatic Neoplasms [C04.588.322.475]" В архиве 19 марта 2016 г. Wayback Machine 16 октября 2014 г.
- ^ а б "Islet Cell Tumors of the Pancreas / Endocrine Neoplasms of the Pancreas". The Sol Goldman Pancreas Cancer Research Center. Johns Hopkins Medicine. 2012 г. В архиве из оригинала 5 января 2015 г.. Получено 5 января 2015.
- ^ а б c d е ж грамм De La Cruz MS, Young AP, Ruffin MT (April 2014). "Diagnosis and management of pancreatic cancer". Американский семейный врач. 89 (8): 626–32. PMID 24784121.
- ^ а б Alberts SR, Goldberg RM (2009). "Chapter 9: Gastrointestinal tract cancers". В Casciato DA, Territo MC (ред.). Manual of clinical oncology. Липпинкотт Уильямс и Уилкинс. стр.188–236. ISBN 978-0-7817-6884-9.
- ^ а б c Pannala R, Basu A, Petersen GM, Chari ST (January 2009). "New-onset diabetes: a potential clue to the early diagnosis of pancreatic cancer". Ланцет. Онкология. 10 (1): 88–95. Дои:10.1016/S1470-2045(08)70337-1. ЧВК 2795483. PMID 19111249.
- ^ "Chapter 15; Pancreas" (PDF). Manual for Staging of Cancer (2-е изд.). American Joint Committee on Cancer. С. 95–98. В архиве (PDF) из оригинала от 29 ноября 2014 г. См. Стр. 95 for citation regarding "... lesser degree of involvement of bones and brain and other anatomical sites."
- ^ Sperti C, Moletta L, Patanè G (October 2014). "Metastatic tumors to the pancreas: The role of surgery". World Journal of Gastrointestinal Oncology. 6 (10): 381–92. Дои:10.4251/wjgo.v6.i10.381. ЧВК 4197429. PMID 25320654.
- ^ "Causes of pancreatic cancer". NHS Choices. National Health Service, England. 7 October 2014. В архиве из оригинала от 6 ноября 2014 г.. Получено 5 декабря 2014.
- ^ Anderson, Laura N.; Коттеркио, Мишель; Gallinger, Steven (5 February 2009). "Lifestyle, dietary, and medical history factors associated with pancreatic cancer risk in Ontario, Canada". Cancer Causes & Control. 20 (6): 825–834. Дои:10.1007/s10552-009-9303-5. ISSN 0957-5243. Получено 20 ноября 2020.
- ^ Bosetti C, Lucenteforte E, Silverman DT, Petersen G, Bracci PM, Ji BT, et al. (Июль 2012 г.). "Cigarette smoking and pancreatic cancer: an analysis from the International Pancreatic Cancer Case-Control Consortium (Panc4)". Анналы онкологии. 23 (7): 1880–8. Дои:10.1093/annonc/mdr541. ЧВК 3387822. PMID 22104574.
- ^ De Rubeis, Vanessa; Коттеркио, Мишель; Smith, Brendan T.; Griffith, Lauren E.; Borgida, Ayelet; Gallinger, Steven; Cleary, Sean; Anderson, Laura N. (1 September 2019). "Trajectories of body mass index, from adolescence to older adulthood, and pancreatic cancer risk; a population-based case–control study in Ontario, Canada". Cancer Causes & Control. 30 (9): 955–966. Дои:10.1007/s10552-019-01197-9. ISSN 1573-7225. Получено 20 ноября 2020.
- ^ Peters ML, Tseng JF, Miksad RA (July 2016). "Genetic Testing in Pancreatic Ductal Adenocarcinoma: Implications for Prevention and Treatment". Клиническая терапия. 38 (7): 1622–35. Дои:10.1016/j.clinthera.2016.03.006. PMID 27041411.
- ^ а б c Reznik R, Hendifar AE, Tuli R (2014). "Genetic determinants and potential therapeutic targets for pancreatic adenocarcinoma". Границы физиологии. 5: 87. Дои:10.3389/fphys.2014.00087. ЧВК 3939680. PMID 24624093.
- ^ Greenhalf W, Grocock C, Harcus M, Neoptolemos J (May 2009). "Screening of high-risk families for pancreatic cancer". Pancreatology. 9 (3): 215–22. Дои:10.1159/000210262. PMID 19349734. S2CID 29100310.
- ^ а б "Cancer Facts and Figures 2014" (PDF). Американское онкологическое общество. В архиве (PDF) из оригинала 18 декабря 2014 г.. Получено 5 января 2015., п. 19, "Though evidence is still accumulating, consumption of red or processed meat, or meat cooked at very high temperatures, may немного increase risk."
- ^ Larsson SC, Wolk A (January 2012). "Red and processed meat consumption and risk of pancreatic cancer: meta-analysis of prospective studies". Британский журнал рака. 106 (3): 603–7. Дои:10.1038/bjc.2011.585. ЧВК 3273353. PMID 22240790.
- ^ а б Pericleous M, Rossi RE, Mandair D, Whyand T, Caplin ME (January 2014). "Nutrition and pancreatic cancer". Противораковые исследования. 34 (1): 9–21. PMID 24403441.
- ^ Delpu Y, Hanoun N, Lulka H, Sicard F, Selves J, Buscail L, et al. (Март 2011 г.). "Genetic and epigenetic alterations in pancreatic carcinogenesis". Текущая геномика. 12 (1): 15–24. Дои:10.2174/138920211794520132. ЧВК 3129039. PMID 21886451.
- ^ Rooney SL, Shi J (October 2016). "Intraductal Tubulopapillary Neoplasm of the Pancreas: An Update From a Pathologist's Perspective". Архив патологии и лабораторной медицины. 140 (10): 1068–73. Дои:10.5858/arpa.2016-0207-RA. PMID 27684978.
- ^ а б "The human pathology proteome in pancreatic cancer – The Human Protein Atlas". www.proteinatlas.org. Получено 28 сентября 2017.
- ^ а б Uhlen M, Zhang C, Lee S, Sjöstedt E, Fagerberg L, Bidkhori G, et al. (Август 2017 г.). "A pathology atlas of the human cancer transcriptome". Наука. 357 (6352): eaan2507. Дои:10.1126/science.aan2507. PMID 28818916.
- ^ а б Lewis MA, Yao JC (February 2014). "Molecular pathology and genetics of gastrointestinal neuroendocrine tumours". Current Opinion in Endocrinology, Diabetes and Obesity. 21 (1): 22–7. Дои:10.1097/MED.0000000000000033. PMID 24310147. S2CID 31094880.
- ^ Thakker RV, Newey PJ, Walls GV, Bilezikian J, Dralle H, Ebeling PR, et al. (Сентябрь 2012 г.). "Clinical practice guidelines for multiple endocrine neoplasia type 1 (MEN1)". Журнал клинической эндокринологии и метаболизма. 97 (9): 2990–3011. Дои:10.1210/jc.2012-1230. PMID 22723327.
- ^ Fitzgerald JE, White MJ, Lobo DN (April 2009). "Courvoisier's gallbladder: law or sign?". Всемирный журнал хирургии. 33 (4): 886–91. Дои:10.1007 / s00268-008-9908-y. PMID 19190960. S2CID 21799234.
- ^ Piraka C, Scheiman JM (September 2011). "New diagnostic imaging modalities for pancreatic disease". Текущее мнение в гастроэнтерологии. 27 (5): 475–80. Дои:10.1097/MOG.0b013e328349e30c. PMID 21743318. S2CID 38963685.
- ^ а б c d Seufferlein T, Bachet JB, Van Cutsem E, Rougier P (October 2012). "Pancreatic adenocarcinoma: ESMO-ESDO Clinical Practice Guidelines for diagnosis, treatment and follow-up". Анналы онкологии. 23 Suppl 7: vii33-40. Дои:10.1093/annonc/mds224. PMID 22997452.
- ^ Skafida E, Grammatoglou X, Glava C, Zissis D, Paschalidis N, Katsamagkou E, et al. (Февраль 2010 г.). "Adenosquamous carcinoma of the pancreas: a case report". Журнал случаев. 3 (1): 41. Дои:10.1186/1757-1626-3-41. ЧВК 2825199. PMID 20205828.
- ^ Diana Agostini-Vulaj. "Pancreas – Exocrine tumors / carcinomas – Intraductal papillary mucinous neoplasm (IPMN)". Очертания патологии. Topic Completed: 1 July 2018. Revised: 9 March 2020
- ^ Adsay V, Mino-Kenudson M, Furukawa T, Basturk O, Zamboni G, Marchegiani G, et al. (Январь 2016 г.). "Pathologic Evaluation and Reporting of Intraductal Papillary Mucinous Neoplasms of the Pancreas and Other Tumoral Intraepithelial Neoplasms of Pancreatobiliary Tract: Recommendations of Verona Consensus Meeting". Анналы хирургии. 263 (1): 162–77. Дои:10.1097/SLA.0000000000001173. ЧВК 4568174. PMID 25775066.
- ^ Cascinu S, Falconi M, Valentini V, Jelic S (May 2010). "Pancreatic cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up". Анналы онкологии. 21 Suppl 5 (Supplement 5): v55-8. Дои:10.1093/annonc/mdq165. PMID 20555103.
- ^ а б c "Staging of pancreatic cancer". Американское онкологическое общество. 11 июня 2014 г.. Получено 29 сентября 2014.
- ^ а б Zyromski NJ, Nakeeb A, Lillemoe KD (2010). Silberman H, Silberman AW (eds.). Principles and practice of surgical oncology : multidisciplinary approach to difficult problems (онлайн-изд.). Philadelphia: Wolters Kluwer/Lippincott Williams & Wilkins. Chapter 35. ISBN 978-0-7817-6546-6. Archived from the original on 6 February 2015. Получено 3 ноября 2014.CS1 maint: BOT: статус исходного URL-адреса неизвестен (связь)
- ^ а б c d "Neuroendocrine tumors, NCCN Guidelines Version 1.2015" (PDF). National Comprehensive Cancer Network, Inc. NCCN). 11 ноября 2014 г.. Получено 25 декабря 2014.
- ^ Национальный институт рака. Pancreatic Neuroendocrine Tumors (Islet Cell Tumors) Treatment (PDQ®) Incidence and Mortality «Архивная копия». В архиве из оригинала 4 января 2015 г.. Получено 29 декабря 2014.CS1 maint: заархивированная копия как заголовок (связь)
- ^ "Diet and activity factors that affect risks for certain cancers: Pancreatic cancer section". Американское онкологическое общество. 20 августа 2012 г. В архиве из оригинала 4 ноября 2014 г.. Получено 4 ноября 2014.
- ^ Owens DK, Davidson KW, Krist AH, Barry MJ, Cabana M, Caughey AB, et al. (August 2019). "Screening for Pancreatic Cancer: US Preventive Services Task Force Reaffirmation Recommendation Statement". JAMA. 322 (5): 438–444. Дои:10.1001/jama.2019.10232. PMID 31386141.
- ^ He XY, Yuan YZ (August 2014). "Advances in pancreatic cancer research: moving towards early detection". Всемирный журнал гастроэнтерологии. 20 (32): 11241–8. Дои:10.3748/wjg.v20.i32.11241. ЧВК 4145762. PMID 25170208.
- ^ а б Okano K, Suzuki Y (August 2014). "Strategies for early detection of resectable pancreatic cancer". Всемирный журнал гастроэнтерологии. 20 (32): 11230–40. Дои:10.3748/wjg.v20.i32.11230. ЧВК 4145761. PMID 25170207.
- ^ Goggins M, Overbeek KA, Brand R, Syngal S, Del Chiaro M, Bartsch DK, et al. (Январь 2020 г.). "Management of patients with increased risk for familial pancreatic cancer: updated recommendations from the International Cancer of the Pancreas Screening (CAPS) Consortium". Кишечник. 69 (1): 7–17. Дои:10.1136/gutjnl-2019-319352. ЧВК 7295005. PMID 31672839.
- ^ Gurusamy KS, Kumar S, Davidson BR, Fusai G (February 2014). "Resection versus other treatments for locally advanced pancreatic cancer". Кокрановская база данных систематических обзоров. 2 (2): CD010244. Дои:10.1002/14651858.CD010244.pub2. PMID 24578248.
- ^ а б Mollberg N, Rahbari NN, Koch M, Hartwig W, Hoeger Y, Büchler MW, Weitz J (December 2011). "Arterial resection during pancreatectomy for pancreatic cancer: a systematic review and meta-analysis". Анналы хирургии. 254 (6): 882–93. Дои:10.1097/SLA.0b013e31823ac299. PMID 22064622. S2CID 42685174.
- ^ а б c "Pancreatic adenocarcinoma. NCCN Guidelines Version 1.2015" (PDF). NCCN Guidelines. National Comprehensive Cancer Network, Inc. 4 December 2014. Получено 26 декабря 2014.
- ^ Alamo JM, Marín LM, Suarez G, Bernal C, Serrano J, Barrera L, et al. (Октябрь 2014 г.). "Improving outcomes in pancreatic cancer: key points in perioperative management". Всемирный журнал гастроэнтерологии. 20 (39): 14237–45. Дои:10.3748/wjg.v20.i39.14237. ЧВК 4202352. PMID 25339810.
- ^ Lopez NE, Prendergast C, Lowy AM (August 2014). "Borderline resectable pancreatic cancer: definitions and management". Всемирный журнал гастроэнтерологии. 20 (31): 10740–51. Дои:10.3748/wjg.v20.i31.10740. ЧВК 4138454. PMID 25152577.
- ^ Polistina F, Di Natale G, Bonciarelli G, Ambrosino G, Frego M (July 2014). "Neoadjuvant strategies for pancreatic cancer". Всемирный журнал гастроэнтерологии. 20 (28): 9374–83. Дои:10.3748/wjg.v20.i28.9374 (неактивно 10 ноября 2020 г.). ЧВК 4110569. PMID 25071332.CS1 maint: DOI неактивен по состоянию на ноябрь 2020 г. (связь)
- ^ Gillen S, Schuster T, Meyer Zum Büschenfelde C, Friess H, Kleeff J (April 2010). "Preoperative/neoadjuvant therapy in pancreatic cancer: a systematic review and meta-analysis of response and resection percentages". PLOS Медицина. 7 (4): e1000267. Дои:10.1371/journal.pmed.1000267. ЧВК 2857873. PMID 20422030.
- ^ Christians KK, Evans DB (June 2015). "Additional support for neoadjuvant therapy in the management of pancreatic cancer". Анналы хирургической онкологии. 22 (6): 1755–8. Дои:10.1245/s10434-014-4307-0. PMID 25519932.
- ^ Tsvetkova EV, Asmis TR (August 2014). "Role of neoadjuvant therapy in the management of pancreatic cancer: is the era of biomarker-directed therapy here?". Current Oncology. 21 (4): e650-7. Дои:10.3747/co.21.2006. ЧВК 4117630. PMID 25089113.
- ^ Zhan HX, Xu JW, Wu D, Zhang TP, Hu SY (February 2015). "Pancreatic cancer stem cells: new insight into a stubborn disease". Письма о раке. 357 (2): 429–37. Дои:10.1016/j.canlet.2014.12.004. PMID 25499079.
- ^ а б Tanase CP, Neagu AI, Necula LG, Mambet C, Enciu AM, Calenic B, et al. (Август 2014 г.). "Cancer stem cells: involvement in pancreatic cancer pathogenesis and perspectives on cancer therapeutics". Всемирный журнал гастроэнтерологии. 20 (31): 10790–801. Дои:10.3748/wjg.v20.i31.10790. ЧВК 4138459. PMID 25152582.
- ^ Allen VB, Gurusamy KS, Takwoingi Y, Kalia A, Davidson BR (July 2016). "Diagnostic accuracy of laparoscopy following computed tomography (CT) scanning for assessing the resectability with curative intent in pancreatic and periampullary cancer". Кокрановская база данных систематических обзоров. 7: CD009323. Дои:10.1002/14651858.CD009323.pub3. ЧВК 6458011. PMID 27383694.
- ^ Heinemann V, Haas M, Boeck S (October 2013). "Neoadjuvant treatment of borderline resectable and non-resectable pancreatic cancer". Анналы онкологии. 24 (10): 2484–92. Дои:10.1093/annonc/mdt239. PMID 23852311.
- ^ а б c Thota R, Pauff JM, Berlin JD (January 2014). "Treatment of metastatic pancreatic adenocarcinoma: a review". Онкология. 28 (1): 70–4. PMID 24683721.
- ^ Ryan DP (8 July 2014). "Chemotherapy for advanced exocrine pancreatic cancer: Topic 2475, Version 46.0" (требуется подписка). Своевременно. Wolters Kluwer Health. В архиве из оригинала 8 декабря 2014 г.. Получено 18 ноября 2014.
- ^ "Cancer Drug Information: FDA Approval for Erlotinib Hydrochloride". Национальный институт рака. Национальные институты здоровья. 3 июля 2013 г. В архиве из оригинала 29 ноября 2014 г.. Получено 5 декабря 2014.
- ^ Borazanci E, Von Hoff DD (September 2014). "Nab-paclitaxel and gemcitabine for the treatment of patients with metastatic pancreatic cancer". Экспертный обзор гастроэнтерологии и гепатологии. 8 (7): 739–47. Дои:10.1586/17474124.2014.925799. PMID 24882381. S2CID 31633898.
- ^ Falconi M, Bartsch DK, Eriksson B, Klöppel G, Lopes JM, O'Connor JM, et al. (2012). "ENETS Consensus Guidelines for the management of patients with digestive neuroendocrine neoplasms of the digestive system: well-differentiated pancreatic non-functioning tumors". Нейроэндокринология. 95 (2): 120–34. Дои:10.1159/000335587. PMID 22261872. S2CID 6985904.
- ^ Jensen RT, Cadiot G, Brandi ML, de Herder WW, Kaltsas G, Komminoth P, et al. (2012). "ENETS Consensus Guidelines for the management of patients with digestive neuroendocrine neoplasms: functional pancreatic endocrine tumor syndromes". Нейроэндокринология. 95 (2): 98–119. Дои:10.1159/000335591. ЧВК 3701449. PMID 22261919.
- ^ Pavel M, Baudin E, Couvelard A, Krenning E, Öberg K, Steinmüller T, et al. (2012). «Консенсусное руководство ENETS по ведению пациентов с печенью и другими отдаленными метастазами от нейроэндокринных новообразований передней, средней и задней кишок, а также неизвестных первичных». Нейроэндокринология. 95 (2): 157–76. Дои:10.1159/000335597. PMID 22262022. S2CID 2097604.
- ^ Росси Р. Э., Массирони С., Конте Д., Пераки М. (январь 2014 г.). «Терапия метастатических нейроэндокринных опухолей поджелудочной железы». Анналы трансляционной медицины. 2 (1): 8. Дои:10.3978 / j.issn.2305-5839.2013.03.01. ЧВК 4200651. PMID 25332984.
- ^ Ник Малкахи (17 декабря 2014 г.). «FDA одобряет ланреотид для лечения нейроэндокринных опухолей». Медицинские новости Medscape. WebMD LLC. В архиве из оригинала 18 января 2015 г.. Получено 25 декабря 2014.
- ^ Эверолимус одобрен для лечения нейроэндокринных опухолей поджелудочной железы В архиве 16 июля 2016 г. Wayback Machine Почта ASCO. 15 мая 2011 г., Том 2, Выпуск 8
- ^ Национальный институт рака. Информация о лекарствах от рака. Одобрение FDA для сунитиниба малата В архиве 5 января 2015 г. Wayback Machine. Нейроэндокринные опухоли поджелудочной железы
- ^ Текст доступен в электронном виде (но может потребоваться бесплатная регистрация) См.: Бенсон А.Б., Майерсон Р.Дж., Сассон А.Р. (2010). Рак поджелудочной железы, нейроэндокринного желудочно-кишечного тракта и надпочечников. Лечение рака: мультидисциплинарный подход (13-е изд.). ISBN 978-0-615-41824-7. В архиве из оригинала 15 мая 2011 г.
- ^ Гуленчин К.Ю., Яо X, Аса С.Л., Сингх С., Закон C (май 2012 г.). «Радионуклидная терапия нейроэндокринных опухолей: систематический обзор». Клиническая онкология. 24 (4): 294–308. Дои:10.1016 / j.clon.2011.12.003. PMID 22221516.
- ^ Виник А.И. (ноябрь 2014 г.). «Достижения в диагностике и лечении нейроэндокринных опухолей поджелудочной железы». Эндокринная практика. 20 (11): 1222–30. Дои:10.4158 / EP14373.RA. PMID 25297671.
- ^ Kwekkeboom DJ, de Herder WW, van Eijck CH, Kam BL, van Essen M, Teunissen JJ, Krenning EP (март 2010 г.). «Радионуклидная терапия пептидных рецепторов у больных с гастроэнтеропанкреатическими нейроэндокринными опухолями». Семинары по ядерной медицине. 40 (2): 78–88. Дои:10.1053 / j.semnuclmed.2009.10.004. PMID 20113677.
- ^ Бодей Л., Кремонези М., Кидд М., Грана С.М., Севери С., Модлин И.М., Паганелли Г. (август 2014 г.). «Радионуклидная терапия пептидных рецепторов для запущенных нейроэндокринных опухолей». Клиники торакальной хирургии. 24 (3): 333–49. Дои:10.1016 / j.thorsurg.2014.04.005. HDL:11392/2378236. PMID 25065935.
- ^ Кастеллано Д., Гранде Е., Валле Дж., Капдевила Дж., Рейди-Лагунес Д., О'Коннор Дж. М., Раймонд Е. (июнь 2015 г.). «Экспертный консенсус в отношении лечения запущенных или метастатических нейроэндокринных и карциноидных опухолей поджелудочной железы». Химиотерапия и фармакология рака. 75 (6): 1099–114. Дои:10.1007 / s00280-014-2642-2. PMID 25480314. S2CID 39434924.
- ^ Сингх С., Дей С., Кеннеке Х., Коча В., Марун Дж., Метракос П. и др. (Август 2015 г.). «Консенсусные рекомендации по диагностике и лечению нейроэндокринных опухолей поджелудочной железы: рекомендации канадской национальной экспертной группы». Анналы хирургической онкологии. 22 (8): 2685–99. Дои:10.1245 / с10434-014-4145-0. PMID 25366583. S2CID 8129133.
- ^ «Паллиативная или поддерживающая терапия». Американское онкологическое общество. 2014 г. В архиве из оригинала 21 августа 2014 г.. Получено 20 августа 2014.
- ^ Буанес Т.А. (август 2014 г.). «Возможно улучшение лечения рака поджелудочной железы». Всемирный журнал гастроэнтерологии. 20 (30): 10405–18. Дои:10.3748 / wjg.v20.i30.10405. ЧВК 4130847. PMID 25132756.
- ^ «Если перестанет работать лечение рака поджелудочной железы». Американское онкологическое общество. 11 июня 2014 г. Архивировано с оригинал 22 октября 2014 г.. Получено 20 августа 2014.
- ^ Arcidiacono PG, Calori G, Carrara S, McNicol ED, Testoni PA (март 2011 г.). Arcidiacono PG (ред.). «Блокада чревного сплетения при боли при раке поджелудочной железы у взрослых». Кокрановская база данных систематических обзоров (3): CD007519. Дои:10.1002 / 14651858.CD007519.pub2. ЧВК 6464722. PMID 21412903.
- ^ «Рак в цифрах и фактах, 2014 г.» (PDF). Американское онкологическое общество. В архиве (PDF) из оригинала 18 декабря 2014 г.. Получено 5 января 2015., Таблица, стр. 18, ставки скорректированы с учетом нормальной продолжительности жизни
- ^ Джемал А., Сигель Р., Уорд Е., Мюррей Т., Сюй Дж., Тун М.Дж. (2007). «Статистика рака, 2007». Ca. 57 (1): 43–66. Дои:10.3322 / canjclin.57.1.43. PMID 17237035. S2CID 22305510.
- ^ «Каковы основные статистические данные о раке поджелудочной железы?». Американское онкологическое общество. 11 июня 2014 г. В архиве из оригинала 11 ноября 2014 г.. Получено 11 ноября 2014.
- ^ «Статистика рака поджелудочной железы». Cancer Research UK. В архиве из оригинала 18 декабря 2014 г.. Получено 18 декабря 2014.; «В 2010 году в Великобритании пожизненный риск развития рака поджелудочной железы составлял 1 из 73 для мужчин и 1 из 74 для женщин», отмечая: «Пожизненный риск ... был рассчитан ... с использованием метода« Текущая вероятность ». ; этот метод отличается от метода, используемого в большинстве других очагов рака, поскольку вероятность иметь более одного диагноза рака поджелудочной железы в течение их жизни очень мала ».
- ^ а б Busnardo AC, DiDio LJ, Tidrick RT, Thomford NR (ноябрь 1983 г.). «История поджелудочной железы». Американский журнал хирургии. 146 (5): 539–50. Дои:10.1016/0002-9610(83)90286-6. PMID 6356946.
- ^ а б c d Аре С., Дхир М., Равипати Л. (июнь 2011 г.). «История панкреатодуоденэктомии: ранние заблуждения, начальные вехи и пионеры». Е.П.Б.. 13 (6): 377–84. Дои:10.1111 / j.1477-2574.2011.00305.x. ЧВК 3103093. PMID 21609369.
- ^ а б Кэмерон Дж. Л., Риал Т. С., Коулман Дж., Белчер К. А. (июль 2006 г.). «Тысяча последовательных панкреатодуоденэктомий». Анналы хирургии. 244 (1): 10–5. Дои:10.1097 / 01.sla.0000217673.04165.ea. ЧВК 1570590. PMID 16794383.
- ^ Фернандес-дель Кастильо С., Моралес-Оярвиде В., МакГрат Д., Варго Дж. А., Ферроне С. Р., Тайер С. П. и др. (Сентябрь 2012 г.). «Эволюция процедуры Уиппла в Массачусетской больнице общего профиля». Хирургия. 152 (3 Дополнение 1): S56-63. Дои:10.1016 / j.surg.2012.05.022. ЧВК 3806095. PMID 22770961.
- ^ а б c "Что нового в исследованиях и лечении рака поджелудочной железы?". Американское онкологическое общество. 2019. Получено 2 мая 2019.
- ^ «Исследование рака поджелудочной железы». Cancer Research UK. В архиве из оригинала 18 февраля 2014 г.. Получено 17 июля 2014.
- ^ "Австралийская инициатива по геному поджелудочной железы". Институт Гарвана. В архиве из оригинала 26 июля 2014 г.. Получено 17 июля 2014.
- ^ Бианкин А.В., Уодделл Н., Кассан К.С., Гинграс М.С., Мутусвами Л.Б., Джонс А.Л. и др. (Ноябрь 2012 г.). «Геномы рака поджелудочной железы выявляют аберрации в генах путей наведения аксонов». Природа. 491 (7424): 399–405. Bibcode:2012Натура.491..399.. Дои:10.1038 / природа11547. ЧВК 3530898. PMID 23103869.
- ^ Грэм Дж. С., Джеймисон Н. Б., Рулах Р., Гриммонд С. М., Чанг Д. К., Бьянкин А. В. (сентябрь 2015 г.). «Геномика рака поджелудочной железы: куда нас может привести наука?». Клиническая генетика. 88 (3): 213–9. Дои:10.1111 / cge.12536. PMID 25388820. S2CID 26414866.
- ^ Чжан Ц., Ян Г, Лин И, Чен Г, Чжоу Т. (декабрь 2014 г.). «Ранняя диагностика рака поджелудочной железы и диабета: какова связь?». Журнал онкологии желудочно-кишечного тракта. 5 (6): 481–8. Дои:10.3978 / j.issn.2078-6891.2014.055. ЧВК 4226830. PMID 25436129.
- ^ Бруендерман Э.Х., Мартин Р.К. (март 2015 г.). «Население высокого риска при спорадической аденокарциноме поджелудочной железы: рекомендации по скринингу». Журнал хирургических исследований. 194 (1): 212–9. Дои:10.1016 / j.jss.2014.06.046. ЧВК 4559279. PMID 25479908.
- ^ «О ЕВРОПАК». Европейский регистр наследственного панкреатита и семейного рака поджелудочной железы (EUROPAC). Ливерпульский университет. Архивировано из оригинал 26 июля 2014 г.. Получено 17 июля 2014.
- ^ Субар Д., Гобардхан П.Д., Гайет Б. (февраль 2014 г.). «Лапароскопическая хирургия поджелудочной железы: обзор литературы и опыта одного центра». Лучшие практики и исследования. Клиническая гастроэнтерология. 28 (1): 123–32. Дои:10.1016 / j.bpg.2013.11.011. PMID 24485260.
- ^ Вайс MJ, Вольфганг CL (2013). «Необратимая электропорация: новая терапия рака поджелудочной железы». Текущие проблемы при раке. 37 (5): 262–5. Дои:10.1016 / j.currproblcancer.2013.10.002. PMID 24331180.
- ^ Moir J, White SA, French JJ, Littler P, Manas DM (декабрь 2014 г.). «Систематический обзор необратимой электропорации в лечении запущенного рака поджелудочной железы». Европейский журнал хирургической онкологии. 40 (12): 1598–604. Дои:10.1016 / j.ejso.2014.08.480. PMID 25307210.
- ^ Клегер А., Перхофер Л., Зеуфферляйн Т. (июль 2014 г.). «Новые лекарства для лечения рака поджелудочной железы». Анналы онкологии. 25 (7): 1260–1270. Дои:10.1093 / annonc / mdu013. PMID 24631947.
- ^ а б Тан С.К., Чен Ю.К. (август 2014 г.). «Новые терапевтические мишени при раке поджелудочной железы». Всемирный журнал гастроэнтерологии. 20 (31): 10825–44. Дои:10.3748 / wjg.v20.i31.10825. ЧВК 4138462. PMID 25152585.
- ^ Росси М.Л., Рехман А.А., Гонди С.С. (август 2014 г.). «Варианты лечения рака поджелудочной железы». Всемирный журнал гастроэнтерологии. 20 (32): 11142–59. Дои:10.3748 / wjg.v20.i32.11142. ЧВК 4145755. PMID 25170201.
- ^ Ади Дж. У., Хеффнер Дж, Кляйн Э, Фонг Й (2014). «Онколитическая вирусная терапия рака поджелудочной железы: текущие исследования и будущие направления». Онколитическая виротерапия. 3: 35–46. Дои:10.2147 / OV.S53858. ЧВК 4918362. PMID 27512661.
- ^ Рен Б., Цуй М., Ян Г, Ван Х, Фэн М., Ю Л., Чжао Ю. (июль 2018 г.). «Микроокружение опухоли участвует в метастазировании рака поджелудочной железы». Молекулярный рак. 17 (1): 108. Дои:10.1186 / s12943-018-0858-1. ЧВК 6065152. PMID 30060755.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |
| Викискладе есть медиафайлы по теме Панкреатический рак. |