WikiDer > Циклическая нейтропения
| Циклическая нейтропения | |
|---|---|
| Другие имена | Периодическая нейтропения, циклическая лейкопения, циклическое кроветворение |
| Специальность | Гематология |
| Симптомы | Лихорадка, недомогание, воспаление и инфекция слизистой оболочки полости рта, дыхательных путей, пищеварительного тракта, кожи и боли в животе[1] |
| Обычное начало | Младенчество[1] |
| Причины | Мутация в ELANE ген[1] |
| Диагностический метод | Анализ крови, генетическое тестирование[1] |
| лечение | G-CSF[1] |
| Медикамент | Филграстим[1] |
| Частота | 1 в млн (2018)[1] |
Циклическая нейтропения (CyN) - редкое гематологическое заболевание и форма врожденный нейтропения это, как правило, происходит примерно каждые три недели и продолжается в течение нескольких дней из-за изменения скорости нейтрофил производство Костный мозг. Это вызывает временное состояние с низким абсолютное количество нейтрофилов и поскольку нейтрофилы составляют большую часть циркулирующих белые кровяные клетки это подвергает организм серьезному риску воспаление и инфекция. По сравнению с тяжелая врожденная нейтропения, хорошо поддается лечению колониестимулирующий фактор гранулоцитов (филграстим), который увеличивает количество нейтрофилов, сокращает продолжительность цикла, а также снижает тяжесть и частоту инфекций.
Признаки и симптомы
Общие симптомы нейтропении повторяются. высокая температура, недомогание, воспаление тканей, окружающих зубы, язвы во рту, воспаление и бактериальная инфекция дыхательных путей, пищеварительного тракта, кожи и боли в животе.[1][2] Считается, что наибольший риск смерти связан с развитием некротический энтероколит (NEC), перитонит, бактериемия или Clostridium и кишечная палочка сепсис и септический шок, и пневмония.[1][3][4]
Причины
Циклическая нейтропения (CyN), как тяжелая врожденная нейтропения (SCN) - редкое заболевание. Считается, что в общей популяции CyN имеет частоту один на миллион.[1] Это результат аутосомно-доминантной мутации в ELANE ген, расположенный на коротком плече (р) хромосома 19 (19p13.3), ген, кодирующий нейтрофильная эластаза, что также является наиболее частой причиной SCN.[1][5][6][7] Спорадически возникает как de novo вариант мутации или может присутствовать среди членов одной семьи.[1] В случае CyN было обнаружено, что варианты мутации в основном группируются в интрон 4 и экзон 4 и 5,[6][3] но также были расположены в интроне 3, экзоне 2 и 3.[8][9][10][11][12] Некоторые варианты мутаций были обнаружены как в Cyn, так и в SCN, что указывает на то, что они фенотипы одного и того же заболевания разной степени тяжести.[9]
Считается, что мутация вызывает снижение «продукции нейтрофилов» или апоптоз (более короткий период полураспада) », что приводит к дефициту зрелых нейтрофилов в крови.[13] Точный патологический механизм все еще исследуется, при этом основными гипотезами являются неправильная локализация ELANE или развернутый белковый ответ (UPR), индуцированный мутантом ELANE,[14] однако согласно Mehta et al. (2016), "индукция UPR мутантным ELANE недостаточно силен, чтобы способствовать гибели клеток, и этот мутант ELANE вызывает SCN через альтернативный механизм ".[15] Согласно Garg et al. (2020), новые «результаты» ставят под сомнение преобладающую в настоящее время модель, согласно которой SCN является результатом мутантного ELANE, который вызывает стресс эндоплазматического ретикулума, UPR и апоптоз ".[16] Выражение ELANE ген был связан с GFI1 ген,[8][17] а некоторые считали, что взаимодействие с другими генами вызывает возникновение и тяжесть того или иного фенотипического расстройства.[9] Неясно, что вызывает циклический аспект в CyN.[17] По данным Donadieu et al. (2011), «циклический аспект ... предполагает существование загадочных биологических часов, которые регулируют гранулопоэз. Эти предполагаемые часы могут быть обнаружены определенными мутациями ".[13] Майкл Макки "постулирует, что выработка нейтрофилов регулируется стимулирующими факторами дальнего действия в длинной петле обратной связи, которая имеет встроенную временную задержку созревания промиелоциты к полностью дифференцированным нейтрофилам ».[18] Также неясно, что является причиной того, что уровни ингибитора секреторной лейкоцитарной протеазы (SLPI), которые влияют на индукцию развернутого белкового ответа (UPR), не уменьшаются, и, следовательно, активация UPR отсутствует в CyN по сравнению с SCN, другими словами, разные ELANE мутации «по-разному влияют на активацию UPR, а SLPI регулирует степень UPR, запускаемого ELANE».[19]
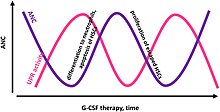
Согласно исследованию 2020 года, опубликованному в Летопись Нью-Йоркской академии наук о патомеханизме CyN, было обнаружено, что "некоторые HSPCs избежать вызванного UPR эндоплазматический ретикулум (ER) стресс и пролиферируют в ответ на гранулоцитарный колониестимулирующий фактор (G-CSF) до определенного порога, при котором UPR снова влияет на большинство HSPC. Существует циклический баланс между индуцированным ER-стрессом апоптозом HSPC и компенсаторной G-CSF-стимулированной пролиферацией HSPC с последующей гранулоцитарной дифференцировкой », другими словами, CyN« характеризуется циклической сменой активности UPR и циклической сменой UPR-ускользающих клеток ». Наиболее вероятная причина того, что из одного и того же варианта мутации развивается SCN, а не CyN, связана с более серьезным повреждением, вызванным UPR-стрессом в SCN.[18]
Диагностика
Диагноз обычно подтверждается мониторингом абсолютного количества нейтрофилов (АНК) три раза в неделю в течение как минимум шести недель.[1][3] Подтверждение может сопровождаться Периодограмма Ломба.[20] Во время состояния, которое длится от трех до шести дней и, как правило, возникает примерно каждые три недели (но может колебаться от 14 до 36 дней),[2][3] то абсолютное количество нейтрофилов (ANC) составляет менее 200-500 клеток / мкл (<0,2-0,5х109/ Л), с увеличением моноцит подсчетов, а также легкие колебания других клеток, в том числе легкие анемия.[1][21] Между циклами количество нейтрофилов в большинстве случаев достигает субнормальных или нормальных значений.[17]
Рекомендуется генетическое тестирование на мутации в ELANE и другие гены, связанные с нейтропенией (например, HAX1, G6PC3, GFI1 и др.), чтобы дифференцировать его от других вторичных причин и форм нейтропении.[1][22] В некоторых случаях интервалы и колебания могут быть меньше, что делает анализ ANC недостаточным,[1] и поскольку оба заболевания могут иметь одинаковые варианты мутации в ELANE Желательно иметь как ДРП, так и генетический анализ, чтобы подтвердить диагноз, тяжелая ли это врожденная или циклическая нейтропения.[21][20]
лечение

Хотя люди между циклами, как правило, здоровы, а симптомы имеют тенденцию улучшаться в зрелом возрасте, рекомендуется избегать деятельности, которая может привести к травмам, регулярно получать уход за полостью рта и зубов[2] и Вакцина БЦЖ следует избегать.[1][13] Рекомендуется контролировать количество лейкоцитов несколько раз в год. Лечение после появления симптомов должно быть немедленным, чтобы предотвратить инфекции, особенно во время лихорадки, когда требуется терапия антибиотиками широкого спектра действия (см. фебрильная нейтропения). Самым важным и часто спасающим жизнь лечением является профилактическая терапия колониестимулирующий фактор гранулоцитов (G-CSF), в виде филграстим, который регулирует выработку нейтрофилов в костном мозге, но сокращает нейтропенический цикл примерно до 7-14 дней и продолжительность тяжелого состояния.[1][17] Подкожные инъекции со средней дозировкой 1,5 мкг / кг / день,[18] можно назначать ежедневно, периодически один раз в три дня или приурочивать только к лечению нейтропенического периода.[13][23] Терапия считается «безопасной и эффективной», без значительных побочных эффектов.[24] помимо возможности развития остеопения.[21]
В колониестимулирующий фактор гранулоцитов-макрофагов (GM-CSF) менее эффективен с большим количеством побочных эффектов. Другая альтернатива - трансплантация гемопоэтических стволовых клеток (HSCT), но обычно практикуется в SCN,[1] и в одном случае между двумя братьями-донорами, один из которых проходил лечение ТГСК от острый миелоидный лейкоз (AML), в то время как второй имел CyN и чей костный мозг был перенесен, CyN также был передан посредством аллогенной трансплантации костного мозга. Это показывает, что CyN является стволовая клетка беспорядок.[25] Ежегодные исследования костного мозга не рекомендуются.[23]
Прогноз
Существует очень высокий риск опасных для жизни инфекций и смерти в раннем возрасте.[13] Качество жизни и выживаемость значительно улучшаются при лечении G-CSF, которое практикуется с конца 1980-х годов.[21] В отличие от тяжелой врожденной нейтропении, люди с циклической нейтропенией лучше реагируют на Г-КСФ и не имеют риска развития миелодиспластический синдром (МДС) и острый миелоидный лейкоз (ОМЛ).[1][3] Однако при длительном наблюдении за более чем 300 пациентов с CyN был зарегистрирован один случай развития хронический миелолейкоз (CML) и один из AML,[21][24] указывает на то, что это также предлейкозное состояние, но риск «очень низкий» (1%[18]),[26] и риск «коррелирует с серьезностью заболевания, а не с возникновением мутации ELANE».[10] По данным Donadieu et al. (2011), «совокупный риск возникновения хотя бы одной серьезной (потенциально опасной для жизни) инфекции к возрасту 20 лет аналогичен у пациентов с постоянной и циклической нейтропенией, хотя у бывших пациентов, как правило, проявляются более ранние проявления».[13]
История
Впервые описано в 1910 г.,[21][2] было предложено и подтверждено наличие аутосомного доминирующий (AD) наследование в 1940-х и 1960-х годах,[27] но дифференцировались от врожденных нейтропений до 1990-х годов, когда были проанализированы родословные и выявлены генетические мутации, общие у пациентов с тяжелая врожденная нейтропения.[13]
Смотрите также
использованная литература
- ^ а б c d е ж г час я j k л м п о п q р s т Дейл Д.К., Макарян В (2018) [2002]. Адам М. П., Ардингер Х. Х., Пагон Р. А., Уоллес С. Е., Бин Л. Дж. (Ред.). «Нейтропения, связанная с ELANE». GeneReviews. PMID 20301705.
- ^ а б c d Ольвера К.И., Барриос В.М., Риос РФ, Руидиас В.К. (2015). «Циклическая нейтропения. Отчет о клиническом случае». Revista Odontológica Mexicana. 19 (4): 246–252. Дои:10.1016 / j.rodmex.2015.10.015. Получено 2019-08-12.
- ^ а б c d е Боксер Л.А. (2012). «Как подойти к нейтропении». Гематология. Американское общество гематологии. Образовательная программа. 2012 (1): 174–82. Дои:10.1182 / asheducation.v2012.1.174.3798251. PMID 23233578.
- ^ Джеймс В.Д., Элстон Д.М., Бергер Т.Г., Эндрюс Г.К. (2006). Болезни кожи Эндрюса: клиническая дерматология. Saunders Elsevier. п.808–811. ISBN 978-0-7216-2921-6.
- ^ Сера Y, Кавагути Х., Накамура К., Сато Т., Хабара М., Окада С. и др. (Август 2005 г.). «Сравнение дефектного гранулопоэза при детской циклической нейтропении и тяжелой врожденной нейтропении». Haematologica. 90 (8): 1032–41. PMID 16079102.
- ^ а б Макарян В., Зейдлер С., Болярд А.А., Скокова Дж., Роджер Э., Келли М.Л. и др. (Январь 2015 г.). «Разнообразие мутаций и клинических исходов нейтропении, связанной с ELANE». Текущее мнение в гематологии. 22 (1): 3–11. Дои:10.1182 / blood.V118.21.3398.3398. ЧВК 4380169. PMID 25427142.
- ^ Хорвиц М.С., Кори С.Дж., Граймс Х.Л., Тидвелл Т. (февраль 2013 г.). «Мутации ELANE при циклической и тяжелой врожденной нейтропении: генетика и патофизиология». Гематологические / онкологические клиники Северной Америки. 27 (1): 19–41, vii. Дои:10.1016 / j.hoc.2012.10.004. ЧВК 3559001. PMID 23351986.
- ^ а б Bellanné-Chantelot C, Clauin S, Leblanc T, Cassinat B, Rodrigues-Lima F, Beaufils S, et al. (Июнь 2004 г.). «Мутации в гене ELA2 коррелируют с более тяжелым проявлением нейтропении: исследование 81 пациента из Французского регистра нейтропении». Кровь. 103 (11): 4119–25. Дои:10.1182 / кровь-2003-10-3518. PMID 14962902.
- ^ а б c Newburger PE, Pindyck TN, Zhu Z, Bolyard AA, Aprikyan AA, Dale DC, et al. (Август 2010 г.). «Циклическая нейтропения и тяжелая врожденная нейтропения у пациентов с общей мутацией ELANE и отцовским гаплотипом: доказательства определения фенотипа путем модификации генов». Детская кровь и рак. 55 (2): 314–7. Дои:10.1002 / pbc.22537. ЧВК 2913300. PMID 20582973.
- ^ а б Гермесхаузен М., Дирберг С., Питер Й, Реймер К., Кратц С. П., Баллмайер М. (июнь 2013 г.). «Спектр мутаций ELANE и их значение при тяжелой врожденной и циклической нейтропении». Человеческая мутация. 34 (6): 905–14. Дои:10.1002 / humu.22308. PMID 23463630.
- ^ Макарян В., Цейдлер С., Болярд А.А., Скокова Дж., Роджер Э., Келли М.Л. и др. (Январь 2015 г.). «Разнообразие мутаций и клинических исходов нейтропении, связанной с ELANE». Текущее мнение в гематологии. 22 (1): 3–11. Дои:10.1097 / MOH.0000000000000105. ЧВК 4380169. PMID 25427142.
- ^ Лю И, Фу Дж, Чжан Дж, Ван Ю, Гуань Х (2017). «Отчет о рецидивах язв в полости рта, связанных с циклической нейтропенией». Анналы отчетов о клинических случаях. 2: 905–914. ISSN 2474-1655. S2CID 21701463.
- ^ а б c d е ж г Donadieu J, Fenneteau O, Beaupain B, Mahlaoui N, Chantelot CB (май 2011 г.). «Врожденная нейтропения: диагностика, молекулярные основы и ведение пациентов». Журнал редких заболеваний Orphanet. 6: 26. Дои:10.1186/1750-1172-6-26. ЧВК 3127744. PMID 21595885.
- ^ Хорвиц М.С., Лаурино М.Ю., Кил С.Б. (август 2019 г.). "Мутация делеции целого гена ELANE". Кровавые достижения. 3 (16): 2470–2473. Дои:10.1182 / bloodadvances.2019000498. ЧВК 6712528. PMID 31427279.
- ^ Мехта Х.М., Дас А., Камель Р., Хорвиц М., Кори С. (декабрь 2016 г.). «Условная экспрессия мутанта ELANE вызывает развернутый белковый ответ, но не способствует гибели клеток или блокировке дифференцировки: каков механизм тяжелой врожденной нейтропении?». Кровь. 128 (22): 3899. Дои:10.1182 / blood.V128.22.3899.3899.
- ^ Гарг Б., Мехта Х.М., Ван Б., Камель Р., Хорвиц М.С., Кори С.Дж. (май 2020 г.). «Мутация ELANE нарушает дифференцировку гранулоцитов, не вызывая развернутого белкового ответа». Журнал биологической химии. 295 (21): 7492–7500. Дои:10.1074 / jbc.RA120.012366. ЧВК 7247317. PMID 32299910.
- ^ а б c d Horwitz MS, Duan Z, Korkmaz B, Lee HH, Mealiffe ME, Salipante SJ (март 2007 г.). «Нейтрофильная эластаза при циклической и тяжелой врожденной нейтропении». Кровь. 109 (5): 1817–24. Дои:10.1182 / кровь-2006-08-019166. ЧВК 1801070. PMID 17053055.
- ^ а б c d е ж Mir P, Klimiankou M, Findik B, Hähnel K, Mellor-Heineke S, Zeidler C и др. (Апрель 2020 г.). «Новое понимание патомеханизма циклической нейтропении». Летопись Нью-Йоркской академии наук. 1466 (1): 83–92. Bibcode:2020НЯСА1466 ... 83М. Дои:10.1111 / няс.14309. PMID 32083314.
- ^ Нустеде Р., Климянкоу М., Клименкова О., Кузнецова И., Цейдлер С., Велте К., Скокова Дж. (Январь 2016 г.). «Специфическая мутантная активация ELANE различных путей UPR при врожденной нейтропении». Британский журнал гематологии. 172 (2): 219–27. Дои:10.1111 / bjh.13823. PMID 26567890.
- ^ а б Дейл, округ Колумбия, Болярд А.А., Люнг Дж., Тран Э, Марреро TM, Newburger PE (2017). «Циклическая нейтропения, врожденная и идиопатическая нейтропения». Кровь. 130: 2275. Получено 2019-08-12.
- ^ а б c d е ж Дейл, округ Колумбия, Болярд А.А., Марреро TM, Бонилья М.А., Линк Д.С., Ньюбургер П.Е., Шимамура А., Боксер Л.А. (2012). «Естественная история циклической нейтропении: долгосрочные перспективные наблюдения и современные перспективы». Кровь. 120 (21): 2141. Дои:10.1182 / blood.V120.21.2141.2141. Получено 2019-08-12.
- ^ Арун А.К., Сентамижселви А., Хемамалини С., Эдисон Е.С., Корула А., Фузия Н.А. и др. (Декабрь 2018 г.). «Мутации ELANE при врожденной нейтропении: одноцентровое исследование у пациентов индийского происхождения». Журнал клинической патологии. 71 (12): 1046–1050. Дои:10.1136 / jclinpath-2018-205235. PMID 30171085. S2CID 52141047.
- ^ а б Дейл, округ Колумбия (август 2017 г.). «Как я веду детей с нейтропенией». Британский журнал гематологии. 178 (3): 351–363. Дои:10.1111 / bjh.14677. PMID 28419427.
- ^ а б Dale DC, Bolyard A, Marrero T., Makaryan V, Bonilla M, Link DC и др. (Декабрь 2017 г.). «Долгосрочные эффекты терапии G-CSF при циклической нейтропении». Медицинский журнал Новой Англии. 377 (23): 2290–2292. Дои:10.1056 / NEJMc1709258. ЧВК 5777346. PMID 29211670.
- ^ Krance RA, Spruce WE, Forman SJ, Rosen RB, Hecht T, Hammond WP, Blume KG (декабрь 1982 г.). «Циклическая нейтропения человека, перенесенная аллогенной трансплантацией костного мозга». Кровь. 60 (6): 1263–6. Дои:10.1182 / blood.V60.6.1263.1263. PMID 6753968.
- ^ Zeidler C, Mellor-Heineke S, Klimiankou M, Skokowa J, Welte K (2015). «Первый случай лейкемии у ребенка, страдающего циклической нейтропенией с мутацией ELANE». Кровь. 126 (23): 997. Дои:10.1182 / кровь.V126.23.997.997.
- ^ Патил В.Х., Хугар С.М., Баликай Г., Патил С. (2016). «Тяжелая врожденная циклическая нейтропения: история болезни». Международный журнал прикладных и фундаментальных медицинских исследований. 6 (4): 293–296. Дои:10.4103 / 2229-516X.192598. ЧВК 5108111. PMID 27857902.
внешние ссылки
- Международный регистр тяжелой хронической нейтропении
- "Понимание нейтропении: 20-летний опыт Международного регистра тяжелой хронической нейтропении (SCNIR)" (2014)
| Классификация | |
|---|---|
| Внешние ресурсы |