WikiDer > Нейрофиброматоз II типа
| Нейрофиброматоз II типа | |
|---|---|
| Другие имена | множественные наследственные шванномы, менингиомы и эпендимомы (синдром MISME) |
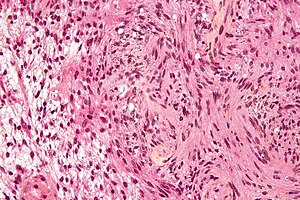 | |
| Микрофотография из шваннома, опухоль, наблюдаемая при нейрофиброматозе II типа. Пятно HPS. | |
| Специальность | Медицинская генетика, неврология |
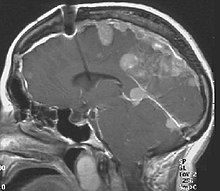
Нейрофиброматоз II типа (также известный как синдром MISME - множественные унаследованные шванномы, менингиомы и эпендимомы) - это генетическое заболевание, которое может передаваться по наследству или возникать спонтанно. Основное проявление состояния - развитие двустороннего доброкачественный опухоли головного мозга в нервной оболочке черепной нерв VIII, который представляет собой «слухово-вестибулярный нерв», передающий сенсорную информацию от внутреннее ухо к мозг. Кроме того, возникают другие доброкачественные опухоли головного и спинного мозга. Симптомы зависят от наличия, локализации и роста опухоли (опухолей). Многие люди с этим заболеванием также испытывают проблемы со зрением. Нейрофиброматоз II типа (NF2 или NF II) вызвано мутации из "Мерлин" ген,[1] что, кажется, влияет на форму и движение клетки. Основные методы лечения состоят из нейрохирургический удаление новообразований и хирургическое лечение поражений глаз. Исторически основное заболевание не лечилось из-за функции клеток, вызванной генетической мутацией.
Классификация
NF2 - это наследственное заболевание с аутосомно-доминантный режим передачи.[требуется медицинская цитата]
Есть две формы NF2:[2]
- В Wishart-Фенотип характеризуется множественными поражениями головного мозга и спинного мозга у людей моложе 20 лет и быстрым прогрессированием опухолей.
- Считается, что люди с NF2, у которых развиваются единичные центральные опухоли с медленным прогрессированием после 20 лет, имеют Фенотип Фейлинга-Гарднера.
Причина
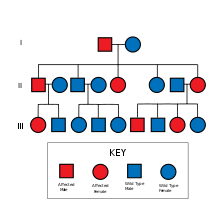
NF2 вызывается инактивирующими мутациями в гене NF2, расположенном в 22q12.2 хромосома 22Типы мутаций различаются и включают усекающие белок изменения (делеции / вставки со сдвигом рамки считывания и бессмысленные мутации), мутации сайтов сплайсинга, миссенс-мутации и другие. Исключения тоже есть в NH2-концевой домен белков мерлина были связаны с ранним началом опухоли и плохим прогнозом у людей с NF2.[3] Мутации, усекающие белок, коррелируют с более тяжелым фенотипом.[4] Известен широкий клинический спектр, но у всех людей с этим заболеванием, которые были проверены, была обнаружена некоторая мутация одного и того же гена. хромосома 22. Согласно статистическим данным, половина случаев передается по наследству, а половина является результатом новых, de novo мутации.
Патогенез
NF2 вызывается дефектом гена, который обычно приводит к образованию продукта, называемого Мерлин или Шванномин, расположенный на полосе 22 хромосомы q11-13.1. Мерлин был впервые открыт как структурный белок, функционирующий как регулятор актинового цитоскелета. Позже была описана роль Мерлина в подавлении опухолей. Мерлин регулирует несколько пролиферативных сигнальных каскадов, таких как рецепторная тирозинкиназа сигнализация, р21-активированная киназа сигнализация, Рас сигнализация, МЕК-ERK каскад Каскад MST-YAP.[5] В нормальной клетке концентрация активного (дефосфорилированного) мерлина контролируется такими процессами, как клеточная адгезия (что указывало бы на необходимость сдерживать деление клеток). Было показано, что Мерлин подавляет Rac1 что имеет решающее значение для подвижности клеток и инвазии опухоли.[6] Кроме того, взаимодействие Мерлина с циклин D был описан.[7] Известно, что дефицит Мерлина может привести к немедленному прогрессированию через клеточный цикл из-за отсутствия контактно-опосредованного подавления опухоли, главным образом из-за разрушения межклеточного соединения, достаточного для образования опухолей, характерных для нейрофиброматоза II типа. Недавние исследования показали, что помимо своих цитоскелетных и цитоплазматических функций Мерлин также перемещается в ядро и подавляет пролиферацию, ингибируя E3 убиквитинлигаза CRL4 (DCAF1).[8] Наконец, самые последние исследования показали, что Мерлин также играет важную роль в регуляции энергетического обмена.[9][10] Предполагается, что мутации NF2 приводят либо к неспособности синтезировать Мерлин, либо к выработке дефектного пептида, у которого отсутствует нормальный эффект подавления опухоли. Шванномин-пептид состоит из 595 аминокислоты. Сравнение Шванномина с другими белки показывает сходство с белками, которые соединяют цитоскелет к клеточная мембрана. Считается, что мутации в гене шванномина изменяют движение и форму пораженных клеток с потерей контактного торможения. Эпендимомы - это опухоли, возникающие из эпендима, эпителиоподобная ткань Центральная нервная система. У людей с NF2 и эпендимомами функция подавления опухоли Мерлин могут быть скомпрометированы. Мутации потери функции, происходящие в хромосома 22q, где кодируются белки Мерлина, могут способствовать туморогенез, или создание новых опухолевых клеток.[3] Исключения тоже есть в NH2-концевой домен белков мерлина были связаны с ранним началом опухоли и плохим прогнозом у пораженных людей.[3]
Патология
Так называемое акустическая неврома NF2 на самом деле шваннома вестибулярного нерва или вестибулярной шванномы. Неправильное название акустической невриномы до сих пор используется. Вестибулярные шванномы медленно растут у внутреннего входа в внутренний слуховой проход (Meatusousticus internus). Они происходят из нервных оболочек верхней части вестибулярного нерва в области между центральным и периферическим миелином (зона Оберштейнера-Редлиха) в области акустической полости на расстоянии 1 см от ствола мозга.
Генотип-фенотип-корреляция
Многие люди с NF2 были включены в исследования, которые были разработаны для сравнения типа заболевания и его прогрессирования с точным определением связанной мутации. Цель таких сравнений генотипа и фенотипа - определить, вызывают ли определенные мутации соответствующие комбинации симптомов. Это было бы чрезвычайно полезно для прогнозирования прогрессирования заболевания и планирования терапии, начиная с раннего возраста. Результаты таких исследований следующие:
- В большинстве случаев мутация в гене NF2 вызывает укороченные пептиды.
- Нет мутационных горячих точек.
- Люди с мутации сдвига рамки считывания или бессмысленные мутации имеют плохой прогноз.
- Люди с миссенс-мутации иметь лучший прогноз.
- В случаях с мутациями в сплайс-акцепторная область, хорошей корреляции для определения нет.
- Точечные мутации может иметь лишь незначительные эффекты.
- Кейсы опубликованы[нужна цитата] в котором одна и та же мутация связана с явно разным исходом.
Эти результаты предполагают, что другие факторы (окружающая среда, другие мутации), вероятно, будут определять клинический результат.
Диагностика
Дородовой
Двусторонние вестибулярные шванномы являются диагностическим признаком NF2.[11]
Послеродовой
Ferner et al.[12] дадим три набора диагностических критериев NF2:
- Двусторонний вестибулярный шваннома (VS) или семейный анамнез NF2 плюс односторонний VS или любые два из: менингиома, глиома, нейрофиброма, шваннома, задние субкапсулярные линзовидные помутнения
- Односторонний ВС плюс любые два из менингиомы, глиомы, нейрофибромы, шванномы, задних субкапсулярных линзовидных помутнений
- Две или более менингиомы плюс односторонний VS или любые две из глиомы, шванномы и катаракты.
Другой набор диагностических критериев следующий:
- Обнаружение двусторонней акустической невриномы с помощью процедур визуализации
- Родственник первой степени родства с NF2 и наличием нейрофибромы, менингиомы, глиомы или шванномы
- Родственник первой степени с NF2 и возникновением ювенильной задней субкапсулярной катаракты.
Критерии менялись со временем.[13]Последний пересмотр критериев NF2 был проведен M.J. Smith в 2017 году. Это включало рассмотрение мутации LZTR1 (шванноматоз) вместо NF2 и исключало двусторонние вестибулярные шванномы, возникающие после 70 лет.[14]
лечение
Хирургия
Существует несколько различных хирургических методов удаления невриномы слухового нерва.[15] Выбор подхода определяется размером опухоли, слуховой способностью и общим клиническим состоянием человека.
- Ретросигмоидный подход предлагает некоторую возможность для сохранения слуха.
- Транслабиринтный подход принесет в жертву слух на этой стороне, но, как правило, щадит лицевой нерв. Послеоперационные утечки спинномозговой жидкости встречаются чаще.
- Доступ к средней ямке предпочтителен для небольших опухолей и предлагает самую высокую вероятность сохранения слуха и вестибулярной функции.
- В течение некоторого времени за пределами США применялись менее инвазивные эндоскопические методы. Сообщается, что время восстановления быстрее. Однако этот метод еще не получил широкого распространения среди хирургов в США.
Более крупные опухоли можно лечить с помощью трансбиринтинного или ретросигмоидного подхода, в зависимости от опыта хирургической бригады. При больших опухолях шанс сохранения слуха при любом подходе невелик. Когда слух уже плохой, транслабиринтный подход можно использовать даже для небольших опухолей. Маленькие латерализованные опухоли у людей с NF2 с хорошим слухом должны иметь доступ к средней ямке. Когда опухоль расположена более медиально, может быть лучше ретросигмоидный доступ.
Декомпрессия слухового канала - еще один хирургический метод, который может продлить полезный слух, когда вестибулярная шваннома стала слишком большой, чтобы удалить ее без повреждения улиткового нерва. При декомпрессии IAC (внутреннего слухового прохода) используется доступ к средней ямке, чтобы обнажить костную крышу IAC без каких-либо попыток удаления опухоли. Кость, лежащая над слуховым нервом, удаляется, позволяя опухоли расширяться вверх в среднюю черепную ямку. Таким образом уменьшается давление на кохлеарный нерв, что снижает риск дальнейшей потери слуха из-за прямого сдавливания или нарушения кровоснабжения нерва.
Радиохирургия является консервативной альтернативой основанию черепа или другой внутричерепной хирургии. При использовании конформных радиохирургических методов терапевтическое излучение фокусировалось на опухоли, избегая воздействия на окружающие нормальные ткани. Хотя радиохирургия редко может полностью уничтожить опухоль, она часто может остановить ее рост или уменьшить ее размер. Хотя облучение оказывает меньшее непосредственное повреждение, чем обычное хирургическое вмешательство, оно сопряжено с более высоким риском последующих злокачественных изменений в облученных тканях, и этот риск выше при NF2, чем при спорадических (не NF2) поражениях.
Лекарства
В настоящее время нет рецептурных лекарств, показанных для снижения опухолевой нагрузки у пациентов с NF2, хотя в исследованиях пациентов Бевацизумаб привело к снижению темпов роста опухоли и улучшению слуха у немного пациенты.[16][17]
Потеря слуха
Поскольку потеря слуха у людей с NF2 почти всегда возникает после приобретения навыков вербального языка, люди с NF2 не всегда хорошо интегрируются в Культура глухих и чаще прибегают к слуховым вспомогательные технологии.[нужна цитата]Одно из таких устройств - кохлеарный имплант, который иногда может восстановить высокий уровень слуховой функции даже при полной потере естественного слуха. Однако степень разрушения кохлеарного нерва, вызванная типичной шванномой NF2, часто исключает использование такого имплантата. В этих случаях слуховой имплант ствола мозга (ABI) может восстановить некоторый уровень слуха, дополненный чтение по губам.
Распространенность
Заболеваемость этим заболеванием составляет около 1 на 60 000.[18]
использованная литература
- ^ Стридингер К., Ванденберг С.Р., Байя Г.С., Макдермотт М.В., Гутманн Д.Х., Лал А. (ноябрь 2008 г.). «Продукт гена супрессора опухолей нейрофиброматоза 2, мерлин, регулирует рост клеток менингиомы человека посредством передачи сигналов через YAP». Неоплазия. 10 (11): 1204–12. Дои:10.1593 / neo.08642. ЧВК 2570596. PMID 18953429.
- ^ Вальтер Дж., Кун С.А., Бродхун М., Райхарт Р., Калфф Р. (июнь 2009 г.). «Легочная менингиома и невринома, связанные с множественными опухолями ЦНС у пациента с нейрофиброматозом 2 типа». Clin Neurol Neurosurg. 111 (5): 454–9. Дои:10.1016 / j.clineuro.2008.11.018. PMID 19249154. S2CID 22696343.
- ^ а б c Стаменкович, I; Ю, Q (2010). «Мерлин,« волшебный »линкер между внеклеточными сигналами и внутриклеточными сигнальными путями, которые регулируют подвижность, пролиферацию и выживание клеток». Современная наука о белках и пептидах. 11 (6): 471–84. Дои:10.2174/138920310791824011. ЧВК 2946555. PMID 20491622.
- ^ Купер, Джонатан; Джанкотти, Филиппо Г. (2014-04-12). «Молекулярное понимание функции супрессора опухолей NF2 / Merlin». Письма FEBS. 588 (16): 2743–2752. Дои:10.1016 / j.febslet.2014.04.001. ЧВК 4111995. PMID 24726726.
- ^ Окада, Томойо; Ты, Лиру; Джанкотти, Филиппо Г. (май 2007 г.). «Проливая свет на волшебство Мерлина». Тенденции в клеточной биологии. 17 (5): 222–229. Дои:10.1016 / j.tcb.2007.03.006. ISSN 1879-3088. PMID 17442573.
- ^ Шерман, Ларри; Гутманн, Дэвид (1 ноября 2001 г.). «Мерлин: вешает подавление опухолей на Rac» (PDF). Тенденции в клеточной биологии. 11 (11): 442–444. Дои:10.1016 / S0962-8924 (01) 02128-6. ISSN 0962-8924. PMID 11684412.
- ^ Сяо, Гуан-Хуэй; Галлахер, Райан; Шетлер, Джастин; Скеле, Кристина; Альтомаре, Дебора; Пестелл, Ричард; Джанвар, Суреш; Теста, Джозеф (март 2005 г.). «Продукт гена-супрессора опухоли NF2, мерлин, ингибирует пролиферацию клеток и развитие клеточного цикла, подавляя экспрессию циклина D1». Молекулярная и клеточная биология. 25 (6): 2384–2394. Дои:10.1128 / MCB.25.6.2384-2394.2005. ISSN 0270-7306. ЧВК 1061616. PMID 15743831.
- ^ Купер, Джонатан; Ли, Вэй; Ты, Лиру; Скьявон, Гайя; Пепе-Каприо, Анджела; Чжоу, Лу; Исии, Рёхей; Джованнини, Марко; Ханеманн, К. Оливер (23 августа 2011 г.). «Мерлин / NF2 функционирует выше ядерной убиквитинлигазы E3 CRL4DCAF1, подавляя экспрессию онкогенных генов». Научная сигнализация. 4 (188): pt6. Дои:10.1126 / scisignal.2002314. ISSN 1937-9145. PMID 21878678. S2CID 9582719.
- ^ Степанова, Дина; Браун, Ланита; Чернофф, Джонатан (май 2018 г.). «Новая концепция фармакотерапии NF2: нацеливание на синтез жирных кислот». Онкология. 5 (5–6): 126–127. Дои:10.18632 / oncoscience.417. ISSN 2331-4737. ЧВК 6049319. PMID 30035161.
- ^ Степанова, Дина; Семенова, Галина; Го, Инь-Мин; Эндрюс, Эндрю Дж .; Аммун, Сильвия; Ханеманн, К. Оливер; Чернофф, Джонатан (15 сентября 2017 г.). «Важная роль супрессора опухолей Мерлина в регулировании синтеза жирных кислот». Исследования рака. 77 (18): 5026–5038. Дои:10.1158 / 0008-5472.CAN-16-2834. ISSN 1538-7445. ЧВК 5600854. PMID 28729415.
- ^ Кристофер Гиллберг (16 октября 2003 г.). Клиническая детская нейропсихиатрия. Издательство Кембриджского университета. стр. 231–. ISBN 978-0-521-54335-4. Получено 20 декабря 2010.
- ^ Фернер, Розали Э., Сьюзан М. Хьюсон и Д. Гарет Р. Эванс. Нейрофиброматозы в клинической практике. Спрингер, 2011.
- ^ «Нейрофиброматоз 2 типа: радиология eMedicine». 2016-09-26. Получено 2010-12-20. Цитировать журнал требует
| журнал =(Помогите) - ^ Жан Режис; Пьер-Юго Рош (2008). Современное лечение акустической невромы. Karger Publishers. С. 191–. ISBN 978-3-8055-8370-1. Получено 20 декабря 2010.
- ^ "Информационная страница о нейрофиброматозе". Национальный институт неврологических заболеваний и инсульта. Получено 16 июня, 2019.
- ^ Катрина А. Моррис; Джон Ф. Голдинг; Патрик Р. Аксон; и другие. (2016). «Бевацизумаб при вестибулярных шванномах, связанных с нейрофиброматозом 2 типа (NF2): скоординированный на национальном уровне подход к доставке и проспективной оценке». Нейроонкол Прак. 3 (4): 281–289. Дои:10.1093 / nop / npv065. ЧВК 5909937. PMID 29692918.
- ^ Эванс Д.Г. (2009). «Нейрофиброматоз 2 типа (NF2): клинический и молекулярный обзор». Орфанет Дж. Редкие Диск.. 4: 16. Дои:10.1186/1750-1172-4-16. ЧВК 2708144. PMID 19545378.
дальнейшее чтение
- Эванс, Д. Гарет (1993). «Нейрофиброматоз 2». GeneReviews. Вашингтонский университет, Сиэтл. Получено 30 мая 2017.
внешние ссылки
| Классификация | |
|---|---|
| Внешние ресурсы |