WikiDer > Эстрадиол
 | |
 | |
| Имена | |
|---|---|
| Произношение | /ˌɛsтрəˈdаɪoʊл/ ES-trə-DY-охл[1][2] |
| Название ИЮПАК (8р,9S,13S,14S,17S) -13-Метил-6,7,8,9,11,12,14,15,16,17-декагидроциклопента [а] фенантрен-3,17-диол | |
| Другие имена Эстрадиол; E2; 17β-эстрадиол; Эстра-1,3,5 (10) -триен-3,17β-диол; 17β-эстрадиол | |
| Идентификаторы | |
3D модель (JSmol) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.000.022 |
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C18ЧАС24О2 | |
| Молярная масса | 272,38 г / моль |
| -186.6·10−6 см3/ моль | |
| Фармакология | |
| G03CA03 (ВОЗ) | |
| Данные лицензии | |
| Устный, сублингвальный, интраназальный, актуальный/трансдермальный, вагинальный, внутримышечный или же подкожный (как сложный эфир), подкожный имплант | |
| Фармакокинетика: | |
| Устно: <5%[3] | |
| ~98%:[3][4] • Альбумин: 60% • SHBG: 38% • Бесплатно: 2% | |
| Печень (через гидроксилирование, сульфатирование, глюкуронизация) | |
| Устно: 13–20 часов.[3] Сублингвально: 8–18 часов[5] Местно (гель): 36,5 часов[6] | |
| Моча: 54%[3] Кал: 6%[3] | |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Эстрадиол (E2), также пишется эстрадиол, является эстроген стероидный гормон и главный женский половой гормон. Он участвует в регулировании эстральный и менструальный женский репродуктивные циклы. Эстрадиол отвечает за развитие женского вторичные половые признаки такой как грудь, расширение бедер, а женский характер распределения жира и важен в развитии и поддержании женского репродуктивные ткани такой как молочные железы, матка, и влагалище в течение половое созревание, совершеннолетие, и беременность.[7] Он также имеет важные эффекты во многих других ткани в том числе кость, толстый, кожа, печень, а мозг. Хотя уровень эстрадиола у мужчин намного ниже, чем у женщин, эстрадиол играет важную роль и у мужчин. Помимо людей и других млекопитающие, эстрадиол также содержится в большинстве позвоночные и ракообразные, насекомые, рыбы, и другие животное разновидность.[8][9]
Эстрадиол производится особенно в фолликулы из яичники, но также и в других тканях, включая яички, то надпочечники, толстый, печень, грудь и мозг. Эстрадиол произведен в теле из холестерин через серию реакции и промежуточные звенья.[10] Главная путь предполагает формирование андростендион, который затем преобразуется ароматаза в эстрон и впоследствии превращается в эстрадиол. Альтернативно, андростендион можно превратить в тестостерон, который затем может быть преобразован в эстрадиол. На менопауза у женщин производство эстрогенов яичниками прекращается, а уровень эстрадиола снижается до очень низкого уровня.
Помимо своей роли естественного гормона, эстрадиол используется как медикамент, например в менопаузальная гормональная терапия и трансгендерная гормональная терапия за трансгендерные женщины; для получения информации об эстрадиоле как лекарстве см. эстрадиол (лекарство) статья.
Биологическая функция
Половое развитие
Развитие вторичные половые признаки у женщин движет эстроген, а точнее эстрадиол.[11][12] Эти изменения инициируются во время половое созревание, большинство из них усиливаются в репродуктивном возрасте и становятся менее выраженными при снижении поддержки эстрадиолом после менопауза. Таким образом, эстрадиол производит развитие груди, и несет ответственность за изменения в форма кузова, поражая кости, суставы и отложение жира.[11][12] У женщин эстрадиол способствует развитию груди, расширение бедер, а женское распределение жира (с отложением жира, в частности, в груди, бедрах, бедрах и ягодицах) и созревание влагалище и вульва, в то время как он является посредником пубертатный скачок роста (косвенно через увеличение гормон роста секреция)[13] и закрытие эпифиза (тем самым ограничивая конечная высота) у обоих полов.[11][12]
Размножение
Женская репродуктивная система
У женщин эстрадиол действует как гормон роста тканей репродуктивных органов, поддерживая слизистую оболочку влагалище, шейные железы, эндометрий, и слизистой оболочки маточных труб. Увеличивает рост миометрий. Эстрадиол необходим для поддержания ооциты в яичник. Вовремя менструальный цикл, эстрадиол, продуцируемый растущими фолликулами, запускает через систему положительной обратной связи гипоталамо-гипофизарные события, которые приводят к лютеинизирующий гормон всплеск, вызывающий овуляцию. В лютеиновой фазе эстрадиол в сочетании с прогестерон, подготавливает эндометрий к имплантация. В течение беременность, эстрадиол увеличивается за счет плацентарный производство. Эффект эстрадиола вместе с эстрон и эстриол, в беременность менее ясно. Они могут способствовать кровотоку в матке, росту миометрия, стимулировать рост груди и в срок, способствовать размягчению шейки матки и экспрессии миометрия. окситоцин рецепторы.[нужна цитата] У бабуинов блокирование выработки эстрогена приводит к потере беременности, что позволяет предположить, что эстрадиол играет важную роль в поддержании беременности. Исследования изучают роль эстрогенов в процессе инициации труд. Действия эстрадиола необходимы до воздействия прогестерона в лютеиновой фазе.[нужна цитата]
Мужская репродуктивная система
Эффект эстрадиола (и эстрогенов в целом) на мужскую репродуктивную функцию сложен. Эстрадиол производится под действием ароматаза в основном в Клетки Лейдига из млекопитающее яички, но и некоторыми стволовые клетки и Клетки Сертоли незрелых млекопитающих.[14] Он функционирует (in vitro) предотвращать апоптоз мужчины сперма клетки.[15]Хотя некоторые исследования в начале 1990-х годов утверждали связь между глобальным снижением количество сперматозоидов и воздействие эстрогена в окружающей среде,[16] более поздние исследования не обнаружили ни такой связи, ни свидетельств общего снижения количества сперматозоидов.[17][18]Подавление выработки эстрадиола в субпопуляции мужчин с низкой фертильностью может улучшить сперма анализ.[19]
Самцы с определенными половая хромосома генетические условия, Такие как Синдром Клайнфельтера, будет иметь более высокий уровень эстрадиола.[20]
Система скелета
Эстрадиол оказывает сильное воздействие на кости. Люди без этого (или других эстрогенов) станут высокими и евнухоид, так как эпифизарный закрытие задерживается или может не состояться. Низкий уровень эстрадиола также может прогнозировать переломы, причем самый высокий риск возникает, особенно у мужчин с низким общим и высоким уровнем глобулин, связывающий половые гормоны белок.[21] Плотность костной ткани также влияет, что приводит к раннему остеопения и остеопороз.[22] У женщин в период менопаузы наблюдается ускоренная потеря костной массы из-за относительного дефицита эстрогена.[23]
Здоровье кожи
В рецептор эстрогена, так же хорошо как рецептор прогестерона, были обнаружены в кожа, в том числе в кератиноциты и фибробласты.[24][25] В менопауза и впоследствии снизился уровень женского половые гормоны результат в атрофия, прореживание и увеличенное морщинистый кожи и уменьшение кожи эластичность, твердость и сила.[24][25] Эти изменения кожи представляют собой ускорение старение кожи и являются результатом уменьшения коллаген содержание, нарушения в морфология из эпидермальный клетки кожи, уменьшилось основное вещество между волокна кожи, и уменьшил капилляры и кровоток.[24][25] Кожа тоже становится более сухой во время менопаузы, что связано с уменьшением кожных покровов гидратация и поверхностные липиды (производство кожного сала).[24] Наряду с хронологическим старением и фотостарением, дефицит эстрогена во время менопаузы является одним из трех основных факторов, которые преимущественно влияют на старение кожи.[24]
Заместительная гормональная терапия состоящий из системного лечения одним эстрогеном или в сочетании с прогестагеном, имеет хорошо документированные и значительные положительные эффекты на кожу женщин в постменопаузе.[24][25] Эти преимущества включают повышенное содержание коллагена в коже, толщину и эластичность кожи, а также увлажнение кожи и поверхностные липиды.[24][25] Было обнаружено, что местный эстроген оказывает аналогичное благотворное воздействие на кожу.[24] Кроме того, исследование показало, что местный 2% -ный крем с прогестероном значительно увеличивает эластичность и упругость кожи и заметно уменьшает морщины у женщин в пери- и постменопаузе.[25] С другой стороны, гидратация кожи и поверхностные липиды существенно не изменились при местном применении прогестерона.[25] Эти данные показывают, что прогестерон, как и эстроген, также оказывает благотворное влияние на кожу и может независимо защищать кожу от старения.[25]
Нервная система
Эстрогены могут производиться в мозг из предшественников стероидов. В качестве антиоксиданты, у них было обнаружено нейропротекторный функция.[26]
Положительное и отрицательное петли обратной связи из менструальный цикл вовлекают эстрадиол яичников в качестве связующего звена с гипоталамо-гипофизарной системой для регулирования гонадотропины.[27] (Видеть Гипоталамо-гипофизарно-гонадная ось.)
Считается, что эстроген играет важную роль в психическом здоровье женщин, предполагая связь между уровнем гормонов, настроением и самочувствием. Внезапные падения, колебания или длительные периоды устойчивого низкого уровня эстрогена могут быть связаны со значительным ухудшением настроения. Клиническое восстановление после послеродовой депрессии, перименопаузы и постменопаузы оказалось эффективным после стабилизации и / или восстановления уровней эстрогена.[28][29]
В последнее время объемы сексуально диморфный структуры мозга в трансгендерные женщины было обнаружено, что при воздействии эстрогена одновременно с андрогенной депривацией в течение нескольких месяцев изменяются и приближаются типичные структуры женского мозга,[30] предполагая, что эстроген и / или андрогены играют важную роль в половой дифференциации мозга, как внутриутробно и позже в жизни.
Есть также свидетельства того, что программирование сексуального поведения взрослых самцов у многих позвоночных в значительной степени зависит от эстрадиола, вырабатываемого во время пренатальной жизни и в раннем младенчестве.[31] Пока не известно, играет ли этот процесс значительную роль в сексуальном поведении человека, хотя данные, полученные от других млекопитающих, как правило, указывают на связь.[32]
Было обнаружено, что эстроген увеличивает секреция окситоцина и увеличить выражение своего рецептор, то рецептор окситоцина, в мозг.[33] Было обнаружено, что у женщин однократной дозы эстрадиола достаточно для повышения концентрации циркулирующего окситоцина.[34]
Гинекологический рак
Эстрадиол был связан с развитием и прогрессированием раковых заболеваний, таких как рак груди, рак яичников и рак эндометрия. Эстрадиол влияет на ткани-мишени в основном за счет взаимодействия с двумя ядерные рецепторы называется рецептор эстрогена α (ERα) и рецептор эстрогена β (ERβ).[35][36] Одна из функций этих рецепторов эстрогена - модуляция экспрессия гена. Как только эстрадиол связывается с ER, рецепторные комплексы связываются со специфическими Последовательности ДНК, что может вызвать повреждение ДНК и увеличение деления клеток и Репликация ДНК. Эукариотические клетки реагировать на поврежденную ДНК, стимулируя или нарушая фазы G1, S или G2 клеточного цикла, чтобы инициировать Ремонт ДНК. В результате происходит клеточная трансформация и пролиферация раковых клеток.[37]
Сердечно-сосудистая система
Эстроген влияет на определенные кровеносный сосуд. Улучшение артериального кровотока было продемонстрировано в коронарные артерии.[38]
В течение беременность, высокий уровень эстрогенов, а именно эстрадиола, увеличивает коагуляция и риск Венозная тромбоэмболия.
| Абсолютная частота первой ВТЭ на 10 000 человеко-лет во время беременности и в послеродовой период | ||||||||
|---|---|---|---|---|---|---|---|---|
| Шведские данные A | Шведские данные B | Английские данные | Датские данные | |||||
| Временной период | N | Частота (95% ДИ) | N | Частота (95% ДИ) | N | Частота (95% ДИ) | N | Частота (95% ДИ) |
| Вне беременности | 1105 | 4.2 (4.0–4.4) | 1015 | 3.8 (?) | 1480 | 3.2 (3.0–3.3) | 2895 | 3.6 (3.4–3.7) |
| Дородовой | 995 | 20.5 (19.2–21.8) | 690 | 14.2 (13.2–15.3) | 156 | 9.9 (8.5–11.6) | 491 | 10.7 (9.7–11.6) |
| 1 триместр | 207 | 13.6 (11.8–15.5) | 172 | 11.3 (9.7–13.1) | 23 | 4.6 (3.1–7.0) | 61 | 4.1 (3.2–5.2) |
| 2 триместр | 275 | 17.4 (15.4–19.6) | 178 | 11.2 (9.7–13.0) | 30 | 5.8 (4.1–8.3) | 75 | 5.7 (4.6–7.2) |
| Триместр 3 | 513 | 29.2 (26.8–31.9) | 340 | 19.4 (17.4–21.6) | 103 | 18.2 (15.0–22.1) | 355 | 19.7 (17.7–21.9) |
| Вокруг доставки | 115 | 154.6 (128.8–185.6) | 79 | 106.1 (85.1–132.3) | 34 | 142.8 (102.0–199.8) | – | |
| Послеродовой | 649 | 42.3 (39.2–45.7) | 509 | 33.1 (30.4–36.1) | 135 | 27.4 (23.1–32.4) | 218 | 17.5 (15.3–20.0) |
| Ранний послеродовой период | 584 | 75.4 (69.6–81.8) | 460 | 59.3 (54.1–65.0) | 177 | 46.8 (39.1–56.1) | 199 | 30.4 (26.4–35.0) |
| Поздний послеродовой период | 65 | 8.5 (7.0–10.9) | 49 | 6.4 (4.9–8.5) | 18 | 7.3 (4.6–11.6) | 319 | 3.2 (1.9–5.0) |
| Коэффициенты заболеваемости (IRR) первой ВТЭ во время беременности и в послеродовой период | ||||||||
| Шведские данные A | Шведские данные B | Английские данные | Датские данные | |||||
| Временной период | IRR * (95% ДИ) | IRR * (95% ДИ) | IRR (95% ДИ) † | IRR (95% ДИ) † | ||||
| Вне беременности | Ссылка (например, 1,00) | |||||||
| Дородовой | 5.08 (4.66–5.54) | 3.80 (3.44–4.19) | 3.10 (2.63–3.66) | 2.95 (2.68–3.25) | ||||
| 1 триместр | 3.42 (2.95–3.98) | 3.04 (2.58–3.56) | 1.46 (0.96–2.20) | 1.12 (0.86–1.45) | ||||
| 2 триместр | 4.31 (3.78–4.93) | 3.01 (2.56–3.53) | 1.82 (1.27–2.62) | 1.58 (1.24–1.99) | ||||
| Триместр 3 | 7.14 (6.43–7.94) | 5.12 (4.53–5.80) | 5.69 (4.66–6.95) | 5.48 (4.89–6.12) | ||||
| Вокруг доставки | 37.5 (30.9–44.45) | 27.97 (22.24–35.17) | 44.5 (31.68–62.54) | – | ||||
| Послеродовой | 10.21 (9.27–11.25) | 8.72 (7.83–9.70) | 8.54 (7.16–10.19) | 4.85 (4.21–5.57) | ||||
| Ранний послеродовой период | 19.27 (16.53–20.21) | 15.62 (14.00–17.45) | 14.61 (12.10–17.67) | 8.44 (7.27–9.75) | ||||
| Поздний послеродовой период | 2.06 (1.60–2.64) | 1.69 (1.26–2.25) | 2.29 (1.44–3.65) | 0.89 (0.53–1.39) | ||||
| Примечания: Шведские данные A = Использование любого кода для VTE независимо от подтверждения. Шведские данные B = Использование только подтвержденных алгоритмом VTE. Ранний послеродовой период = первые 6 недель после родов. Поздний послеродовой период = более 6 недель после родов. * = С поправкой на возраст и календарный год. † = нескорректированный коэффициент, рассчитанный на основе предоставленных данных. Источник: [39] | ||||||||
Прочие функции
Эстрадиол оказывает комплексное воздействие на печень. Это влияет на производство нескольких белки, включая липопротеины, связывающие белки и белки, ответственные за свертывание крови.[нужна цитата] В больших количествах эстрадиол может привести к холестаз, например холестаз беременности.
Некоторые гинекологические состояния зависят от эстрогена, например: эндометриоз, лейомиомы матки и маточное кровотечение.[нужна цитата]
Биологическая активность
Эстрадиол действует прежде всего как агонист из рецептор эстрогена (ER), а ядерный рецептор стероидного гормона. Есть два подтипа ER, ERα и ERβ, а эстрадиол сильно связывается с обоими этими рецепторами и активирует их. Результатом активации ER является модуляция транскрипция гена и выражение в ER-экспрессии клетки, который является основным механизмом, с помощью которого эстрадиол опосредует свои биологические эффекты в организме. Эстрадиол также действует как агонист мембранные рецепторы эстрогена (mER), например GPER (GPR30), недавно обнаруженный неядерный рецептор эстрадиола, через который он может опосредовать различные быстрые, неядерныегеномный последствия.[40] В отличие от случая ER, GPER кажется селективный для эстрадиола и показывает очень низкий родство для других эндогенных эстрогенов, таких как эстрон и эстриол.[41] Дополнительные MER помимо GPER включают ER-X, ERx, и граммq-mER.[42][43]
ERα / ERβ находятся в неактивном состоянии, захваченные многомолекулярными шаперонными комплексами, организованными вокруг белка теплового шока 90 (HSP90), содержащего белок p23 и иммунофилин, и локализуются большей частью в цитоплазме и частично в ядре. В классическом пути E2 или классическом пути эстрогена эстрадиол входит в цитоплазма, где он взаимодействует с ER. После связывания E2 ER диссоциируют от молекулярных комплексов шаперонов и становятся компетентными для димеризации, миграции в ядро и связывания со специфическими последовательностями ДНК (элемент эстрогенового ответа, ERE), что позволяет транскрипцию генов, которая может происходить в течение нескольких часов и дней.
Дано подкожная инъекция у мышей эстрадиол примерно в 10 раз эффективнее эстрона и примерно в 100 раз сильнее эстриола.[44][45][46] Таким образом, эстрадиол является основным эстрогеном в организме, хотя считается, что роль эстрона и эстриола как эстрогенов не является незначительной.[46]
| Эстроген | ER РБА (%) | Масса матки (%) | Утеротрофия | LH уровни (%) | SHBG РБА (%) |
|---|---|---|---|---|---|
| Контроль | – | 100 | – | 100 | – |
| Эстрадиол | 100 | 506 ± 20 | +++ | 12–19 | 100 |
| Estrone | 11 ± 8 | 490 ± 22 | +++ | ? | 20 |
| Эстриол | 10 ± 4 | 468 ± 30 | +++ | 8–18 | 3 |
| Эстетрол | 0.5 ± 0.2 | ? | Неактивный | ? | 1 |
| 17α-эстрадиол | 4.2 ± 0.8 | ? | ? | ? | ? |
| 2-гидроксиэстрадиол | 24 ± 7 | 285 ± 8 | +б | 31–61 | 28 |
| 2-метоксиэстрадиол | 0.05 ± 0.04 | 101 | Неактивный | ? | 130 |
| 4-гидроксиэстрадиол | 45 ± 12 | ? | ? | ? | ? |
| 4-метоксиэстрадиол | 1.3 ± 0.2 | 260 | ++ | ? | 9 |
| 4-фторэстрадиола | 180 ± 43 | ? | +++ | ? | ? |
| 2-гидроксиэстрон | 1.9 ± 0.8 | 130 ± 9 | Неактивный | 110–142 | 8 |
| 2-метоксиэстрон | 0.01 ± 0.00 | 103 ± 7 | Неактивный | 95–100 | 120 |
| 4-гидроксиэстрон | 11 ± 4 | 351 | ++ | 21–50 | 35 |
| 4-метоксиэстрон | 0.13 ± 0.04 | 338 | ++ | 65–92 | 12 |
| 16α-гидроксиэстрон | 2.8 ± 1.0 | 552 ± 42 | +++ | 7–24 | <0.5 |
| 2-гидроксиэстриол | 0.9 ± 0.3 | 302 | +б | ? | ? |
| 2-метоксиэстриол | 0.01 ± 0.00 | ? | Неактивный | ? | 4 |
| Примечания: Значения представляют собой среднее ± стандартное отклонение или диапазон. ER РБА = Относительная аффинность связывания к рецепторы эстрогена крысы матка цитозоль. Масса матки = процентное изменение влажной массы матки овариэктомия крысам через 72 часа при непрерывном введении 1 мкг / час через подкожно имплантированный осмотические насосы. LH уровни = Лютеинизирующий гормон уровни относительно исходного уровня у овариэктомированных крыс после 24-72 часов непрерывного введения через подкожный имплант. Сноски: а = Синтетический (т.е. не эндогенный). б = Атипичный утеротрофический эффект, достигающий плато в течение 48 часов (утеротрофия эстрадиола линейно продолжается до 72 часов). Источники: См. Шаблон. | |||||
Биохимия
Биосинтез
Эстрадиол, как и другие стероидные гормоны, происходит от холестерин. После боковая цепь спайности и используя Δ5 или Δ4- дорожка, андростендион является ключевым посредником. Часть андростендиона превращается в тестостерон, который, в свою очередь, превращается в эстрадиол под действием ароматазы. Альтернативным путем андростендион является ароматизированный к эстрон, который впоследствии превращается в эстрадиол через 17β-гидроксистероид дегидрогеназа (17β-HSD).[48]
В репродуктивном возрасте большая часть эстрадиола у женщин продуцируется клетками гранулезы яичников путем ароматизации андростендиона (продуцируемого в клетках фолликулов) в эстрон с последующим превращением эстрона в эстрадиол с помощью 17β-HSD. Меньшие количества эстрадиола также производятся кора надпочечников, а у мужчин - яичками.[требуется медицинская цитата]
Эстрадиол не производится в гонады только, в частности, жировые клетки вырабатывают активные предшественники эстрадиола и будут продолжать это делать даже после менопаузы.[49] Эстрадиол также производится в мозг И в артериальные стенки.
У мужчин примерно от 15 до 25% циркулирующего эстрадиола вырабатывается в яички.[50][51] Остальное синтезируется посредством периферической ароматизации тестостерона в эстрадиол и андростендиона в эстрон (который затем превращается в эстрадиол через периферический 17β-HSD).[50][51] Эта периферическая ароматизация происходит преимущественно в жировая ткань, но встречается и в других ткани Такие как кость, печень, а мозг.[50] У мужчин в сутки вырабатывается примерно 40-50 мкг эстрадиола.[50]
Распределение
В плазме эстрадиол в значительной степени связывается с SHBG, а также с альбумин. Только 2,21% (± 0,04%) являются свободными и биологически активными, процентное содержание остается постоянным на протяжении всего периода времени. менструальный цикл.[52]
Метаболизм
Метаболические пути эстрадиола у людей |
Инактивация эстрадиола включает преобразование в менее активные эстрогены, такие как эстрон и эстриол. Эстриол является основным мочевым метаболит.[нужна цитата] Эстрадиол сопряженный в печень формировать конъюгаты эстрогенов подобно эстрадиол сульфат, эстрадиол глюкуронид и, как таковой, выводится через почки. Некоторые водорастворимые конъюгаты выводятся через желчный проток, и частично реабсорбируется после гидролиз от кишечного тракта. Этот энтерогепатическое кровообращение способствует поддержанию уровня эстрадиола.
Эстрадиол также метаболизируется через гидроксилирование в катехол эстрогены. В печени неспецифически метаболизируется CYP1A2, CYP3A4, и CYP2C9 через 2-гидроксилирование в 2-гидроксиэстрадиол, и по CYP2C9, CYP2C19, и CYP2C8 через 17β-гидроксидегидрирование в эстрон,[53] с различными другими цитохром P450 (CYP) ферменты и метаболические превращения также участвует.[54]
Эстрадиол дополнительно сопряженный с сложный эфир в липоидный эстрадиол формы как эстрадиол пальмитат и стеарат эстрадиола в некоторой степени; эти сложные эфиры хранятся в жировая ткань и может действовать как очень длительный резервуар эстрадиола.[55][56]
Экскреция
Эстрадиол выделенный в виде глюкуронид и сульфат конъюгаты эстрогенов в моча. После внутривенная инъекция из маркированный эстрадиол у женщин почти 90% выводится с мочой и кал в течение 4-5 дней.[57][58] Энтерогепатическая рециркуляция вызывает задержку выведения эстрадиола.[57]
Уровни

Уровни эстрадиола у женщин в пременопаузе сильно различаются на протяжении менструального цикла, а контрольные диапазоны широко варьируются от источника к источнику.[60] Уровни эстрадиола минимальны и, по данным большинства лабораторий, колеблются от 20 до 80 пг / мл в течение ранней и средней фолликулярной фазы (или первой недели менструального цикла, также известной как менструация).[61][62] Уровни эстрадиола постепенно повышаются в течение этого времени и в течение средней и поздней фолликулярной фазы (или второй недели менструального цикла) до преовуляторной фазы.[60][61] Во время предовуляции (период примерно от 24 до 48 часов) уровни эстрадиола на короткое время повышаются и достигают максимальной концентрации в любое другое время менструального цикла.[60] В настоящее время уровни циркуляции обычно составляют от 130 до 200 пг / мл, но у некоторых женщин могут достигать 300-400 пг / мл, а верхний предел референсного диапазона некоторых лабораторий даже больше (например, 750 пг / мл). пг / мл).[60][61][63][64][65] После овуляции (или середины цикла) и во время второй половины менструального цикла или лютеиновой фазы уровни эстрадиола плато и колеблются между 100 и 150 пг / мл во время ранней и средней лютеиновой фазы, а также во время поздней. лютеиновая фаза или за несколько дней до менструации достигает минимума около 40 пг / мл.[60][62] Средние интегрированные уровни эстрадиола во время полного менструального цикла, по разным данным из разных источников, составляют 80, 120 и 150 пг / мл.[62][66][67] Хотя существуют противоречивые сообщения, одно исследование показало, что средние интегрированные уровни эстрадиола составляют 150 пг / мл у молодых женщин, тогда как средние интегрированные уровни колеблются от 50 до 120 пг / мл у пожилых женщин.[67]
В репродуктивном возрасте у женщин уровень эстрадиола несколько выше, чем у эстрона, за исключением ранней фолликулярной фазы менструального цикла; таким образом, эстрадиол может считаться преобладающим эстрогеном в репродуктивном возрасте женщины у человека с точки зрения абсолютных уровней в сыворотке и эстрогенной активности.[нужна цитата] Во время беременности эстриол становится преобладающим циркулирующим эстрогеном, и это единственный момент, когда эстетрол появляется в организме, в то время как во время менопаузы эстрон преобладает (оба в зависимости от уровня в сыворотке).[нужна цитата] Эстрадиол, вырабатываемый мужчинами из тестостерона, присутствует в сыворотке крови примерно сравнимо с уровнем постменопаузальный женщины (14–55 против <35 пг / мл соответственно).[нужна цитата] Также сообщалось, что если концентрация эстрадиола у 70-летнего мужчины по сравнению с концентрацией эстрадиола у 70-летней женщины, уровни у мужчины примерно в 2–4 раза выше.[68]
Измерение
У женщин уровень эстрадиола в сыворотке крови измеряется в клиническая лаборатория и отражает, прежде всего, активность яичников. Анализ крови на эстрадиол измеряет количество эстрадиола в крови.[69] Его применяют для проверки функции яичников, плаценты, надпочечников.[69] Это может определить исходный уровень эстрогена у женщин с аменорея или менструальной дисфункции, а также для выявления состояния гипоэстрогенности и менопаузы. Кроме того, мониторинг эстрогенов во время терапии бесплодия позволяет оценить рост фолликулов и полезен для мониторинга лечения. Опухоли, продуцирующие эстроген, будут демонстрировать стойкий высокий уровень эстрадиола и других эстрогенов. В преждевременное половое созревание, уровни эстрадиола неуместно повышены.
Диапазоны
Отдельные лабораторные результаты всегда следует интерпретировать с использованием диапазонов, предоставленных лабораторией, проводившей тест.
| Тип пациента | Нижний предел | Верхний предел | Единица измерения |
|---|---|---|---|
| Взрослый самец | 50[70] | 200[70] | пмоль / л |
| 14 | 55 | пг / мл | |
| Взрослая самка (фолликулярный фаза, день 5) | 70[70] 95% ЧИСЛО ПИ (стандарт) | 500[70] 95% ИП | пмоль / л |
| 110[71] 90% ЧИСЛО ПИ (использовал в диаграмма) | 220[71] 90% ИП | ||
| 19 (95% ИП) | 140 (95% ИП) | пг / мл | |
| 30 (90% ИП) | 60 (90% ИП) | ||
| Взрослая самка (преовуляторный вершина горы) | 400[70] | 1500[70] | пмоль / л |
| 110 | 410 | пг / мл | |
| Взрослая самка (лютеиновой фазы) | 70[70] | 600[70] | пмоль / л |
| 19 | 160 | пг / мл | |
| Взрослая женщина - бесплатно (не связывается с белками) | 0.5[72][оригинальное исследование?] | 9[72][оригинальное исследование?] | пг / мл |
| 1.7[72][оригинальное исследование?] | 33[72][оригинальное исследование?] | пмоль / л | |
| Женщина в постменопаузе | Нет данных[70] | < 130[70] | пмоль / л |
| Нет данных | < 35 | пг / мл |
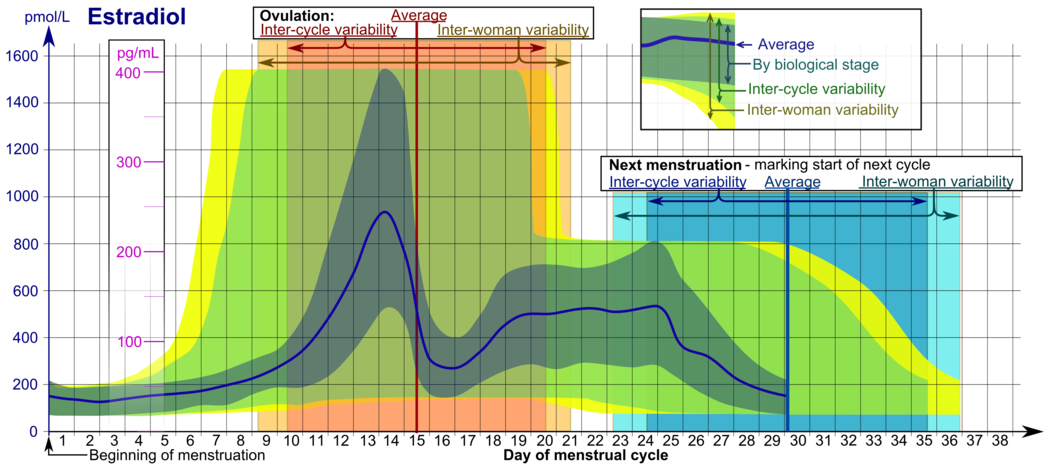
- Обозначенные диапазоны По биологической стадии может использоваться в тщательно контролируемых менструальных циклах в отношении других маркеров его биологической прогрессии, при этом временная шкала сжимается или растягивается до того, насколько быстрее или медленнее, соответственно, цикл прогрессирует по сравнению со средним циклом.
- Обозначенные диапазоны Межцикловая изменчивость являются более подходящими для использования в неконтролируемых циклах, когда известно только начало менструации, но когда женщина точно знает среднюю продолжительность своего цикла и время овуляции, и что они в некоторой степени средне регулярны, при этом шкала времени сжимается или растягивается до того, насколько сильно средняя продолжительность цикла женщины короче или длиннее, чем в среднем в популяции.
- Обозначенные диапазоны Межженщина изменчивость более подходят для использования, когда средняя продолжительность цикла и время овуляции неизвестны, но указано только начало менструации.[73]
В нормальном менструальном цикле уровни эстрадиола обычно составляют <50 пг / мл во время менструации, повышаются по мере развития фолликулов (пик: 200 пг / мл), кратковременно падают во время овуляции и снова повышаются во время лютеиновой фазы для второго пика. В конце лютеиновой фазы уровень эстрадиола падает до уровня менструального цикла, если не наступила беременность.
Во время беременности уровень эстрогенов, включая эстрадиол, неуклонно повышается к сроку беременности. Источником этих эстрогенов является плацента, который ароматизирует прогормоны вырабатывается в надпочечниках плода.
| Секс | Половой гормон | Репродуктивный фаза | Кровь дебит | Гонад скорость секреции | Метаболический скорость оформления | Референсный диапазон (уровни сыворотки) | |
|---|---|---|---|---|---|---|---|
| SI единицы | Не-SI единицы | ||||||
| Мужчины | Андростендион | – | 2,8 мг / день | 1,6 мг / день | 2200 л / сутки | 2,8-7,3 нмоль / л | 80–210 нг / дл |
| Тестостерон | – | 6,5 мг / день | 6,2 мг / день | 950 л / сутки | 6,9–34,7 нмоль / л | 200–1000 нг / дл | |
| Estrone | – | 150 мкг / день | 110 мкг / день | 2050 л / сутки | 37–250 пмоль / л | 10–70 пг / мл | |
| Эстрадиол | – | 60 мкг / день | 50 мкг / день | 1600 л / сутки | <37–210 пмоль / л | 10–57 пг / мл | |
| Эстрона сульфат | – | 80 мкг / день | Незначительный | 167 л / сутки | 600–2500 пмоль / л | 200–900 пг / мл | |
| Женщины | Андростендион | – | 3,2 мг / день | 2,8 мг / день | 2000 л / сутки | 3,1–12,2 нмоль / л | 89–350 нг / дл |
| Тестостерон | – | 190 мкг / день | 60 мкг / день | 500 л / сутки | 0,7–2,8 нмоль / л | 20–81 нг / дл | |
| Estrone | Фолликулярная фаза | 110 мкг / день | 80 мкг / день | 2200 л / сутки | 110–400 пмоль / л | 30–110 пг / мл | |
| Лютеиновой фазы | 260 мкг / день | 150 мкг / день | 2200 л / сутки | 310–660 пмоль / л | 80–180 пг / мл | ||
| Постменопауза | 40 мкг / день | Незначительный | 1610 л / сутки | 22–230 пмоль / л | 6–60 пг / мл | ||
| Эстрадиол | Фолликулярная фаза | 90 мкг / день | 80 мкг / день | 1200 л / сутки | <37–360 пмоль / л | 10–98 пг / мл | |
| Лютеиновой фазы | 250 мкг / день | 240 мкг / день | 1200 л / сутки | 699–1250 пмоль / л | 190–341 пг / мл | ||
| Постменопауза | 6 мкг / день | Незначительный | 910 л / сутки | <37–140 пмоль / л | 10–38 пг / мл | ||
| Эстрона сульфат | Фолликулярная фаза | 100 мкг / день | Незначительный | 146 л / сутки | 700–3600 пмоль / л | 250–1300 пг / мл | |
| Лютеиновой фазы | 180 мкг / день | Незначительный | 146 л / сутки | 1100–7300 пмоль / л | 400–2600 пг / мл | ||
| Прогестерон | Фолликулярная фаза | 2 мг / день | 1,7 мг / день | 2100 л / сутки | 0,3–3 нмоль / л | 0,1–0,9 нг / мл | |
| Лютеиновой фазы | 25 мг / день | 24 мг / день | 2100 л / сутки | 19–45 нмоль / л | 6–14 нг / мл | ||
Примечания и источники Примечания: "The концентрация Количество стероида в кровотоке определяется скоростью, с которой он секретируется железами, скоростью метаболизма предшественника или прегормонов в стероид и скоростью, с которой он извлекается тканями и метаболизируется. В скорость секреции стероида относится к общей секреции соединения железой за единицу времени. Скорость секреции оценивалась путем отбора проб венозного стока из железы с течением времени и вычитания концентрации артериальных и периферических венозных гормонов. В скорость метаболического клиренса стероида определяется как объем крови, который полностью очищен от гормона за единицу времени. В дебит стероидного гормона относится к поступлению в кровь соединения из всех возможных источников, включая секрецию желез и превращение прогормонов в интересующий стероид. В устойчивом состоянии количество гормона, поступающего в кровь из всех источников, будет равно скорости, с которой он очищается (скорость метаболического клиренса), умноженной на концентрацию в крови (скорость продукции = скорость метаболического клиренса × концентрация). Если метаболизм прогормона вносит небольшой вклад в циркулирующий пул стероидов, то скорость производства будет приблизительно соответствовать скорости секреции ». Источники: См. Шаблон. | |||||||
Медицинское использование
Эстрадиол используется как медикамент, прежде всего в гормональная терапия за менопаузальный симптомы а также заместительная терапия трансгендерными гормонами.[74]
Химия
Эстрадиол - это эстран стероидный препарат.[74] Он также известен как 17β-эстрадиол (чтобы отличить его от 17α-эстрадиол) или в виде эстра-1,3,5 (10) -триен-3,17β-диола. Имеет два гидроксильные группы, один в позиции C3, другой в позиции 17β, а также три двойные связи в А звенеть. Из-за наличия двух гидроксильных групп эстрадиол часто обозначают сокращенно E2. Структурно родственные эстрогены, эстрон (E1), эстриол (E3) и эстетрол (E4) имеют одну, три и четыре гидроксильные группы соответственно.
История
Открытие эстрогена обычно приписывают Американец ученые Эдгар Аллен и Эдвард А. Дойзи.[75][76] В 1923 году они наблюдали, что закачка жидкости из свинья фолликулы яичников произведено пубертатный- и течкаизменения типа (в том числе вагинальный, матка, и молочная железа изменения и сексуальная восприимчивость) в сексуально незрелый, овариэктомия мыши и крысы.[75][76][77] Эти данные продемонстрировали существование гормон который производится яичники и участвует в половое созревание и воспроизведение.[75][76][77] Во время открытия Аллен и Дойзи не называли гормон, а просто называли его «гормоном яичников» или «фолликулярным гормоном»;[76] другие называли это по-разному феминин, фолликулин, менформон, теликинин, и Эмменин.[78][79] В 1926 году Паркс и Беллерби ввели термин эстрин описать гормон на основе того, что он вызывает течку у животных.[80][78] Estrone был выделен и очищен независимо Алленом и Дойзи и Немецкий ученый Адольф Бутенандт в 1929 г. и эстриол был изолирован и очищен Маррианом в 1930 году; они были первыми идентифицированными эстрогенами.[76][81][82]
Эстрадиол, самый мощный из трех основных эстрогенов, был идентифицирован последним из трех.[76][80] Он был открыт Швенком и Хильдебрантом в 1933 году, которые синтезированный это через снижение эстрона.[76] Впоследствии Эстрадиол был выделен и очищен из яичников свиноматок Дойзи в 1935 г. химическая структура определяется одновременно,[83] и упоминался по-разному как дигидротеелин, дигидрофолликулин, дигидрофолликулярный гормон, и дигидроксиэстрин.[76][84][85] В 1935 году название эстрадиол и срок эстроген были официально учреждены Комитетом по половым гормонам Организации здравоохранения Лига Наций; за этим последовали названия эстрон (который первоначально назывался теелин, прогинон, фолликулин и кетогидроксиэстрин) и эстриол (первоначально назывался теелол и тригидроксиэстрин), которые были введены в 1932 году на первом заседании Международной конференции по стандартизации половых гормонов в Лондон.[80][86] После его открытия частичный синтез эстрадиола из холестерин был разработан Inhoffen и Hohlweg в 1940 году, а полный синтез был разработан Аннером и Мишером в 1948 году.[76]
Общество и культура
Этимология
Название эстрадиол происходит от эстра-, Gk. οἶστρος (Oistros, буквально означающее "воодушевление или вдохновение"),[87] который относится к эстран стероидный препарат звенеть система и -диол, химический термин и суффикс, указывающий, что соединение является типом алкоголь несущий два гидроксил группы.
Рекомендации
- ^ Ford SM, Roach SS (7 октября 2013 г.). Вводная клиническая фармакология Роуча. Липпинкотт Уильямс и Уилкинс. С. 525–. ISBN 978-1-4698-3214-2.
- ^ Hochadel M (1 апреля 2015 г.). Справочник лекарств Мосби для медицинских работников. Elsevier Health Sciences. стр. 602–. ISBN 978-0-323-31103-8.
- ^ а б c d е Станчик Ф.З., Арчер Д.Ф., Бхавнани Б.Р. (июнь 2013 г.). «Этинилэстрадиол и 17β-эстрадиол в комбинированных пероральных контрацептивах: фармакокинетика, фармакодинамика и оценка риска». Контрацепция. 87 (6): 706–27. Дои:10.1016 / j.contraception.2012.12.011. PMID 23375353.
- ^ Фальконе Т., Херд WW (2007). Клиническая репродуктивная медицина и хирургия. Elsevier Health Sciences. С. 22–. ISBN 978-0-323-03309-1.
- ^ Прайс TM, Блауэр К.Л., Хансен М., Станчик Ф., Лобо Р., Бейтс Г.В. (март 1997 г.). «Фармакокинетика однократной дозы сублингвального по сравнению с пероральным введением микронизированного 17-бета-эстрадиола». Акушерство и гинекология. 89 (3): 340–5. Дои:10.1016 / S0029-7844 (96) 00513-3. PMID 9052581. S2CID 71641652.
- ^ Нонтон М., Аль-Хадити А.Ф., Брауэрс-младший, Арчер Д.Ф. (2006). «Гель эстрадиола: обзор фармакологии, фармакокинетики, эффективности и безопасности у женщин в менопаузе». Менопауза. 13 (3): 517–27. Дои:10.1097 / 01.gme.0000191881.52175.8c. PMID 16735950. S2CID 42748448.
- ^ Райан К.Дж. (август 1982 г.). «Биохимия ароматазы: значение для женской репродуктивной физиологии». Исследования рака. 42 (8 Прил.): 3342s – 3344s. PMID 7083198.
- ^ Mechoulam R, Brueggemeier RW, Denlinger DL (сентябрь 1984 г.). «Эстрогены у насекомых». Клеточные и молекулярные науки о жизни. 40 (9): 942–944. Дои:10.1007 / BF01946450. S2CID 31950471.
- ^ Озон Р. (1972). «Эстрогены у рыб, амфибий, рептилий и птиц». В Idler DR (ред.). Стероиды у позвоночных, не являющихся млекопитающими. Оксфорд: Elsevier Science. С. 390–414. ISBN 978-0323140980.
- ^ Салдана, Колин Дж., Люк Ремедж-Хили и Барни А. Шлингер. «Передача сигналов синаптокрина: синтез стероидов и действие в синапсе». Эндокринные обзоры 32.4 (2011): 532–549.
- ^ а б c Макмиллан Дж. А., Фейгин Р. Д., ДеАнгелис С., Джонс М. Д. (2006). Педиатрия Оски: принципы и практика. Липпинкотт Уильямс и Уилкинс. С. 550–. ISBN 978-0-7817-3894-1.
- ^ а б c Крейг CR, Stitzel RE (2004). Современная фармакология с клиническим применением. Липпинкотт Уильямс и Уилкинс. С. 706–. ISBN 978-0-7817-3762-3.
- ^ Виктор Р. Приди (2 декабря 2011 г.). Справочник по мониторингу роста и роста в условиях здоровья и болезней. Springer Science & Business Media. С. 2661–. ISBN 978-1-4419-1794-2.
- ^ Карро С., Ламбар С., Делаланд С., Дени-Галеро I, Билинска Б., Бургиба С. (апрель 2003 г.). «Экспрессия ароматазы и роль эстрогенов в мужских гонадах: обзор». Репродуктивная биология и эндокринология. 1: 35. Дои:10.1186/1477-7827-1-35. ЧВК 155680. PMID 12747806.
- ^ Пентикяйнен В., Эрккиля К., Суомалайнен Л., Парвинен М., Дункель Л. (май 2000 г.). «Эстрадиол действует как фактор выживания половых клеток в семенниках человека in vitro». Журнал клинической эндокринологии и метаболизма. 85 (5): 2057–67. Дои:10.1210 / jcem.85.5.6600. PMID 10843196.
- ^ Sharpe RM, Skakkebaek NE (май 1993 г.). «Участвуют ли эстрогены в падении количества сперматозоидов и нарушениях мужских репродуктивных путей?». Ланцет. 341 (8857): 1392–5. Дои:10.1016 / 0140-6736 (93) 90953-Е. PMID 8098802. S2CID 33135527.
- ^ Handelsman DJ (2001). «Эстрогены и падающая сперма имеет значение». Размножение, фертильность и развитие. 13 (4): 317–24. Дои:10.1071 / rd00103. PMID 11800170.
- ^ Фиш Х, Гольдштейн Р (2003). «Экологические эстрогены и количество сперматозоидов» (PDF). Чистая и прикладная химия. 75 (11–12): 2181–2193. Дои:10.1351 / pac200375112181. S2CID 11068097.
- ^ Раман Дж. Д., Шлегель П. Н. (февраль 2002 г.). «Ингибиторы ароматазы при мужском бесплодии». Журнал урологии. 167 (2 Пет 1): 624–9. Дои:10.1016 / S0022-5347 (01) 69099-2. PMID 11792932.
- ^ Высоцак Дж., Грэм Дж. М. (октябрь 2006 г.). «Синдром Клайнфельтера и анеуплоидии других половых хромосом». Журнал редких заболеваний Orphanet. 1 (42): 42. Дои:10.1186/1750-1172-1-42. ЧВК 1634840. PMID 17062147.
- ^ Vanderschueren D, Laurent MR, Claessens F, Gielen E, Lagerquist MK, Vandenput L, et al. (Декабрь 2014 г.). «Действия половых стероидов в мужской кости». Эндокринные обзоры. 35 (6): 906–60. Дои:10.1210 / er.2014-1024. ЧВК 4234776. PMID 25202834.
- ^ Карани К., Цин К., Симони М., Фаустини-Фустини М., Змеиный С., Бойд Дж. И др. (Июль 1997 г.). «Влияние тестостерона и эстрадиола на человека с дефицитом ароматазы». Медицинский журнал Новой Англии. 337 (2): 91–5. Дои:10.1056 / NEJM199707103370204. PMID 9211678.
- ^ Олбрайт Ф, Смит PH, Ричардсон AM (31 мая 1941 г.). «Постменопаузальный остеопороз: его клинические особенности». JAMA. 116 (22): 2465–2474. Дои:10.1001 / jama.1941.02820220007002.
- ^ а б c d е ж грамм час Рейн-Феннинг, штат Нью-Джерси, член парламента Бринката, Маскат-барон Y (2003). «Старение кожи и менопауза: значение для лечения». Американский журнал клинической дерматологии. 4 (6): 371–8. Дои:10.2165/00128071-200304060-00001. PMID 12762829. S2CID 20392538.
- ^ а б c d е ж грамм час Holzer G, Riegler E, Hönigsmann H, Farokhnia S, Schmidt JB, Schmidt B (сентябрь 2005 г.). «Эффекты и побочные эффекты 2% крема с прогестероном на коже женщин в пери- и постменопаузе: результаты двойного слепого рандомизированного исследования с контролем носителя». Британский журнал дерматологии. 153 (3): 626–34. Дои:10.1111 / j.1365-2133.2005.06685.x. PMID 16120154. S2CID 6077829.
- ^ Бел С., Видманн М., Трапп Т., Хольсбоер Ф. (ноябрь 1995 г.). «17-бета-эстрадиол защищает нейроны от вызванной окислительным стрессом гибели клеток in vitro». Сообщения о биохимических и биофизических исследованиях. 216 (2): 473–82. Дои:10.1006 / bbrc.1995.2647. PMID 7488136.
- ^ Meethal SV, Liu T, Chan HW, Ginsburg E, Wilson AC, Gray DN, Bowen RL, Vonderhaar BK, Atwood CS (август 2009 г.). «Идентификация регуляторной петли для синтеза нейростероидов: стероидогенный острый регуляторный белок-зависимый механизм с участием рецепторов оси гипоталамуса-гипофиза-гонад». Журнал нейрохимии. 110 (3): 1014–27. Дои:10.1111 / j.1471-4159.2009.06192.x. ЧВК 2789665. PMID 19493163.
- ^ Дума С.Л., Муж С., О'Доннелл М.Э., Барвин Б.Н., Вуденд А.К. (2005). «Расстройства настроения, связанные с эстрогенами: факторы репродуктивного жизненного цикла». Достижения в области сестринского дела. 28 (4): 364–75. Дои:10.1097/00012272-200510000-00008. PMID 16292022. S2CID 9172877.
- ^ Ласюк ГК, Хегадорен К.М. (октябрь 2007 г.). «Влияние эстрадиола на центральные серотонинергические системы и его связь с настроением у женщин». Биологические исследования для медсестер. 9 (2): 147–60. Дои:10.1177/1099800407305600. PMID 17909167. S2CID 37965502.
- ^ Hulshoff HE, Cohen-Kettenis PT, Van Haren NE, Peper JS, Brans RG, Cahn W., Schnack HG, Gooren LJ, Kahn RS (июль 2006 г.). «Смена пола меняет ваш мозг: влияние тестостерона и эстрогена на структуру мозга взрослого человека». Европейский журнал эндокринологии. 155 (Suppl_1): 107–114. Дои:10.1530 / eje.1.02248.
- ^ Harding CF (июнь 2004 г.). «Гормональная модуляция пения: гормональная модуляция мозга певчей птицы и певческое поведение». Летопись Нью-Йоркской академии наук. 1016 (1): 524–39. Bibcode:2004НЯСА1016..524Х. Дои:10.1196 / летопись.1298.030. PMID 15313793. S2CID 12457330. Архивировано из оригинал 27 сентября 2007 г.
- ^ Симерлы РБ (27 марта 2002 г.). «Запрограммирован для воспроизводства: организация и развитие половых диморфных цепей в переднем мозге млекопитающих» (PDF). Ежегодный обзор нейробиологии. 25: 507–36. Дои:10.1146 / annurev.neuro.25.112701.142745. PMID 12052919.
- ^ Гольдштейн И., Местон С.М., Дэвис С., Трейш А. (17 ноября 2005 г.). Женская сексуальная функция и дисфункция: исследование, диагностика и лечение. CRC Press. С. 205–. ISBN 978-1-84214-263-9.
- ^ Асеведо-Родригес А, Мани СК, Ханда Р.Дж. (2015). «Окситоцин и рецептор эстрогена β в головном мозге: обзор». Границы эндокринологии. 6: 160. Дои:10.3389 / fendo.2015.00160. ЧВК 4606117. PMID 26528239.
- ^ Булзоми П., Болли А., Галлуццо П., Леоне С., Акконсия Ф, Марино М. (январь 2010 г.). «Совместное введение нарингенина и 17-бета-эстрадиола предотвращает индуцированный гормонами рост раковых клеток человека». IUBMB Life. 62 (1): 51–60. Дои:10.1002 / iub.279. PMID 19960539. S2CID 7903757.
- ^ Sreeja S, Santhosh Kumar TR, Lakshmi BS, Sreeja S (июль 2012 г.). «Экстракт граната демонстрирует профиль селективного модулятора рецептора эстрогена в линиях опухолевых клеток человека и на моделях лишения эстрогена in vivo». Журнал пищевой биохимии. 23 (7): 725–32. Дои:10.1016 / j.jnutbio.2011.03.015. PMID 21839626.
- ^ Томас К.Г., Стром А., Линдберг К., Густафссон Дж. А. (июнь 2011 г.). «Рецептор эстрогена бета снижает выживаемость p53-дефектных раковых клеток после повреждения ДНК за счет нарушения передачи сигналов контрольной точки G check / M». Исследования и лечение рака груди. 127 (2): 417–27. Дои:10.1007 / s10549-010-1011-z. PMID 20623183. S2CID 6752694.
- ^ Коллинз П., Розано Г.М., Саррел П.М., Ульрих Л., Адамопулос С., Бил С.М., Макнил Дж. Г., Пул-Уилсон П.А. (июль 1995 г.). «17-бета-эстрадиол ослабляет вызванное ацетилхолином сужение коронарной артерии у женщин, но не у мужчин с ишемической болезнью сердца». Тираж. 92 (1): 24–30. Дои:10.1161 / 01.CIR.92.1.24. PMID 7788912.
- ^ Абдул Султан А., Вест Дж., Стефанссон О., Грейндж М. Дж., Тата Л. Дж., Флеминг К. М., Хьюмс Д., Людвигссон Дж. Ф. (ноябрь 2015 г.). «Определение венозной тромбоэмболии и измерение ее частоты с использованием шведских регистров здоровья: общенациональное когортное исследование беременных». BMJ Open. 5 (11): e008864. Дои:10.1136 / bmjopen-2015-008864. ЧВК 4654387. PMID 26560059.
- ^ Просниц Э. Р., Бартон М. (май 2014 г.). «Биология эстрогенов: новое понимание функции GPER и клинических возможностей». Молекулярная и клеточная эндокринология. 389 (1–2): 71–83. Дои:10.1016 / j.mce.2014.02.002. ЧВК 4040308. PMID 24530924.
- ^ Просниц Э. Р., Артерберн Дж. Б., Склар Л. А. (2007). «GPR30: рецептор эстрогена, связанный с G-белком». Мол. Клетка. Эндокринол. 265–266: 138–42. Дои:10.1016 / j.mce.2006.12.010. ЧВК 1847610. PMID 17222505.
- ^ Солтысик К., Чекай П. (апрель 2013 г.). «Мембранные рецепторы эстрогенов - альтернативный способ действия эстрогенов?». Журнал физиологии и фармакологии. 64 (2): 129–42. PMID 23756388.
- ^ Мицевич PE, Келли MJ (2012). «Регуляция функции гипоталамуса мембранными рецепторами эстрогена». Нейроэндокринология. 96 (2): 103–10. Дои:10.1159/000338400. ЧВК 3496782. PMID 22538318.
- ^ А. Лабхарт (6 декабря 2012 г.). Клиническая эндокринология: теория и практика. Springer Science & Business Media. С. 548–. ISBN 978-3-642-96158-8.
- ^ Сьюзан Такер Блэкберн (2007). Физиология матери, плода и новорожденного: клиническая перспектива. Elsevier Health Sciences. С. 43–. ISBN 978-1-4160-2944-1.
- ^ а б Джон Э. Холл (31 мая 2015 г.). Электронный учебник по медицинской физиологии Гайтона и Холла. Elsevier Health Sciences. С. 1043–. ISBN 978-0-323-38930-3.
- ^ Хэггстрём М, Ричфилд Д. (2014). «Схема путей стероидогенеза человека». WikiJournal of Медицина. 1 (1). Дои:10.15347 / wjm / 2014.005. ISSN 2002-4436.
- ^ Бор WF, Boulpaep EL (2003). Медицинская физиология: клеточный и молекулярный подход. Elsevier / Saunders. п. 1300. ISBN 978-1-4160-2328-9.
- ^ Mutschler E, Schäfer-Korting M (2001). Arzneimittelwirkungen (на немецком языке) (8-е изд.). Штутгарт: Wissenschaftliche Verlagsgesellschaft. С. 434, 444. ISBN 978-3-8047-1763-3.
- ^ а б c d Шломо Мелмед (1 января 2016 г.). Учебник эндокринологии Уильямса. Elsevier Health Sciences. С. 710–. ISBN 978-0-323-29738-7.
- ^ а б Маркус Р., Фельдман Д., Демпстер Д. В., Лаки М., Коли Дж. А. (13 июня 2013 г.). Остеопороз. Академическая пресса. стр. 331–. ISBN 978-0-12-398252-0.
- ^ Wu CH, Motohashi T, Abdel-Rahman HA, Flickinger GL, Михаил Г. (август 1976 г.). «Свободный и связанный с белками бета-эстрадиол-17 в плазме во время менструального цикла». Журнал клинической эндокринологии и метаболизма. 43 (2): 436–45. Дои:10.1210 / jcem-43-2-436. PMID 950372.
- ^ Ченг Ц.Н., Шу И, Лю Ц.и., Ван Л.С., Оу-Ян Д.С., Чжоу Х.Х. (февраль 2001 г.). «Роль цитохрома P450 в метаболизме эстрадиола in vitro». Acta Pharmacologica Sinica. 22 (2): 148–54. PMID 11741520.
- ^ Ли AJ, Cai MX, Thomas PE, Conney AH, Zhu BT (август 2003 г.). «Характеристика окислительных метаболитов 17бета-эстрадиола и эстрона, образованных 15 селективно экспрессируемыми изоформами человеческого цитохрома p450». Эндокринология. 144 (8): 3382–98. Дои:10.1210 / en.2003-0192. PMID 12865317.
- ^ Эттель М., Шиллингер Э. (6 декабря 2012 г.). Эстрогены и антиэстрогены I: физиология и механизмы действия эстрогенов и антиэстрогенов. Springer Science & Business Media. С. 235–237. ISBN 978-3-642-58616-3.
- ^ Эттель М., Шиллингер Э. (6 декабря 2012 г.). Эстрогены и антиэстрогены II: фармакология и клиническое применение эстрогенов и антиэстрогенов. Springer Science & Business Media. С. 268, 271. ISBN 978-3-642-60107-1.
- ^ а б Дорфман, Ральф I. (1961). «Метаболизм стероидных гормонов». Радиоактивные изотопы в физиологической диагностике и терапии / Künstliche Radioaktive Isotope in Physiologie Diagnostik und Therapie. С. 1223–1241. Дои:10.1007/978-3-642-49761-2_39. ISBN 978-3-642-49477-2.
- ^ Сандберг А.А., Слаунвайт В.Р. (август 1957 г.). «Исследования фенольных стероидов на людях. II. Метаболическая судьба и гепато-билиарно-кишечная циркуляция C14-эстрона и C14-эстрадиола у женщин». J. Clin. Вкладывать деньги. 36 (8): 1266–78. Дои:10.1172 / JCI103524. ЧВК 1072719. PMID 13463090.
- ^ http://www.ilexmedical.com/files/PDF/Estradiol_ARC.pdf
- ^ а б c d е Беккер Дж. Б., Беркли К. Дж., Гири Н., Хэмпсон Э, Герман Дж. П., Young E (4 декабря 2007 г.). Половые различия в мозге: от генов к поведению. Издательство Оксфордского университета. С. 64–. ISBN 978-0-19-804255-6.
Уровни эстрадиола минимальны в первые дни фолликулярной фазы, но увеличивающиеся концентрации попадают в общую циркуляцию крови по мере созревания фолликула. Наивысшие уровни достигаются примерно за 24-48 часов до пика ЛГ. Фактически, предовуляторный пик эстрадиола представляет собой его самую высокую концентрацию в течение всего менструального цикла. Концентрации в сыворотке в это время обычно составляют около 130–200 пг / мл, но у некоторых женщин могут быть достигнуты такие высокие концентрации, как 300–400 пг / мл. После кратковременного падения в связи с овуляцией секреция эстрадиола восстанавливается за счет продукции желтым телом во время лютеиновой фазы. Уровни плато около 100–150 пг / мл (Abraham, 1978; Thorneycroft et al., 1971) чаще всего наблюдаются в период от -10 до -5 дней до начала менструации. По мере регресса желтого тела уровень эстрадиола падает, постепенно у некоторых женщин и резко у других, в течение последних нескольких дней лютеиновой фазы. Это знаменует начало менструации, отслаивание эндометрия. Уровень эстрадиола в сыворотке крови во время менструации составляет примерно 30–50 пг / мл. (Источник.)
- ^ а б c Штраус Дж. Ф., Барбьери Р. Л. (2009). Репродуктивная эндокринология Йена и Яффе: физиология, патофизиология и клиническое управление. Elsevier Health Sciences. С. 807–. ISBN 978-1-4160-4907-4.
В большинстве лабораторий уровни эстрадиола в сыворотке крови колеблются от 20 до 80 пг / мл во время ранней и средней фолликулярной фазы менструального цикла и достигают максимума от 200 до 500 пг / мл во время преовуляторного всплеска. Во время средней ягодичной фазы уровень эстрадиола в сыворотке колеблется от 60 до 200 пг / мл.
- ^ а б c Кристиан С., фон Шульц Б. (15 марта 1994 г.). Заместительная гормональная терапия: стандартизованные или индивидуально адаптированные дозы?. CRC Press. С. 60–. ISBN 978-1-85070-545-1.
Уровни эстрадиола в плазме колеблются от 40 до 80 пг / мл в течение 1-й недели цикла яичников (ранняя фолликулярная фаза) и от 80 до 300 пг / мл в течение 2-й недели (средне- и поздняя фолликулярная фаза, включая периовуляторный пик). Затем в течение 3-й и 4-й недель эстрадиол колеблется от 100 до 150 пг / мл (ранняя и средняя лютеиновая фаза) до 40 пг / мл за несколько дней до менструации (поздняя лютеиновая фаза). Средний интегрированный уровень эстрадиола в течение полного 28-дневного нормального цикла составляет около 80 пг / мл.
- ^ Джеймсон Дж. Л., Де Гроот Л. Дж. (18 мая 2010 г.). Эндокринология: взрослая и детская. Elsevier Health Sciences. С. 2812–. ISBN 978-1-4557-1126-0.
Средний цикл: 150-750 пг / мл
- ^ Hay ID, Wass JA (26 января 2009 г.). Клиническая эндокринная онкология. Джон Вили и сыновья. стр. 623–. ISBN 978-1-4443-0023-9.
В середине цикла: 110-330 пг / мл
- ^ Роберт Ф. Донс (12 июля 1994 г.). Руководство по эндокринному и метаболическому тестированию. CRC Press. С. 8–. ISBN 978-0-8493-7657-3.
Овуляторная: 200-400 пг / мл.
- ^ Нотеловиц М., ван Кип П.А. (6 декабря 2012 г.). Климактерический период в перспективе: материалы Четвертого Международного конгресса по менопаузе, проходившего в Лейк-Буэна-Виста, Флорида, 28 октября - 2 ноября 1984 г.. Springer Science & Business Media. С. 397–. ISBN 978-94-009-4145-8.
[...] после менопаузы уровни циркулирующего эстрадиола снижаются со среднего значения в предменопаузе 120 пг / мл до 13 пг / мл.
- ^ а б Müller EE, MacLeod RM (6 декабря 2012 г.). Нейроэндокринные перспективы. Springer Science & Business Media. стр. 121–. ISBN 978-1-4612-3554-5.
[...] [в пременопаузе] средняя концентрация [эстрадиола] 150 пг / мл [...]
- ^ Sayed Y, Taxel P (декабрь 2003 г.). «Применение терапии эстрогенами у мужчин». Текущее мнение в фармакологии. 3 (6): 650–4. Дои:10.1016 / j.coph.2003.07.004. PMID 14644018.
- ^ а б «Анализ крови на эстрадиол: Медицинская энциклопедия MedlinePlus». medlineplus.gov. Получено 6 мая 2019.
- ^ а б c d е ж грамм час я j GPNotebook - контрольный диапазон (эстрадиол) Проверено 27 сентября 2009 г.
- ^ а б Значения, взятые с 1 дня после всплеска ЛГ: Стрикер Р., Эберхарт Р., Чевайллер М.С., Куинн Ф.А., Бишоф П., Стрикер Р. (2006). «Установление подробных эталонных значений лютеинизирующего гормона, фолликулостимулирующего гормона, эстрадиола и прогестерона во время различных фаз менструального цикла на анализаторе Abbott ARCHITECT». Клиническая химия и лабораторная медицина. 44 (7): 883–7. Дои:10.1515 / CCLM.2006.160. PMID 16776638. S2CID 524952. как PDF
- ^ а б c d Общая сумма умножена на 0,022 согласно 2,2%, представленной в: Wu CH, Motohashi T, Abdel-Rahman HA, Flickinger GL, Михаил Г. (август 1976 г.). «Свободный и связанный с белками бета-эстрадиол-17 в плазме во время менструального цикла». Журнал клинической эндокринологии и метаболизма. 43 (2): 436–45. Дои:10.1210 / jcem-43-2-436. PMID 950372.[оригинальное исследование?]
- ^ Хэггстрем, Микаэль (2014). «Референсные диапазоны для эстрадиола, прогестерона, лютеинизирующего гормона и фолликулостимулирующего гормона во время менструального цикла». WikiJournal of Медицина. 1 (1). Дои:10.15347 / wjm / 2014.001. ISSN 2002-4436.
- ^ а б Kuhl H (август 2005 г.). «Фармакология эстрогенов и прогестагенов: влияние разных путей введения». Климактерический. 8 Дополнение 1: 3–63. Дои:10.1080/13697130500148875. PMID 16112947. S2CID 24616324.
- ^ а б c Loriaux DL, Loriaux L (14 марта 2016 г.). Биографическая история эндокринологии. Джон Вили и сыновья. С. 345–. ISBN 978-1-119-20246-2.
- ^ а б c d е ж грамм час я Лауритцен С., Стадд Дж. У. (22 июня 2005 г.). Текущее лечение менопаузы. CRC Press. С. 44–. ISBN 978-0-203-48612-2.
- ^ а б Аллен Э., Дойзи Э.А. (1923). «Гормон яичников». Журнал Американской медицинской ассоциации. 81 (10): 819. Дои:10.1001 / jama.1923.02650100027012. ISSN 0002-9955.
- ^ а б Грун Дж. Г., Казер Р. Р. (11 ноября 2013 г.). Гормональная регуляция менструального цикла: эволюция представлений. Springer Science & Business Media. С. 69–73. ISBN 978-1-4899-3496-3.
- ^ Ньюерла, Герхард Дж. (1944). «История открытия и выделения женских половых гормонов». Медицинский журнал Новой Англии. 230 (20): 595–604. Дои:10.1056 / NEJM194405182302001. ISSN 0028-4793.
- ^ а б c Фриц М.А., Сперофф Л. (28 марта 2012 г.). Клиническая гинекологическая эндокринология и бесплодие. Липпинкотт Уильямс и Уилкинс. С. 750–. ISBN 978-1-4511-4847-3.
- ^ Фриц Ф. Парл (2000). Эстрогены, рецепторы эстрогенов и рак груди. IOS Press. С. 4–. ISBN 978-0-9673355-4-4.
- ^ Sartorelli AC, Johns DG (27 ноября 2013 г.). Противоопухолевые препараты и иммунодепрессанты. Springer Science & Business Media. С. 104–. ISBN 978-3-642-65806-8.
- ^ Shoupe D, Haseltine FP (6 декабря 2012 г.). Контрацепция. Springer Science & Business Media. С. 2–. ISBN 978-1-4612-2730-4.
- ^ MacCorquodale DW, Thayer SA, Doisy EA (1935). «Кристаллический фолликулярный гормон яичников». Экспериментальная биология и медицина. 32 (7): 1182. Дои:10.3181 / 00379727-32-8020P. ISSN 1535-3702. S2CID 83557813.
- ^ Химические вещества, обнаруженные в биологических средах человека: база данных. Отдел проектирования и разработки, Отдел исследований и анализа, Управление интеграции программ и информации, Управление пестицидов и токсичных веществ, Агентство по охране окружающей среды. 1981. С. 114–.
- ^ Энн Фаусто-Стерлинг (2000). Определение пола тела: гендерная политика и конструирование сексуальности. Основные книги. стр.189–. ISBN 978-0-465-07714-4.
- ^ «Инструмент для изучения греческого слова: oistros». Цифровая библиотека Персея. Получено 28 декабря 2011.


