WikiDer > Иттербий (III) хлорид
Эта статья ведущий раздел не адекватно подвести итог ключевые моменты его содержания. Пожалуйста, подумайте о расширении интереса до предоставить доступный обзор обо всех важных аспектах статьи. (Сентябрь 2013) |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Иттербий (III) хлорид | |
| Идентификаторы | |
3D модель (JSmol) | |
| ChemSpider | |
| ECHA InfoCard | 100.030.715 |
| |
| |
| Свойства | |
| YbCl3 | |
| Молярная масса | 279,40 г / моль |
| Внешность | белый порошок |
| Плотность | 4,06 г / см3 (твердый) |
| Температура плавления | 854 ° С (1569 ° F, 1127 К)[1] |
| Точка кипения | 1453 ° С (2647 ° F, 1726 К)[1] |
| 17 г / 100 мл (25 ° С) | |
| Структура | |
| Моноклиника, mS16 | |
| С12 / м1, №12 | |
| Родственные соединения | |
Другой анионы | Оксид иттербия (III) |
Другой катионы | Хлорид тербия (III), Лютеций (III) хлорид |
| Страница дополнительных данных | |
| Показатель преломления (п), Диэлектрическая постоянная (εр), так далее. | |
Термодинамический данные | Фазовое поведение твердое тело – жидкость – газ |
| УФ, ИК, ЯМР, РС | |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Иттербий (III) хлорид (YbCl3) представляет собой неорганическое химическое соединение. Реагирует с NiCl2 сформировать очень эффективный катализатор для восстановительное дегалогенирование из арилгалогениды.[2] Он ядовит при инъекции и умеренно токсичен при приеме внутрь. Это экспериментальный тератоген, Известно, что раздражать кожа и глаза. При нагревании до разложение он излучает токсичный пары Cl−.[3]
История
Иттербий, а лантаноид серии элемент, был открыт в 1878 году швейцарским химиком Жан-Шарль Галиссар де Мариньяк, назвавший элемент в честь города (Иттерби) в Швеция.[4] Первый синтез YbCl3 в литературе был написан Яном Хугшагеном в 1946 году.[5] YbCl3 теперь коммерчески доступный источник Yb3+ ионы и поэтому представляют значительный химический интерес.
Химические свойства
Валентная электронная конфигурация Yb+3 (из YbCl3) равно 4ж135s25п6, что имеет решающее значение для химического поведения Yb+3. Также размер Yb+3 определяет его каталитическое поведение и биологические применения. Например, в то время как Ce+3 и Yb+3 иметь один непарный ж электрон, Ce+3 намного больше, чем Yb+3 потому что лантаноиды становятся намного меньше с увеличением эффективного ядерного заряда в результате ж электроны не так хорошо защищены, как d электроны.[4] Такое поведение известно как сокращение лантаноидов. Небольшой размер Yb+3 обеспечивает быстрое каталитическое поведение и атомный радиус (0,99 Å), сравнимый со многими биологически важными ионами.[4]
Термодинамические свойства этого химического вещества в газовой фазе определить сложно, поскольку химическое вещество может диспропорционировать с образованием [YbCl6]−3 или димеризовать.[6] Yb2Cl6 была обнаружена масс-спектрометрией с электронным ударом (EI) как (Yb2Cl5+).[6] Дополнительные сложности при получении экспериментальных данных возникают из-за множества низколежащих ж-d и ж-ж электронные переходы.[7] Несмотря на эти проблемы, термодинамические свойства YbCl3 были получены и C3В симметрия группа была назначена на основе четырех активных инфракрасных колебаний.[7]
Подготовка
YbCl3 готовится из Yb2О3 с высокой температурой четыреххлористый углерод газ[8] или горячий соляная кислота с последующей сушкой при высокой температуре.[9]
- 2 Yb2О3 + 3 CCl4(грамм) → 4 YbCl3(s) + 3 СО2(грамм)
- Yb2О3 + 6 HCl(грамм) → 2 YbCl3(s) + 3 часа2О
На практике[требуется разъяснение] есть способы лучше приготовить YbCl3 для лабораторного использования. Водный HCl /хлорид аммония маршрут[требуется разъяснение] бесхитростный[требуется разъяснение] но очень эффективный. Альтернативно гидратированный YbCl3 могут быть обезвожены с использованием различных реагентов, в частности триметилсилилхлорид. Были опубликованы и другие методы, в том числе взаимодействие мелкодисперсного порошка металла с хлорид ртути при высокой температуре в герметичной тубе.[нужна цитата] Различные способы получения сольватированного YbCl3 было сообщено[нужна цитата] включая реакцию металла с различными галоидоуглероды в присутствии донорного растворителя, такого как THF, или дегидратация гидратированного хлорида с использованием триметилсилила или тионилхлоридснова в растворителе, таком как ТГФ.
Использует
Катализ
YbCl3, с одним неспаренный электрон, действует как Кислота Льюиса чтобы заполнить 4ж орбитальный. Кислотная природа YbCl по Льюису3 позволяет YbCl3 для координации (обычно как [YbCl2]+) в переходные состояния катализировать алкилирование реакции, такие как альдольная реакция[10] и Реакция Пикте-Шпенглера.[11]
- Альдольная реакция
Альдольная реакция - это универсальная реакция в синтетической органической химии. YbCl3 служит катализатором кислоты Льюиса, который помогает Pd(0) катализированный декарбоксилатный альдольная реакция между кетоном энолировать и альдегид. Переходные состояния А и B показать метод координации соли иттербия как кислоты Льюиса.[10] Для изображенной реакции декарбоксилирования альдола с R = трет-бутил и R ’= - (CH2)2Ph, выходы реакции показывают YbCl3 является эффективным катализатором кислоты Льюиса:
| Металлическая соль[10] | % доходности 2 |
|---|---|
| FeCl3 | 40 |
| ZnCl2 | 68 |
| CuCl2 | 40 |
| LaCl3 | 60 |
| YbCl3 | 93 |
- Реакция Пикте-Шпенглера
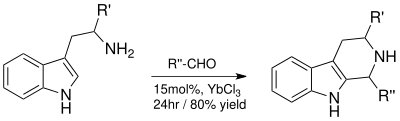
Реакция Пикте-Шпенглера дает ценный тетрагидро-β-карболин кольцевая система, которая позже может быть использована для синтетически полученного индола алкалоиды.[11] Катализируемая кислотой Льюиса реакция с YbCl3 дает превосходные выходы и сокращает время реакции с четырех дней до 24 часов.[11]
- Этерификация
Небольшой размер Yb3+ обеспечивает быстрый катализ, но за счет селективности. Например, моно-ацетилирование измезо-1,2-диолы являются самыми быстрыми (2 часа) с YbCl3, но хемоселективность моноацетилированного продукта низкая (50%) по сравнению с CeCl3 (23ч, 85%).[12]
- Ацетализация
Хлорид иттербия (III) - мощный катализатор образования ацетали с использованием триметила ортоформиат.[13] По сравнению с хлорид церия (III) и хлорид эрбия (III), соль иттербия оказалась наиболее эффективной. Превосходные выходы достигаются из различных альдегидов в течение нескольких минут при комнатной температуре, как в приведенном выше примере с участием чувствительного к кислоте альдегида.
Биология
YbCl3 является Реагент сдвига ЯМР который вызывает различные резонансы с ядрами, контактирующими с YbCl3 по сравнению с ядрами, не контактирующими со сдвигающим реагентом.[14] Обычно парамагнитные соединения, такие как (лантаноид)+3 ion, желательны сдвиговые реагенты.[14] На биологию мембран большое влияние оказал YbCl3, где39K+ и23Na+ движение ионов имеет решающее значение для установления электрохимических градиентов.[14] Передача нервных сигналов - фундаментальный аспект жизни, который можно исследовать с помощью YbCl.3 с использованием методов ЯМР. YbCl3 может также использоваться в качестве зонда для ионов кальция аналогично зонду для ионов натрия.[15]
YbCl3 также используется для отслеживания пищеварения у животных. Некоторые добавки к корму для свиней, такие как пробиотики, можно добавлять как в твердый корм, так и в питьевые жидкости. YbCl3 путешествует с твердой пищей и, следовательно, помогает определить, какая фаза питания идеально подходит для включения пищевой добавки.[16] YbCl3 концентрация определяется количественно масс-спектрометрия с индуктивно связанной плазмой с точностью до 0,0009 мкг / мл.[4] YbCl3 концентрация в зависимости от времени дает скорость потока твердых частиц в пищеварении животного. YbCl не вредит животному.3 поскольку YbCl3 просто выводится с фекалиями, и у мышей не наблюдалось изменений массы тела, веса органов или уровней гематокрита.[15]
Каталитическая природа YbCl3 также находит применение в микрочипах ДНК или так называемых «чипах» ДНК.[17] YbCl3 привело к увеличению в 50–80 раз флуоресцеин включение в ДНК-мишень, которое может произвести революцию в обнаружении инфекционных заболеваний (например, в экспресс-тестах на туберкулез).[17]
использованная литература
- ^ а б Уолтер Бененсон; Джон В. Харрис; Хорст Штёкер (2002). Справочник по физике. Springer. п. 781. ISBN 0-387-95269-1.
- ^ Zhang, Y. et al. Synth. Commun. 27, 4327, (1997)
- ^ «Хлорид иттербия; трихлорид иттербия; хлорид иттербия (III), хлорид иттербия (YbCl3), словарь - Guidechem.com». www.guidechem.com. Получено 2016-11-30.
- ^ а б c d Эванс, К. Биохимия лантаноидов; Пленум: Нью-Йорк, 1990.
- ^ Hoogschagen, J. (1946). «Поглощение света в ближней инфракрасной области растворов празеодима, самария и иттербия». Physica. 11 (6): 513–517. Bibcode:1946Phy .... 11..513H. Дои:10.1016 / S0031-8914 (46) 80020-X.
- ^ а б Червонный, А.Д .; Червонная, Н.А. (2004). «Термодинамические свойства хлоридов иттербия». Русь. J. Inorg. Chem. (Англ. Пер.). 49 (12): 1889–1897.
- ^ а б Засорин, Э. (1988). Русь. J. Phys. Chem. (Англ. Пер.). 62 (4): 441–447. Отсутствует или пусто
| название =(Помогите) - ^ Горюшкин, В.Ф .; Залымова, С.А .; Пошевнева, А. (1990). Русь. J. Inorg. Chem. (Англ. Пер.). 35 (12): 1749–1752. Отсутствует или пусто
| название =(Помогите) - ^ Jörg, S .; Зайферт, Х.Дж. (1998). «Тройные хлориды в системах ACl / YbCl3 (A = Cs, Rb, K)». Термохимика Акта. 318 (1–2): 29–37. Дои:10.1016 / S0040-6031 (98) 00326-8.
- ^ а б c Lou, S .; Westbrook, J.A .; Schaus, S.E. (2004). «Декарбоксилирующие альдольные реакции аллилбета-кетоэфиров посредством гетеробиметаллического катализа». Журнал Американского химического общества. 126 (37): 11440–11441. Дои:10.1021 / ja045981k. PMID 15366881.
- ^ а б c Srinivasan, N .; Ганесан, А. (2003). «Высокоэффективные реакции Пикте-Шпенглера, катализируемые кислотой Льюиса, обнаруженные путем параллельного отбора». Chemical Communications (Кембридж, Англия) (7): 916–917. Дои:10.1039 / b212063a. PMID 12739676.
- ^ Кларк, П.А. (2002). «Селективное моноацилирование мезо- и С2-симметричных 1,3- и 1,4-диолов». Буквы Тетраэдра. 43 (27): 4761–4763. Дои:10.1016 / S0040-4039 (02) 00935-8.
- ^ Люш, Жан-Луи; Gemal, Андре Луис (1978). «Эффективный синтез ацеталей на основе хлоридов редкоземельных элементов». Журнал химического общества, химические коммуникации. 1978 (22): 976–977. Дои:10.1039 / c39780000976.
- ^ а б c Hayer, M.K .; Ридделл, Ф. (1984). «Сдвиг реагентов на 39К ЯМР». Неорганика Chimica Acta. 92 (4): L37 – L39. Дои:10.1016 / S0020-1693 (00) 80044-4.
- ^ а б Шинохара, А .; Chiba, M .; Инаба, Ю. (2006). «Сравнительное исследование поведения тербия, самария и иттербия, вводимых внутривенно мышам». Журнал сплавов и соединений. 408–412: 405–408. Дои:10.1016 / j.jallcom.2004.12.152.
- ^ Охаши, Й .; Umesaki, Y .; Ушида, К. (2004). "Переход пробиотических бактерий, Lactobacillus casei штамм Широта, в желудочно-кишечном тракте свиньи ». Международный журнал пищевой микробиологии. 96 (1): 61–66. Дои:10.1016 / j.ijfoodmicro.2004.04.001. PMID 15358506.
- ^ а б Браун, К. (2002). "Катализируемое ионами металлов алкилирование нуклеиновых кислот и фрагментация". Журнал Американского химического общества. 124 (27): 7950–7962. Дои:10.1021 / ja017746x. PMID 12095339.